概述
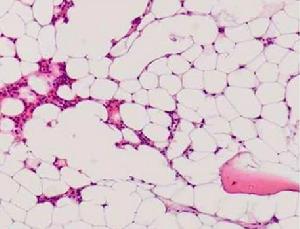 陣發性睡眠性血紅蛋白尿
陣發性睡眠性血紅蛋白尿陣發性睡眠性血紅蛋白尿(paroxysmal nocturnal hemoglobinuria,PNH),系獲得性的紅細胞膜缺陷引起的慢性血管內溶血,常睡眠時加重,可伴發作性血紅蛋白尿和全血細胞減少症。本病雖少見,但近年發病有增多趨勢。我國北方多於南方,半數以上發生在20-40歲青壯年,個別10歲以下及70歲以上。男性多於女性。我國患者的臨床表現與歐美例有所不同,起病多隱襲緩慢,以貧血、出血為首發症狀較多,以血紅蛋白尿起病者較少。個別以感染、血栓形成或再障表現,起病急驟。
臨床表現
典型的PNH以慢性血管內溶血,血紅蛋白尿,及含鐵血黃素尿為主要表現,但大多數患者常不典型,發病隱襲,病程遷延,病情輕重不一。發病高峰年齡在 20~40歲之間,個別發生兒童或老年,男性顯著多於女性。國內總結203例PNH患者,首發症狀為貧血占56.7%,血紅蛋白尿僅占12.8%,黃疸兼貧血占5.9%。
診斷
近來陣發性睡眠性血紅蛋白尿症(PNH)診斷與治療均有一些進展,涉及到PNH的FLAER診斷、肺動脈高壓以及Eulizumab和化療治療PNH。
流式細胞術診斷
流式細胞術是診斷PNH的金標準,可以對PNH血細胞進行定量分析。基本原理是抗原抗體反應。最常用的是抗CD55及CD59抗體,加入流式細胞儀後可以與細胞表面CD55及CD59特異性的結合。而未被CD55、CD59結合的細胞即為PNH細胞。通過顯色分析可以確定CD55ˉ、CD59ˉ的細胞數量。
隨著研究的不斷深入,人們已經注意到了傳統的流式細胞術對於PNH克隆檢測的局限性。MDS、細胞發育不全或炎症反應等都有可能導致膜蛋白的缺失,如CD14、CD16、CD55、CD59等不表達,這時若還是採用傳統的流式細胞術就會出現誤診的可能性。而FLAER白細胞分析法就避免了此種情況的發生。
FLAER能特異地與細胞膜上的GPI蛋白結合,在膜上形成孔洞而使細胞溶破。由於缺失GPI蛋白是PNH細胞的專有特性,可以用此法把PNH細胞和正常細胞區分開來,從而為PNH診斷提供一種簡便的方法。最近有文獻報導,以FLAER為基礎對粒細胞和單核細胞進行多參數分析能夠檢測到較小的PNH克隆,這種方法可以提高檢測的陽性率。主要原理是利用PNH的粒細胞和單核細胞缺乏CD45、CD33、CD14。在流式細胞儀中加入相應的抗體後,正常細胞可以與之結合,而PNH粒細胞和中性細胞由於缺乏相應抗原而不能與之結合,最後通過顯色分析確定PNH粒細胞和中性粒細胞的數量。在此項研究中收集了536例患者,將FLAER對白細胞的分析和CD59對紅細胞的分析進行了比較。結果發現採用FLAER分析法,有63例患者檢測到了PNH克隆,檢出率11.8%,並且克隆數都較大,不受溶血和輸血的影響;而傳統的CD59分析法只有33例患者被檢測出有PNH克隆,檢出率6.2%,檢測出的克隆數都較小,很容易受到溶血和輸血的影響。因此,FLAER對白細胞的分析能夠更可靠的反應PNH克隆的數量。此篇文獻還建議,對於疑似PNH患者的初篩應選擇FLAER分析法,CD59對紅細胞的分析應該在檢測到有PNH粒細胞和單核細胞克隆的基礎上再進行。這種做法既可靠又經濟。有少數PNH患者只有粒細胞表達異常,對於此種情況來說只能採用白細胞分析法才能檢測到PNH克隆,若此時採用紅細胞分析法只能導致錯誤的診斷。許多文獻已經報導了血栓事件的發生可能與PNH白細胞克隆數有關,PNH粒細胞大於50%,血栓形成的風險增加,此時應採取預防性抗凝治療。所以可以這樣理解,以FLAER為基礎的多參數分析法對白細胞檢出率的高敏感性能夠指導治療。
再障患者隨著病情的發展也可以檢測出PNH克隆,FLAER白細胞分析法的高敏感性對於監測AA患者病情的變化有著總要意義,可以較早的了解疾病所處階段,以調整治療方案。有文獻報導,再障患者檢測到PNH克隆後會影響到免疫抑制治療的效果。免疫抑制劑治療PNH+再障的6個月療效、5年無失敗生存率明顯好於PNH-再障患者。對於PNH患者異基因骨髓或幹細胞移植術後微小殘留病灶的檢測,FLAER白細胞分析法的意義更大。
治療
常規治療
 陣發性睡眠性血紅蛋白尿症
陣發性睡眠性血紅蛋白尿症常規治療主要是控制溶血發作,如右鏇糖酐、碳酸氫鈉、腎上腺皮質激素等免疫抑制劑,以及雄激素刺激血細胞生成。長期血紅蛋白尿可導致缺鐵。鐵劑可使活性氧產生,PNH細胞對氧化損傷很敏感,易誘發血紅蛋白尿。肯定缺鐵後應從小劑量開始治療,為常規劑量的1/3~1/10,仍有反應者應停用。輸血除能提高血紅蛋白,維持組織需氧,尚能抑制紅細胞生成,間接減少補體敏感的紅細胞。近來,PNH治療主要有以下進展:
Eulizumab
Eculizumab人源型抗補體C5單克隆抗體,補體C5是補體級聯反應中最後一個酶促反應底物,C5在C5轉化酶作用下裂解為C5a和C5b, C5b參與膜攻擊複合物(MAC)C5b-9的形成。Eculizumab是抑制末端補體成分活化的重組人源型單克隆抗體,能特異性與人末端補體蛋白C5 結合,通過抑制補體C5向C5a和C5b的裂解,阻斷炎症因子C5a的釋放及膜攻擊複合物C5b-9的組成。臨床研究
表明,該抗體對C5有高度親和力,能阻斷C5a和C5b-9的形成,並保護哺乳動物細胞不受C5b-9介導的損傷,完全阻斷補體介導的血細胞破壞。
Eulizumab可以降低PNH患者血壓,從而改善患者肺動脈高壓的情況。有文獻報導,大部分PNH患者血NT-proBNP水平較高,它是肺血管阻力增加、右心室舒張功能不全的標誌,最終會導致PH 的發生。用Eulizumab治療後,溶血、NO清除、血管張力、呼吸困難等症狀在2周內會得到明顯改善,同時高NT-proBNP水平也有所下降。可以認為PH的改善是由於溶血、NO消耗、肺血管阻力的快速下降,或者肺微血栓的迅速溶解的結果。在Eulizumab治療1-4周過程中,患者的血壓明顯下降,收縮壓中位改變為-10mmHg。已經發現患者NT-proBNP高水平、呼吸困難與肺動靜脈壓力升高高度相關。
Eulizumab還能夠使患者呼吸困難的症狀得到改善。呼吸困難是肺壓力增高的重要表現。 Anita Hill等觀察了Eulizumab對呼吸困難治療的療效,與安慰劑組相比實驗組患者呼吸困難明顯改善(P<0.001),大概2周左右出現療效,持續到實驗結束。值得注意的是患者呼吸困難的改善與血漿游離血紅蛋白的水平無關。血紅蛋白總水平在Eulizumab 26周的治療過程中並沒有發生改變。
Eulizumab能夠減少血栓的形成。血栓形成是PNH患者最常見的症狀,肺栓塞及肺微血栓形成也可以導致肺動脈高壓。為了確定Eulizumab對血栓形成的影響,Peter Hillmen等對195例患者進行了對照試驗,接受Eulizumab治療的患者血栓發生率從7.37%降至1.07%(P<0.01),而未接受Eulizumab治療的對照組血栓發生率從2.34%升至4.38%;接受抗凝治療的血栓發生率為10.61%,同樣的病人再接受Eulizumab 治療血栓的發生率降至0.62%(P<0.01)。說明抗凝治療不足以預防血栓的形成,而Eulizumab可顯著減少PNH病人血栓的發生率。
Eulizumab減少補體介導的溶血作用,使紅細胞的破壞減少,溶血依賴的輸血就會相應減少,從而提高患者的生活質量。
聯合化療
對於難治、復發的PNH患者還可以進行聯合化療。有文獻報導,予8例難治及復發的PNH患者化療方法,其中3例套用DA方案:柔紅黴素40mg靜滴,第 1、2天,20mg靜滴,第3天,阿糖胞苷100mg/d靜滴,共5天。5例使用HA方案:高三尖杉酯鹼2-3mg/d靜滴,共5天;阿糖胞苷100mg /d靜滴,共5天。同時給予基礎及支持治療。結果發現8例例患者化療均有效。治療後所有患者腎上腺糖皮質激素的用量較化療前減少66%-100%,中位數 75%;化療前用量為(62.9±19.1)mg/d,化療後(10.6±3.O)mg/d(P<0.01),2例已經脫離激素治療。7例患者化療前重度貧血,1例中度貧血,血紅蛋白濃度為(52.8±13.6)g/L,化療後2例進步,6例明顯進步,血紅蛋白濃度為(85.5±17.1)g /L(P<0.01)。8例患者中除1例從未輸過血外,6例患者化療後完全脫離輸血;另1例輸血間期延長。提示DA或HA方案化療能夠有效地減少 PNH克隆負荷,控制溶血,改善血常規,而且大大減少了激素的用量,無嚴重、致命的不良反應。
異基因造血幹細胞移植
這是目前唯一能夠治癒PNH的方法。BMT治療一般僅限於那些難治性、耐腎上腺皮質激素或有激素禁忌症的PNH患者。移植前要進行化療,只有在預處理中儘可能地清除PNH克隆,才能夠防止PNH復發。對於大多數患者目前還是以藥物治療為主。
抗凝治療
靜脈血栓是PNH最重要的併發症,主要在腔靜脈和顱靜脈,約50%的歐美PNH患者發生過靜脈血栓,且約1/3由於血栓致死。東方人較西方人更易罹患再生障礙貧血,PNH患者也以PNH/AA綜合徵表現多,溶血和血栓的表現要少些。PNH患者易形成血栓確切原因未知,但目前已知道GPI缺乏的血小板較正常血小板更易被補體激活。
由於一次靜脈血栓發生就可以對PNH患者的預後產生極大影響,已有建議在PNH患者中常規抗凝治療。回顧性研究分析表明,華法令能顯著降低血栓的形成,建議中性粒細胞中PNH克隆超過50%,血小板大於10萬/dL,無其他華法令禁忌症者考慮使用。關於抗血小板藥物,如阿司匹林的套用尚無研究報導。
總之,流式細胞技術在PNH的診斷中發揮著重要作用,只採用抗CD55和CD59抗體對紅系和粒系檢測的方法相對已較成熟,但對於那些只有粒系表達障礙的患者此種檢驗方法就存在局限性。FLAER為基礎的多參數分析彌補了這一不足,但目前還沒有統一診斷標準。在治療上主要是Eulizumab所引起的不良反應,常見的有頭痛、背痛、乏力、上呼吸道感染、單純性皰疹、便秘等。套用Eulizumab 的病人會出現腦膜炎球菌感染,因此在開始治療前2周要注射腦膜炎球菌疫苗。此外,在臨床套用過程中尚存在限制因素包括:①藥物相關因素:Eculizumab可顯著減少血管內溶血,但並不能治癒PNH,患者一旦套用Eculizumab,則需每兩周輸注一次直到患者去世或PNH自發消失(極少發生),若中斷治療,患者隨即出現溶血性PNH臨床症狀及其併發症;輸注次數頻繁,輸注計畫嚴格,長期套用不良反應不可預知和價格昂貴等。至於其對PH的影響,由於病例數有限,Eulizumab是否真的能夠逆轉PH還需要大量的臨床數據來證實。