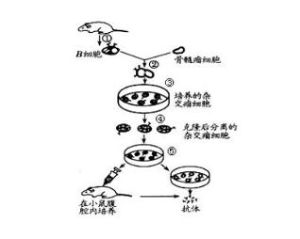
基本簡介
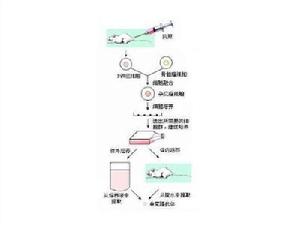 單克隆抗體製備流程
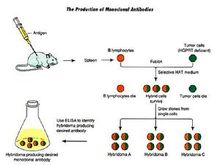
單克隆抗體製備流程1975年分子生物學家G.J.F.克勒和C.米爾斯坦在自然雜交技術的基礎上,創建立雜交瘤技術,他們把可在體外培養和大量增殖的小鼠骨髓瘤細胞與經抗原免疫後的純系小鼠脾細胞融合,成為雜交細胞系,既具有瘤細胞易於在體外無限增殖的特性,又具有抗體形成細胞的合成和分泌特異性抗體的特點。將這種雜交瘤作單個細胞培養,可形成單細胞系,即單克隆。利用培養或小鼠腹腔接種的方法,便能得到大量的、高濃度的、非常均一的抗體,其結構、胺基酸順序、特異性等都是一致的,而且在培養過程中,只要沒有變異,不同時間所分泌的抗體都能保持同樣的結構與機能。這種單克隆抗體是用其他方法所不能得到的。
這項新技術從根本上解決了在抗體製備中長期存在的特異性和可重複性問題,可用於探討①蛋白質的精細結構;②淋巴細胞亞群的表面新抗原;③組織相容性抗原;④激素和藥物的放射免疫(或酶免疫)分析;⑤腫瘤的定位和分類;⑥純化微生物和寄生蟲抗原;⑦免疫治療和與藥物結合的免疫-化學療法 (“飛彈”療法,利用單克隆抗體與靶細胞特異性結合,將藥物帶至病灶部位。因此,單克隆抗體可直接用於人類疾病的診斷、預防、治療以及免疫機制的研究,為人類惡性腫瘤的免疫診斷與免疫治療開闢了廣闊前景。
製備過程
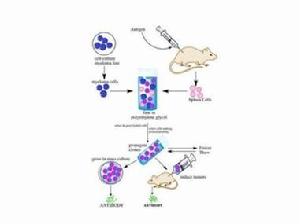
1、免疫動物 免疫動物是用目的抗原免疫小鼠,使小鼠產生致敏B淋巴細胞的 過程。 一般選用6-8周齡雌性Balb/c小鼠,按照預先制定的免疫方案進行免疫注射。 抗原通過血液循環或淋巴循環進入外周免疫器官,刺激相應B淋巴細胞克隆,使其活化、增殖,並分化成為致敏B淋巴細胞。
2、細胞融合 採用二氧化碳氣體處死小鼠,無菌操作取出脾臟,在平皿內擠壓研磨,製備脾細胞懸液。 將準備好的同系骨髓瘤細胞與小鼠脾細胞按一定比例混合,並加入促融合劑聚乙二醇。在聚乙二醇作用下,各種淋巴細胞可與骨髓瘤細胞發生融合,形成雜交瘤細胞。
3、選擇性培養 選擇性培養的目的是篩選融合的雜交瘤細胞,一般採用HAT選擇性培養基。在HAT培養基中,未融合的骨髓瘤細胞因缺乏次黃嘌呤-鳥嘌呤-磷酸核糖轉移酶,不能利用補救途徑合成DNA而死亡。 未融合的淋巴細胞雖具有次黃嘌呤-鳥嘌呤-磷酸核糖轉移酶,但其本身不能在體外長期存活也逐漸死亡。 只有融合的雜交瘤細胞由於從脾細胞獲得了次黃嘌呤鳥嘌呤磷酸核糖轉移酶,並具有骨髓瘤細胞能無限增殖的特性,因此能在HAT培養基中存活和增殖。
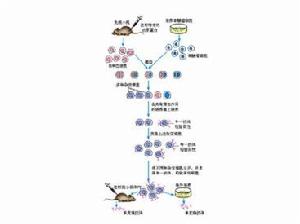 單克隆抗體製備流程
單克隆抗體製備流程4、雜交瘤陽性克隆的篩選與克隆化 在HAT培養基中生長的雜交瘤細胞,只有少數是分泌預定特異性單克隆抗體的細胞,因此,必須進行篩選和克隆化。通常採用有限稀釋法進行雜交瘤細胞的克隆化培養。採用靈敏、快速、特異的免疫學方法,篩選出能產生所需單克隆抗體的陽性雜交瘤細胞,並進行克隆擴增。經過全面鑑定其所分泌單克隆抗體的免疫球蛋白類型、亞類、特異性、親和力、識別抗原的表位及其分子量後,及時進行凍存。
5、單克隆抗體的大量製備 單克隆抗體的大量製備重要採用動物體內誘生法和體外培養法。
(1)體內誘生法 取Balb/c小鼠,首先腹腔注射0.5ml液體石蠟或降植烷進行預處理。1-2周后,腹腔內接種雜交瘤細胞。雜交瘤細胞在小鼠腹腔內增殖,並產生和分泌單克隆抗體。約1-2周,可見小鼠腹部膨大。用注射器抽取腹水,即可獲得大量單克隆抗體。
(2)體外培養法 將雜交瘤細胞置於培養瓶中進行培養。在培養過程中,雜交瘤細胞產生並分泌單克隆抗體,收集培養上清液,離心去除細胞及其碎片,即可獲得所需要的單克隆抗體。但這種方法產生的抗體量有限。各種新型培養技術和裝置不斷出現,大大提高了抗體的生產量。
抗原準備
抗原,是指能夠刺激機體產生(特異性)免疫應答,並能與免疫應答產物抗體和致敏淋巴細胞在體外結合,發生免疫效應(特異性反應)的物質。抗原的基本特性有兩種,一是誘導免疫應答的能力,也就是免疫原性,二是與免疫應答的產物發生反應,也就是抗原性。
很多物質都可以成為抗原,抗原的具體分類可以參見抗原,在進行單克隆抗體製備過程中,很多物質都可以成為抗原,在常規的科研實驗中,科研者經常選用每隻小鼠/大鼠每次注射10~50ug重組蛋白、偶聯多肽、偶聯小分子等作為抗原產生特異性的單克隆抗體。
動物免疫
單克隆抗體製備的宿主動物一般選用Balb/c小鼠,鼠單抗的套用範圍相當廣泛,一些國內外公司均開發出了兔的單克隆抗體製備技術。
免疫原分為可溶性抗原和顆粒性(細胞)抗原,用無菌鹽水稀釋並與佐劑混合,腹腔注射抗原與佐劑徹底混勻後形成的穩定乳狀液,在免疫原提供持續的免疫應答基礎上進行加強免疫
周期第1天 採血0.2ml(獲得0.1ml免疫前血清)
第一次免疫(抗原加弗氏完全佐劑)
第14天 第二次免疫(抗原加弗氏不完全佐劑)
第21天 採血和ELISA檢測
第35天 第三次免疫(抗原加弗氏不完全佐劑)
第42天 採血和ELISA檢測
第56天 第四次免疫(抗原溶於PBS或鹽水)
第61天 細胞融合
細胞融合
(一)融合劑
細胞融合的方法有物理法,如電融合、雷射融合,化學融合法和生物融合法,如滅活的仙台病毒,此處例舉化學融合法中的一種即聚乙二醇融合法。聚乙二醇(PEG),在分子量為200~700時,呈無色、無臭的粘稠狀液體,分子量大於1000時,呈乳白色蠟狀固體,能溶於水、乙醇及其他許多有機溶劑,對熱穩定,與許多化學藥品不起作用。用作細胞融合劑的聚乙二醇一般選用分子量為4000者,常用濃度為50%,pH8.0~pH8.2(用10%NaHCO3調整),分子量小的PEG,融合效應差,又有毒性,分子量過大,則粘性太大,不易操作。50%濃度,pH偏鹼時融合效應最高。也有採用30%~50%濃度的PEG加上10%二甲亞碸。不同批號的PEG,即使分子量相同,但融合率卻有明顯差異,選用時必須注意。每批都必須進行細胞毒性試驗後方可套用。要買高純度的,一般選供氣相色譜用的PEG。
(二)融合過程
融合的方法很多,常用的有轉動法和離心法。融合時脾細胞和骨髓瘤細胞的比例為1:1至10:1不等。3:1或5:1最為常用。
1.試劑與材料
(1)供融合用的脾細胞及骨髓瘤細胞。
(2)1640培養液100ml。
(3)完全1640液100ml。
(4)2.5%FCS-1640液50ml。
(5)HAT培養液100ml。
(6)50%PEG:取分子量4000,高純度的(日本進口或Serva)PEG10g放入25ml瓶中高壓滅菌,使用前用預熱於40℃的1640液10ml等量(W/V)混合,以酚紅檢查pH,一般不必調pH。如pH有改變,可用HCl或NaHCO3調整。
(7)10ml和50ml的滅菌沉澱管或瓶。
(8)40孔塑膠培養盤。
2.操作方法
⑴準備好脾細胞。
⑵在50ml沉澱管中混合108脾細胞和107小鼠骨髓瘤細胞,並加入50ml2.5%FCS-1640液。
⑶室溫400g離心3min,使細胞沉澱。
⑷移去上清液。
⑸輕敲管底部,使沉澱流動,把沉澱管放於40℃水浴中,使其達融合溫度。
⑹加預熱至40℃的50%PEG0.8ml,用1ml吸管緩慢滴加,邊加邊搖沉澱管,肉眼觀察可見有顆粒出現,滴加過程要求持續2min。
⑺加1ml1640液,邊加邊搖動,持續1min。
⑻重複⑺一次。
⑼加1ml1640液,邊加邊搖動,持續0.5min。
⑽重複⑼一次。
⑾加1640液15ml。
⑿室溫,400g離心1min,使細胞沉澱。
⒀去上清,輕敲管底部,加25ml含有HAT的完全1640液。
⒁往已於前一日種有飼養細胞的40孔塑膠培養盤中滴加融合的細胞液,每孔1滴(約0.05ml)。
⒂輕搖後,放入5%CO2飽和濕度的37℃溫箱中培育。
⒃第3、6、9、10日換入含HAT的完全1640培養液。注意輕輕吸取上清液,勿將固定於孔底的細胞吸出,根據需要加入適量的飼養細胞。
⒄於第12、15日加入含有HAT的完全1640培養液。在每次換液前用倒置顯微鏡觀察,大約在10天左右就可觀察到雜交瘤細胞生長出來。大多數雜交瘤細胞在10~20天內出現,但也有在1個月左右才能出現的。雜交瘤細胞出現後,吸取上清液,檢查抗體。
⒅對繼續生長的雜交瘤細胞進行增殖傳代。在傳代過程中,依情況取消HAT液和完全1640液而代之以10%FCS-1640液。同時保存於液氮和進行克隆化,在這期間每代都要檢查抗體,以防止產生抗體細胞的變異和丟失。
(三)細胞融合的關鍵
1.技術上的誤差常常導致融合的失敗。例如,供者淋巴細胞沒有查到免疫應答。這必然要失敗的。
2.融合試驗最大的失敗原因是污染,融合成功的關鍵是提供一個無毒無菌的操作環境。
提純實驗
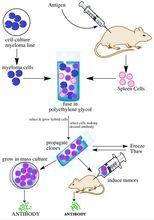 單克隆抗體製備流程
單克隆抗體製備流程1.材料
(1)20mMol/LpH7.8~7.9Tris—HCl緩衝液
20mMol/LNaCl
(2)20mMol/LpH7.8~7.9Tris—HCl緩衝液
40mMol/LNaCl
(3)20mMol/LpH7.8~7.9Tris—HCl緩衝液
80mMol/LNaCl
(4)20mMol/LpH7.8~7.9Tris—HCl緩衝液
(5)飽和硫酸銨液
(6)DEAE—纖維素柱
2.操作方法
(1)小鼠腹水用冷PBS液稀釋4倍後,於1.00×105轉離心30min,去沉澱。
(2)在4℃於上清中緩緩滴加飽和硫酸銨液,邊加邊攪拌,使溶液最終為50%硫酸銨濃度。
(3)此溶液置冰中30min~60min,然後5000r/min離心10min,去上清。
(4)將沉澱溶於Tris-HCl緩衝液(40mMol/LNaCl)中(溶液可能混濁)。
(5)裝入透析袋於Tris-HCl緩衝液(20mMol/LNaCl)中透析除鹽。
 單克隆抗體製備流程
單克隆抗體製備流程(6)離心去沉澱。
(7)溶液稀釋(1:100或更高倍稀釋)後,於280nm測蛋白含量,估計蛋白質含量1A280unit=0.8mg蛋白質一般每ml腹水中,含有總蛋白約25mg~36mg。
(8)過DEAE—纖維素柱:纖維素柱高40cm,以20mMol/LNaClTris緩衝液平衡。透析樣品以Tris緩衝液等量稀釋。
樣品進入柱床速度為1ml~2ml/min,以NaCl線形梯度洗脫。大部分單克隆IgG於40mMol/L和80mMol/LNaCl洗脫,也有極少例外的單克隆抗體於120mMol/L~150mMol/LNaCl洗脫。測OD280nm收集蛋白峰,單克隆IgG保存備用。
雜交瘤產生各種免疫球蛋白,但主要是IgG和IgM,究竟是哪種為主,則決定於抗原的免疫程式。免疫一次,且3天后就取脾,多為產生IgM的B淋巴細胞。免疫多次的多為IgG。
鑑定實驗
 單克隆抗體製備
單克隆抗體製備1.雜交瘤細胞染色體的檢查採用秋水仙素裂解法進行。
2.單克隆抗體的類型、亞型的測定:購買兔抗小鼠Ig類型和亞型的標準抗血清,採用瓊脂擴散法或ELISA夾心法測定單抗的Ig類型和亞型。
ELISA夾心法測定單抗的Ig類型和亞型的試劑盒說明書
一、試劑原理:本試劑盒利用雙抗體夾心法鑑定小鼠淋巴細胞雜交瘤培養上清中單克隆抗體或特異親和純化的單克隆抗體的類和亞類(可區分出IgG1\IgG2a\IgG2b\IgG3\IgM\IgA)。採用小鼠抗體共有位點的二抗包被微孔板,與加入的培養上清中的小鼠抗體結合,再加入HRP標記的抗小鼠各類、亞類的抗體來分別反應,最後用TMB底物系統顯色並用稀硫酸終止,再通過酶標儀檢測吸光度來判斷被測單克隆抗體的類或亞類。本試劑盒具有極高的解析度,是您鑑定小鼠單克隆抗體類、亞類的可靠工具。
三、使用範圍:用於小鼠單克隆抗體Ig類、亞類的鑑定以及相關內容的研究。
四、使用方法:
1、首先將試劑盒恢復室溫(大約30分),然後用純水把清洗液配成工作濃度(一份濃縮清洗液加19份純水)。
2、取出酶標板。每個標本需要6孔,陽性對照6孔。多餘的用自封袋保存,記得放入乾燥劑。
3、將細胞培養上清(或特異親和純化的抗體)50μl加入酶標微孔板,每個標本加6孔,陽性對照也是加6孔每孔50μl。然後每孔再加入50μl標本稀釋液。貼上封板膜37℃溫育30分鐘。
4、棄去板內液體,洗板5遍後在不掉纖維的吸水材料上拍乾或機洗5遍。再在每個標本的6孔中分別加入6種酶標二抗各100μl,通用陽性對照的6孔也一樣。在加樣圖上或酶標板上做好標記。貼上封板膜37℃溫育30分鐘。
5、吸棄板內液體,洗板5遍後在不掉纖維的吸水材料上拍乾或機洗5遍。每孔分別加入顯色劑A和顯色劑B各50μl,換一張新的封板膜貼板避光37℃顯色20分鐘。
6、本試劑盒特異性好一般肉眼即可觀察出結果,看顯色藍的那個孔所對應的酶標二抗就知道此標本的Ig類或亞類。更可將反應終止液(每孔50μl)終止反應後用酶標儀450nm測定波長,630nm參考波長雙波長測定結果,參看高值孔所對應的酶標二抗就知道此標本的Ig類或亞類。陽性對照0D小於0.5實驗無效,需要重做。
五、產品特點:高靈敏度、高特異性、結果容易判定。當然您如果覺得很多試劑自己可以準備想省一筆費用,那您可以登入網站選擇我們為您準備的簡裝抗體鑑定產品C030215。當然您也可以下次把標本交給我們來做並且不會增加太多費用!!
六、保存條件:2-8℃避光保存效期一年。不正確存放或過於頻繁開啟使用有可能因此使效期縮短。
七、注意事項:
1、雖然本試劑盒過期後很久還有使用價值但還是請您在有效期內使用。
2、在檢測腹水類單抗時要稀釋到1/5萬,雖然可以分辨但並不建議您這樣做。此類樣品成分十分複雜,有干擾結果的可能。在此種情況下您可以選擇本公司的C030215抗體鑑定試劑。它會給您帶來滿意的結果。
3、手洗板子時一定要把孔加滿,停留10秒然後棄盡,最後要拍乾淨。特別是在酶標二抗溫育後洗板時一定要把酶吸出而不是甩出,要吸淨。這個在手工洗板時對結果很重要。
4、一次沒用完的板子要帶乾燥劑放自封袋封好,隨盒存放。
5、拿放板子時不要劇烈抖動,以免孔間交叉污染出現錯誤結果。
6、出現異常結果請隨時諮詢我們。
3.單抗的特異性鑑定可以採用各種方法,如免疫螢光法、ELISA法、間接血凝和免疫印跡技術等,同時還需做免疫阻斷試驗等。
4.單抗的效價測定可採用凝集反應、ELISA或放射免疫測定。不同的測定方法效價不同。培養上清液的效價遠不如腹水的效價。採用凝集反應,腹水效價可達5×104。而採用ELISA檢查,腹水效價可達1.0×106。單抗的效價以培養上清和腹水的稀釋度表示。
5.必要時還可以測定單抗的親和力和識別抗原表位的能力測定。
細胞選擇
(一)脾細胞
1.材料
 單克隆抗體製備流程
單克隆抗體製備流程(1)免疫過的血清抗體滴度高的Balb/c鼠。
(2)1640培養液
(3)2.5%FCS-1640營養液
2.操作方法
(1)拉頸或用CO2處死小白鼠。
(2)將小鼠放於70%酒精中浸泡消毒,取出固定於板上,在無菌條件下取脾。
(3)把脾放入5ml含有2.5%FCS的1640液中,冰浴下輕輕洗去脾上的紅血球。
(4)用鑷子輕輕擠壓脾,做成脾細胞懸液,用毛細管將懸液移入小試管中。
(5)直立小試管3min,使大塊的結締組織下沉,把細胞懸液移入離心管中。
(6)以2.5%FCS—1640充滿離心管,並以400g離心7min~10min(與此同時應開始製備骨髓細胞)。
(7)把沉澱用約10ml的新鮮培養液再懸浮。
(8)重複⑹、⑺步驟。
(9)計算細胞,以台盼蘭染色用相差顯微鏡檢查,活細胞數應高於80%為合格。
(二)骨髓瘤細胞
骨髓瘤細胞能產生並分泌大量的免疫球蛋白,這樣的瘤細胞融合後,可能影響或降低所分泌抗體的滴度,所以必須選育出非分泌免疫球蛋白缺陷型的骨髓瘤細胞。
選擇骨髓瘤細胞的條件:①該瘤細胞系的來源應與製備脾細胞小鼠為同一品系,以便兩者的組織相容性抗原一致;②骨髓瘤細胞必須是靜息狀態,不產生γ球蛋白或不分泌到細胞外;③骨髓瘤細胞生長需要一個較高的細胞密度,最好106個細胞/ml;④生長速度快,繁殖時間短。常用的Balb/c小鼠產生的骨髓瘤細胞株有:①S194/5XXO·BU·1;②SP2/0—Ag14(簡稱SP2);③P2—X;—Ag8·6·5·3(簡稱653);④FO以653最為常用,它是由礦物油4-甲基-15烷(Pristane,降植烷)誘發出來的一種漿細胞瘤(MinerolOilplasmacytoma,MOPC)並經過培育形成一株8-氮鳥嘌呤有抵抗力的亞系。骨髓瘤細胞一般由有關單位直接引入,保存於-195℃液氮罐中,試驗時復甦、增殖、傳代即可。由於骨髓瘤細胞是半貼壁狀態,很容易脫落,因此不需要胰酶處理。為了防止出現返祖現象,在融合前,可將培養基內加入15μg/ml8-氮鳥嘌呤。取約1×107~6×107對數生長期(即培養15h~20h)的骨髓瘤細胞,在室溫離心(400g)10min,沉澱以2.5%FCS—1640液再懸浮並計數。
(三)飼養細胞
在體外的細胞培養中,單個的或數量很少的細胞不易生存與繁殖,必須加入其它活的細胞才能使其生長繁殖,加入的細胞稱之為飼養細胞(Feedercell)。在細胞融合和單克隆的選擇過程中,就是在少量的或單個細胞的基礎上使其生長繁殖成群體,因此在這一過程中必須使用飼養細胞。許多種類的動物細胞都可以做飼養細胞,如正常的脾細胞、胸腺細胞、腹腔滲出細胞等,常選用腹腔滲出細胞,其中主要是巨噬細胞和淋巴細胞。套用腹腔滲出細胞的好處是:一方面做飼養細胞,另一方面巨噬細胞可以吞噬死亡的細胞和細胞碎片,為融合細胞的生長造成良好的環境。腹腔細胞的來源可以是與骨髓瘤細胞同系鼠。也可以是其他種類的小鼠,如C57鼠,昆明小白鼠等。
1.材料
(1)小鼠(Balb/c或C57小白鼠)若干只。
(2)11.6%蔗糖溶液(經10磅30min高壓滅菌)。
2.操作方法
(1)拉頸處死小鼠。
(2)70%酒精浸泡消毒10min。
(3)用手術剪將小鼠腹部剪開一小口,剝開皮膚,露出腹腔。
(4)用注射器將4ml11.6%蔗糖溶液注入腹腔,用手指輕揉1min仍用該注射器回抽腹腔液體,加入離心管。
(5)1000r/min離心10min。
(6)取上清,以HAT選擇培養液將細胞製成懸液。台盼藍染色計數活細胞,使每毫升含40萬個活細胞。
(7)以1ml吸管將細胞種入微量培養皿,每孔0.05ml,含2萬個細胞,放入CO2培養箱培養,即可供細胞融合和克隆化之用.
套用領域
單克隆抗體問世以來,由於其獨有的特徵已迅速套用於醫學很多領域。主要表現在以下幾個方面。
1.檢驗醫學診斷試劑
作為檢驗醫學實驗室的診斷試劑,單克隆抗體以其特異性強、純度高、均一性好等優點,廣泛套用於酶聯免疫吸附試驗、放射免疫分析、免疫組化和流式細胞儀等技術。並且單克隆抗體的套用,很大程度上促進了商品化試劑盒的發展。套用單克隆抗體製作的商品化試劑盒廣泛套用於:
①病原微生物抗原、抗體的檢測;
②腫瘤抗原的檢測;
 單克隆抗體細胞
單克隆抗體細胞③免疫細胞及其亞群的的檢測;
④激素測定;
⑤細胞因子的測定。
單克隆抗體對抗原的識別,與多克隆抗體有很大的不同。不同試劑盒因使用的單克隆抗體不同,識別抗原的位點不同,導致檢測結果有一定差異。因此,標準化問題還需要進一步研究。
2.蛋白質的提純
單克隆抗體是親和層析中重要的配體。將單克隆抗體吸附在一個惰性的固相基質(如Speharose 2B、4B、6B等)上,並製備成層析柱。當樣品流經層析柱時,待分離的抗原可與固相的單克隆抗體發生特異性結合,其餘成分不能與之結合。將層析柱充分洗脫後,改變洗脫液的離子強度或pH,欲分離的抗原與抗體解離,收集洗脫液便可得到欲純化的抗原。
3. 腫瘤的導向治療和放射免疫顯像技術
將針對某一腫瘤抗原的單克隆抗體與化療藥物或放療物質連線,利用單克隆抗體的導向作用,將藥物或放療物質攜帶至靶器官,直接殺傷靶細胞,稱為腫瘤導向治療。另外,將放射性標記物與單克隆抗體連線,注入患者體內可進行放射免疫顯像,協助腫瘤的診斷。單克隆抗體主要為鼠源性抗體,異種動物血清可引起人體過敏反應。因此,製備人-人單克隆抗體或人源化抗體更為重要,但此方面仍未取得明顯進展。
優點局限
1.單克隆抗體的優點
(1)雜交瘤可以在體外“永久”地存活並傳代,只要不發生細胞株的基因突變,就可以不斷地生產高特異性、高均一性的抗體。
(2)可以用相對不純的抗原,獲得大量高度特異的、均一的抗體。
(3)由於可能得到“無限量”的均一性抗體,所以適用於以標記抗體為特點的免疫學分析方法,如IRMA和ELISA等。
(4)由於單克隆抗體的高特異性和單一生物學功能,可用於體內的放射免疫顯像和免疫導向治療。
2.單克隆抗體的局限性
(1)單克隆抗體固有的親和性和局限的生物活性限制了它的套用範圍。由於單克隆抗體不能進行沉澱和凝集反應,所以很多檢測方法不能用單克隆抗體完成。
(2)單克隆抗體的反應強度不如多克隆抗體。
(3)製備技術複雜,而且費時費工,所以單克隆抗體的價格也較高。
研究進展
單克隆抗體藥物的發展起源於1975年,雜交瘤技術的問世使大量製備均一的鼠源單克隆抗體成為可能。1986年第一個抗移植後免疫排斥反應的鼠源單克隆抗體muromonab-CD3(OKT3)經美國食品藥品監督管理局(Food andDrug Administration, FDA)批准上市,但是來源於鼠源淋巴細胞雜交瘤的抗體被人的免疫系統識別,會引起嚴重的人抗鼠抗體反應(human anti-mouse antibody,HAMA),不僅使治療性單抗半衰期變短,療效減弱,有時還會引起嚴重的不良反應。
單克隆抗體藥物的發展在1988年到1993年間陷入低谷。隨著重組DNA技術的發展,各種抗體人緣化技術迅速發展,單克隆抗體藥物經歷了人鼠嵌合單抗、人源化單抗階段。隨後出現的噬菌體展示文庫技術和轉基因小鼠技術,使全人源單抗的產生成為可能,2002年第一個全人源抗體阿達木單抗上市。
如今單克隆抗體藥物已經成為生物醫藥的重要組成部分,在醫藥治療上也具有廣闊的套用前景,已經被成功用於治療腫瘤、自身免疫性疾病、感染性疾病和移植排斥反應等多種疾病。阿達木單抗、英夫利西單抗、托珠單抗等均屬於醫用單克隆抗體藥物。如用於緩解抗風濕性藥物(DMARD)治療無效的結構性損傷的中至重度類風濕關節炎(RA)成年患者的體徵與症狀的修美樂-阿達木單抗注射液,可單獨使用,也可與甲氨蝶呤或其他DMA用於緩解抗風濕性藥物(DMARD)治療無效的結構性損傷的中至重度類風濕關節炎(RA)成年患者的體徵與症狀。
全人源單克隆抗體
單克隆抗體的發展經歷了四個階段,分別為:鼠源性單克隆抗體、嵌合性單克隆抗體、人源化單克隆抗體和全人源單克隆抗體。全人源單克隆抗體:其抗體的可變區和恆定區都是人源的,去除免疫原性和毒副作用。全人源抗體製備的相關技術主要有:人雜交瘤技術、EBV 轉化 B 淋巴細胞技術、噬菌體顯示技術(phage display)、轉基因小鼠抗體製備技術(transgenic mouse)和單個B細胞抗體製備技術等。
由人源化和全人源抗體製備的人源化和全人源抗體藥物因其具有高親和力、高特異性、毒副作用小的特點,克服了動物源抗體及嵌合抗體的各種缺點,已經成為了治療性抗體藥物發展的必然趨勢。
當今最被業界看好的是阿達木單抗,原因在於,其作為生物單抗藥物,在療效和技術門檻方面難以挑戰;另外,越來越多的醫生在治療類風濕時首選皮下注射給藥的劑型,不需要注射過程和費用,這一點阿達木單抗將具有巨大優勢。雖然與依那西普的對比臨床試驗還未出來,但是人們普遍認為阿達木單抗的療效更好。國外機構預測,未來3年類風濕關節炎用藥阿達木單抗將成為老大,到2016年達到銷售最高峰,超過百億美元。
發展情況
銷售及增長
2010年全球治療用單抗藥物的銷售總額達到440億美元,如果加上100億美元的單抗診斷和研究試劑,單抗藥物的市場總量達到550億美元。2011年單抗藥物的市場總量已經達到628億美元。未來,全球單克隆抗體藥依舊會保持較高的增長率。到2015年,全球單克隆抗體藥銷售額有望達980億美元左右。我國的單克隆抗體藥物從無到有,並且在我國醫藥市場發揮越來越重要的作用。目前我國單抗市場規模每年以50%以上的速度遞增。單克隆抗體在我國市場仍屬高端產品,主要依賴進口。羅氏是我國單抗市場最大的贏家,市場份額最高的品種利妥昔單抗和曲妥珠單抗均來自羅氏製藥,羅氏所有產品份額超過國內單抗產品份額半數。2010年我國腫瘤藥物市場銷售額達160億元,同比增長24%,全球排名第七,遠超美國4.4%和其他成熟或新興市場;2011年市場銷售額達到208億元。同比增長率30%。對生物仿製藥的市場滲透率形成制約的其中一個因素是立法,它阻止了用生物仿製藥來替代原研產品。這意味著,生物仿製藥的使用只限於新病人和短期適應症。然而,使用生物仿製藥創造的醫療成本控制機會卻是巨大的。在那些尚未為生物仿製藥確定監管路徑的市場上(其中包括美國),生物仿製藥獲得成功的關鍵因素是專利的獨有性、臨床試驗要求和互換性。
研發的政策支持
"十二五"期間,我國"重大新藥創製"專項將獲中央財政下撥資金100億元,配套資金300億元。專項戰略重點包括創新藥物研究開發、藥物大品種技術改造等。惡性腫瘤、心腦血管疾病、神經退行性疾病、糖尿病、肺結核等10類重大疾病藥物的研發是創製資金支持重點。"十二五"期間,醫藥工業發展目標為總產值年均增長20%,到2015年達到3.1萬億元。2011年,單克隆抗體藥物繼續領跑全球藥品市場,同比有較大的增長。2000-2010年10年間,全球單克隆抗體藥物市場的複合增長率高達32%。2011年,全球處方藥前20位中,有6個為單克隆抗體藥物,其中有5個銷售額超過50億美元。而在此前的2009年和2008年,該數字分別為400億美元和370億美元。當前,幾乎所有大型製藥公司都有單抗研發項目。在2011年全球最暢銷的20種藥品中,美國輝瑞公司用於降低膽固醇的阿托伐他汀鈣居於首位,達到133億美元。2011年,全球生物製藥產品的市場規模超過1550億美元,占製藥/生物製藥產品的25%。不過,有研究數據表明,生物製藥產品今後幾年在全球市場上的占比將明顯上升。據預測,到2014年,全球銷售額前三大產品都將是生物技術藥物(Avastin,Humira和Enbrel),屆時它們的銷售額合計將達到254億美元。單克隆抗體藥物已經成為生物製藥中最為重要的一類:2011年銷售規模最大的7種抗體藥物的銷售額達到了388.2億美元,占整個生物製藥市場份額接近50%;單克隆抗體仍是研發的熱點,也將是未來生物製藥行業發展的重要動力所在。
免疫系統
| 系統 | 自適應與天然 | 體液與細胞 | 補體(過敏毒素) | 固有 |
| 抗原與抗體 | 抗原 (超抗原;變應原) | 半抗原 |
| 表位 (線性;構象) | |
| 抗體 (單克隆抗體; 多克隆抗體;自身抗體) | 多克隆B細胞反應 | 同種異型 | 同種型 | 遺傳型 | |
| 免疫複合物 | |
| 免疫細胞/白細胞 | 淋巴系細胞: T細胞 | B細胞 | NK細胞 |
| 髓系細胞:肥大細胞 | 嗜鹼性粒細胞 | 嗜酸性粒細胞 | 巨噬細胞 | |
| 吞噬細胞:中性粒細胞 | 巨噬細胞/網狀內皮系統 | |
| 專職型 APCs:樹突狀細胞 | 巨噬細胞 | B細胞 | |
| 免疫與耐受 | 作用:免疫性 | 自身免疫 | 變態反應 | 炎症 | 交叉反應性 |
| 無作用:耐受 (中樞耐受;外周耐受;克隆無能;克隆缺失) | 免疫缺損 | |
| 免疫遺傳學 | 體細胞超突變 | V(D)J 重組 | 免疫球蛋白類別轉換 | MHC/HLA |
| 免疫物質 | 細胞因子 | 調理素 | 溶細胞素 |
| 其他 | 診斷免疫學 |
免疫系統/ 免疫學
| 免疫系統 | 它是人體抵禦病原菌侵犯最重要的保衛系統。 |
| 系統 | |
| 抗原與抗體 | 抗原 (超抗原, 變應原) | 半抗原 表位 (線性表位, 構象表位) 抗體 (單克隆抗體, 多克隆抗體, 自身抗體) | 多克隆B細胞反應 | 同種異型 | 免疫球蛋白同種異型 | 遺傳型 | 免疫複合物 |
| 免疫細胞/白細胞 | 淋巴系細胞:T細胞 | B細胞 | NK細胞 髓系細胞:肥大細胞 | 嗜鹼性粒細胞 | 嗜酸性粒細胞 | 巨噬細胞 吞噬細胞:中性粒細胞 | 巨噬細胞 | 網狀內皮系統 抗原遞呈細胞:樹突狀細胞 | 巨噬細胞 | B細胞 |
| 免疫 與 耐受 | 作用:免疫性 | 自身免疫 | 變態反應 | 炎症 | 交叉反應性 無作用:耐受 (中樞耐受, 外周耐受, 克隆無能, 克隆缺失) | 免疫缺損 |
| 免疫遺傳學 | 體細胞超突變 | V(D)J 重組 | 免疫球蛋白類別轉換 | MHC/HLA |
| 免疫物質 | 細胞因子 | 調理素 | 溶細胞素 |
| 其他 | 診斷免疫學 |