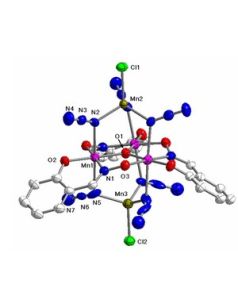
概述
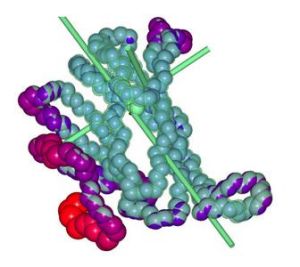 離子化合物
離子化合物代表物:
鹼性氧化物(Fe2O3)
鹽(NaCl)
鹼[NaOH]
存在形式
離子化合物(ioniccompound)是存在於:1、活潑金屬(指第一和第二主族的金屬元素)與活潑的非金屬元素(指第六和第七主族的元素)之間形成的化合物
2、金屬元素與酸根離子之間形成的化合物。(酸根離子如硫酸根離子SO42-、硝酸根離子NO3-、碳酸根離子CO32-等等);
3、銨根離子(NH4+)和酸根離子之間,或銨根離子與非金屬元素之間,例如NH4Cl、NH4NO3。
離子化合物都是強電解質。在熔融狀態下:都可以導電(此類物質加熱時易分解或易氧化)。在水中:有的可以導電,有的不可以導電(此類物質易與水反應或不溶於水)。在原電池中的作用:形成閉合電路。
相關關係
離子化合物和共價化合物都涉及到電子的移動。離子化合物是通過離子鍵形成的化合物,離子鍵是由電子轉移(失去電子者為陽離子,獲得電子者為陰離子)形成的。即正離子和負離子之間由於靜電作用所形成的化學鍵。
而共價化合物是通過共用電子構成的共價鍵結合而成的化合物,共價鍵是化學鍵的一種,兩個或多個原子共同使用它們的外層電子,在理想情況下達到電子飽和的狀態,由此組成比較穩定和堅固的化學結構叫做共價鍵。與離子鍵不同的是進入共價鍵的原子向外不顯示電性,因為它們並沒有獲得或損失電子。共價鍵的強度比氫鍵要強,與離子鍵差不太多或甚至比離子鍵強。
區分
(1)根據化合物組成元素的性質來判斷(2)根據構成化合物的離子鍵是以離子鍵還是以共價鍵結合來判斷
(3)根據化合物的類型來判斷
(4)根據化合物的導電性來判斷
(5)根據化合物的熔沸點來判斷
離子化合物由陽離子和陰離子組成的化合物。活潑金屬(如鉀、鈣、鈉、鎂等)與活潑非金屬(如氟、氯、氧、硫等)相互化合時,活潑金屬失去電子形成帶正電荷的陽離子(如Na+、K+、Ca2+、Mg2+等),活潑非金屬得到電子形成帶負電荷的陰離子(如F-、Cl-、O2-、S2-等),陽離子和陰離子靠靜電作用形成了離子化合物。例如,氯化鈉即是由帶正電的鈉離子(Na+)和帶負電的氯離子(Cl-)構成的離子化合物。許多鹼(如NaOH、KOH、Ba(OH)2等)和鹽(如CaCl2、KNO3、CuSO4等)都是離子化合物。在離子化合物里陽離子所帶的正電荷總數等於陰離子所帶的負電荷總數,整個化合物呈電中性。多數離子化合物在固態(或晶態)時不能導電,而它的水溶液或熔化狀態則能導電。離子化合物一般說來,熔點和沸點較高,硬度較大,質脆,難於壓縮,難揮發。
某些鹼性氧化物,如Na2O、K2O,常見的鹽類如NaCl、KF,常見的鹼,如NaOH等都屬於離子化合物。
離子化合物是存在於1、活潑金屬(指第一和第二主族的金屬元素)與活潑的非金屬元素(指第六和第七主族的元素)之間形成的化合物。2、金屬元素與酸根離子之間形成的化合物。(酸根離子如硫酸根離子、硝酸根離子、碳酸根離子等等)3、銨根離子(NH4+)和酸根離子之間,或銨根離子與非金屬元素之間。
共價化合物存在於非金屬元素之間,對於由兩種元素形成的化合物。如果存在於同種非金屬元素之間那么是非極性共價鍵,如是不同種元素之間形成的是極性共價鍵,他們都是共價化合物。
離子化合物都是電解質,且在水溶液或熔融狀態下可以導電。在原電池中的作用:形成閉合電路!
離子化合物中一定含有至少一個離子鍵,並且可能同時含有共價鍵。
形式
具體來說,強鹼、鹽、金屬氧化物和銨鹽都是離子化合物,但不僅僅這些,詳見離子化合物的存在形式。電子式:..
..Cl..-Na+(NaCl)
離子聚合物
聚丙烯醯胺為水溶性高分子聚合物,不溶於大多數有機溶劑,具有良好的絮凝性,可以降低液體之間的磨擦阻力,按離子特性分可分為非離子、陰離子、陽離子和兩性型四種類型。注意事項
陽離子聚丙烯醯胺使用注意事項:1、絮團的大小:絮團太小會影響排水的速度,絮團太大會使絮團約束較多水而降低泥餅乾度。經過選擇聚丙烯醯胺的分子量能夠調整絮團的大小。
2、污泥特性。第一點理解污泥的來源,特性以及成分,所占比重。依據性質的不同,污泥可分為有機和無機污泥兩種。陽離子聚丙烯醯胺用於處置有機污泥,相對的陰離子聚丙烯醯胺絮凝劑用於無機污泥,鹼性很強時用陽離子聚丙烯醯胺,而酸性很強時不宜用陰離子聚丙烯醯胺,固含量高時污泥通常聚丙烯醯胺的用量也大。
3、絮團強度:絮團在剪下作用下應堅持穩定而不破碎。進步聚丙烯醯胺分子量或者選擇適宜的分子構造有助於進步絮團穩定性。
4、聚丙烯醯胺的離子度:針對脫水的污泥,可用不同離子度的絮凝劑經過先做小試停止挑選,選出最佳適宜的聚丙烯醯胺,這樣即能夠獲得最佳絮凝劑效果,又可使加藥量最少,節約本錢。 5、聚丙烯醯胺的溶解:溶解良好才幹發充沛發揮絮凝作用。有時需求加快溶解速度,這時可思索進步聚丙烯醯胺溶液的濃度。
使用特性
1、絮凝性:PAM能使懸浮物質通過電中和,架橋吸附作用,起絮凝作用。2、粘合性:能通過機械的、物理的、化學的作用,起粘合作用。
3、降阻性:PAM能有效地降低流體的摩擦阻力,水中加入微量PAM就能降阻50—80%。
4、增稠性:PAM在中性和酸條件下均有增稠作用,當PH值在10以上PAM易水解。呈半網狀結構時,增稠將更明顯。
作用原理
1)絮凝作用原理:PAM用於絮凝時,與被絮凝物種類表面性質,特別是動電位,粘度、濁度及懸浮液的PH值有關,顆粒表面的動電位,是顆粒阻聚的原因加入表面電荷相反的PAM,能使動電位降低而凝聚。2)吸附架橋:PAM分子鏈固定在不同的顆粒表面上,各顆粒之間形成聚合物的橋,使顆粒形成聚集體而沉降。
3)表面吸附:PAM分子上的極性基團顆粒的各種吸附。
4)增強作用:PAM分子鏈與分散相通過種種機械、物理、化學等作用,將分散相牽連在一起,形成網狀
用途
水處理領域。PAM在水處理工業中的套用主要包括原水處理、污水處理和工業水處理3個方面。在原水處理中,PAM與活性炭等配合使用,可用於生活水中懸浮顆粒的凝聚和澄清;在污水處理中。PAM可用於污泥脫水;在工業水處理中,PAM主要用作配方藥劑。在原水處理中,用有機絮凝劑PAM代替無機絮凝劑,即使不改造沉降池,淨水能力也可提高20%以上。所以21世紀許多大中城市在供水緊張或水質較差時,都採用PAM作為補充。工業廢水處理,特別是對於懸浮顆粒、較粗、濃度高、粒子帶陽電荷,水的PH值為中性或鹼性的污水、鋼鐵廠廢水,電鍍廠廢水,冶金廢水,洗煤廢水等污水處理,效果最好。在污水處理中,採用PAM可以增加水回用循環的使用率。石油採油領域。在石油開採中,PAM主要用於鑽井泥漿材料以及提高採油率等方面,廣泛套用於鑽井、完井、固井、壓裂、強化採油等油田開採作業中,具有增粘、降濾失、流變調節、膠凝、分流、剖面調整等功能。目前我國油田開採已經步入中後期,為提高原油採收率,21世紀主要推廣聚合物驅油和三元複合驅油技術。通過注入PAM水溶液,改善油水流速比,使采出物中原油含量提高。21世紀國外PAM在油田方面的套用不多,我國由於特殊的地質條件,大慶油田和勝利油田已經開始廣泛採用聚合物驅油技術。
造紙領域。PAM在造紙領域中廣泛用作駐留劑、助濾劑、均度劑等。它的作用是能夠提高紙張的質量,提高漿料脫水性能,提高細小纖維及填料的留著率,減少原材料的消耗以及對環境的污染等。PAM在造紙中使用的效果取決於其平均分子量、離子性質、離子強度及其它共聚物的活性。非離子型PAM主要用於提高紙漿的濾性,增加乾紙強度,提高纖維及填料的留著率;陰離子型共聚物主要用作紙張的乾濕增強劑和駐留劑;陽離子型共聚物主要用於造紙廢水處理和助濾作用,另外對於提高填料的留著率也有較好的效果。此外,PAM還套用於造紙廢水處理和纖維回收。
紡織領域在紡織工業中,PAM作為織物後處理的上漿劑、整理劑,可以生成柔順、防皺、耐黴菌的保護層。利用它的吸濕性強的特點,能減少紡細紗時的斷線率;PAM作後處理劑可以防止織物的靜電和阻燃;用作印染助劑時,PAM可使產品附著牢度大、鮮艷度高,還可以作為漂白的非矽高分子穩定劑;此外,PAM還可以用於紡織印染污水的高效淨化。
其他領域在採礦、洗煤領域,採用PAM作絮凝劑可促進採礦、洗煤回收水中固體物的沉降,使水澄清,同時可回收有用的固體顆粒,避免對環境造成污染;在製糖工業中,PAM可加速蔗汁中細粒子的下沉,促進過濾和提高濾液的清澈度;在養殖工業中,PAM可改善水質,增加水的透光性能,從而改善水的光合作用;在醫藥工業中,PAM可用作分離抗菌素的絮凝劑、用作藥片的賦型粘接劑以及工藝水澄清劑等;在建材工業中,PAM可用作塗料增稠分散劑、鋸石板材冷卻劑以及陶瓷粘接劑等;在農業上,PAM作為高吸水性材料可用作土壤保濕劑以及種子培養劑等。在建築工業中,PAM可以增強石膏水泥的硬度,加速石棉水泥的脫水速度。此外,PAM還可用作天然或合成皮革的保護塗層以及無機肥料的造粒助劑等。