藥品介紹
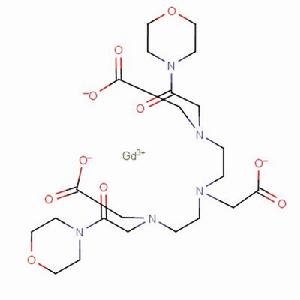 釓貝葡胺分子結構
釓貝葡胺分子結構通用名:釓貝葡胺注射液
英文名稱 Gadobenate Dimeglumine Injection
漢語拼音:Gabeipu’an Zhusheye
藥品劑型:注射劑
藥品成分:釓貝葡胺。
化學名稱:釓化(2-),[4-羧基-5,8,11-三(羧甲基)-1-苯基-2-氧雜-5,8,11-三氮雜十三烷-13-羧基(5)-N5,N8,N1,O4,O5,O8,O11,
O13]-二氫化合物化合1-脫氧-1-甲基胺-D-葡萄糖醇(1:2)。
分子式:C22H28GdN3O11·2C7H17NO5
分子量:1058.16
藥品規格:20ml:10.58g釓貝葡胺(相當於釓貝酸6.680g,葡甲胺3.900g)。
貯藏方法:遮光,15- 30℃貯存,切勿冷凍。
包裝:玻璃瓶,1瓶/盒。
有效期限:36個月
藥品性狀:本品為幾乎無色的澄明液體。
藥理毒理
 釓貝葡胺製劑
釓貝葡胺製劑本品為藥理作用釓螯合物,釓貝葡胺,可以縮短人體組織氫質子的縱向弛豫時間(T1),並在較小程度上同時縮短橫向弛豫時間(T2)。釓貝葡胺在水溶液中的弛豫率20MHz時為r1=4.4,r2=5.6mM-1s-1。釓貝葡胺在血清蛋白溶液中的弛豫率較水溶液有明顯的增大。在人類血漿中r1和r2值分別為9.7和12.5mM-1s-1。肝臟釓貝葡胺在肝臟T1加權成像中能使正常肝實質呈現顯著而持久的信號強度增強。以0.05或0.10mmol/Kg的劑量給藥後信號強度至少在2小時內可維持較高的水平。在T1加權動態成像中,釓貝葡胺團注後幾乎立即(約2-3分鐘)可以觀察到局灶性肝臟病變與正常實質之間的對比。此為非特異性病灶增強,在一定時間之後,這一對比趨於減弱。由於在給藥後40-120分鐘之間,釓貝葡胺進一步從病灶內排出而正常實質信號強度持久增強,使得病灶檢出增多,病變部位的檢出閾值降低。中樞神經系統在中樞神經系統成像中,釓貝葡胺可使缺乏血腦屏障的正常組織,軸外腫瘤和血腦屏障已被破壞的區域出現信號增強。臨床資料中樞神經系統成像在這一適應症關鍵性的III期臨床試驗中,非現場讀片者報告釓貝葡胺對診斷信息的改善程度為32—69%,陽性對照組為35—69%。肝臟成像對於已知或可疑肝癌或轉移癌患者,使用釓貝葡胺可以發現在未用造影增強的MRI檢查中不可見的病變。採用MRI對比增強所發現的病變性質還沒有通過病理解剖的檢查證實。遺傳毒性在所進行的體內、體外試驗中均未發現釓貝葡胺具有致突變效應。 致癌性由於釓貝葡胺為單次給藥,且不具有誘變潛力,故未進行致癌性研究。
藥動力學
 釓貝葡胺注射液
釓貝葡胺注射液人體藥代動力學描述呈二級指數衰變形式。靜脈注射釓貝葡胺,其分布和清除半衰期分別為0.085—0.117和1.17—1.68小時。總的分布容積從0.170— 0.248 L/kg體重,化合物分布於血漿及細胞外。釓貝酸離子快速從血漿中清除,並且主要從尿中排出,很少量的從膽汁中排出。在24小時內,注射劑量78~94%的釓貝酸離子以原形從尿中排出。總血漿清除率為0.098—0.133 L/h公斤體重,腎臟清除率從0.082—0.104 L/h公斤體重,由腎小球過濾排出。血漿濃度和曲線下面積(AUC)呈現與給藥劑量相關的線性關係,且具有統計學意義。給藥劑量的2~4%可從糞便中檢出。釓貝酸離子不能穿過完整的血腦屏障。因此,它不會在正常的腦組織中或具有正常血腦屏障的損傷腦組織中累積。然而,當血腦屏障遭到破壞或血管不正常時則允許釓貝酸離子滲入到損傷的部位中。
適應症狀
 釓貝葡胺注射液
釓貝葡胺注射液釓貝葡胺是一種適用於肝臟和中樞神經系統的診斷性磁共振成像(MRI)的順磁性對比劑。
肝臟:適用於探測已知或懷疑患有原發性肝癌(例如:肝細胞癌)或轉移性癌患者的局灶性肝損傷。
中樞神經系統:釓貝葡胺也適用於腦和脊柱的MRI增強檢查,可以增強損害的檢出,與未增強的磁共振影像相比,可以提供更多的診斷信息。為順磁性造影劑,可在特定組織產生局部磁場而增加其信號強度。給藥後迅速分布,不經體內代謝,在體內的離子解離率小於 1%。主要經腎臟隨尿液排泄。
用法用量
 釓貝葡胺注射液
釓貝葡胺注射液1、肝臟:對成年患者的推薦劑量為0.1mmol/kg,相當於0.5M的溶液0.2ml/kg。造影劑團注後可以立刻作對比成像(動態增強MRI)。在肝臟,依據個體需要,可以在注射後40~120分鐘之間進行延遲成像。
2、中樞神經系統:釓貝葡胺對成年患者的建議劑量是0.1mmol/kg,相對應為0.5M溶液0.2ml/kg。該產品應在未經稀釋的情況下以團注或緩慢注射的形式靜脈給藥,並隨之注入至少5毫升生理鹽水沖洗。為了使釓貝葡胺軟組織外滲的潛在危險降至最低,保證注射針頭或插管準確地插入靜脈中是很重要的。請勿稀釋,於使用前將本品抽吸入無菌注射器中。抽吸前,請檢查瓶、蓋有無破損。任何未用完的剩餘產品必須丟棄,而不能用於其他的MRI檢查。釓貝葡胺不能與其他藥物混合注射。
不良反應
 釓貝葡胺注射液
釓貝葡胺注射液絕大多數症狀是不嚴重的、短暫的,並且能夠無後遺症地自動消退。副反應的發生與年齡、性別和給藥劑量尚無相關性的證據。在釓貝葡胺的臨床套用中出現下列不良反應超過1%:
全身反應:頭痛。
高血壓神經系統:感覺異常,眩暈。
心血管系統:心動過速,房顫,心律不齊,一級動靜脈堵塞,室性期外收縮,竇性心動過緩,低血壓,暈厥,心肌缺血,不正常心電圖,QT或PR間隔延長。
消化系統:腹瀉,嘔吐,便秘,消化不良。
神經系統:感覺過敏,震顫,多涎。
呼吸系統:呼吸困難,鼻炎,喉炎。
亦有報告顯示,注射釓貝葡胺後低於0.4%的患者出現實驗室異常,如:低血色素性貧血,白細胞增多,白細胞減少,嗜鹼性粒細胞減少,嗜鹼性粒細胞增多,低蛋白血症,低血鈣,高血鉀,高血糖或低血糖,糖尿,蛋白尿,血尿,血脂增高;血清鐵、血清轉氨酶、鹼性磷酸酶、乳酸脫氫酶、血膽紅素及血肌酐增高。
注意事項
 釓貝葡胺製劑
釓貝葡胺製劑鐮狀細胞性貧血患者可能會因為套用該藥而誘發脈管阻塞性危象,因此,這類患者應儘可能避免使用該藥。該藥可能會導致部分患者出現房性或室性心律失常。
對釓貝葡胺及製劑中其他成分(如苯甲醇)過敏者禁用。
孕婦及哺乳期婦女用藥:不推薦在孕婦中使用釓貝葡胺,因為尚無臨床數據支持它可套用於此患者群。人乳中釓貝葡胺排泌量是未知的。但是從動物實驗中知道,少於給藥劑量0.5%的本品通過母親乳汁轉移給新生兒。雖然此發現的臨床相關性是未知的,但是在使用釓貝葡胺前應該停止哺乳,並且建議在用藥後至少24小時內不應哺乳。
兒童用藥:未在18歲以下患者群中進行釓貝葡胺的安全性和有效性試驗。因此,不建議在此患者群中使用。
老年患者用藥:由於老年患者多伴有腎功能的減退,且已知腎臟為本品的主要排泄器官,當老年患者使用釓貝葡胺時,請注意監測其腎功能情況。
相互作用
 釓貝葡胺製劑
釓貝葡胺製劑該藥與某些藥物合用時,可能會產生陰離子轉運器的競爭作用,從而導致後者的體內消除過程受到影響。這些藥物包括:順鉑、蒽環類抗生素、長春花鹼類藥物、甲氨喋呤、依託泊苷、他莫昔芬和紫杉醇等。
臨床試驗中該藥最常見的不良事件為頭痛和噁心。最罕見但嚴重的不良事件包括癲癇發作、急性肺水腫、急性胰腺炎和過敏樣反應。
