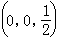點陣中間隙位置
如果把晶體中的金屬原子看成是一些簡單的相互接觸的球體,則在等徑圓球的三種簡單密排結構中存在兩種間隙位置,即四面體間隙和八面體間隙。
面心立方 (fcc)結構的間隙位置見圖1。八面體間隙(圖1) 由八面體頂角的六個原子所圍成,間隙的中心位於單位晶胞的每個棱邊的中點如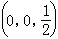 等和體心位置
等和體心位置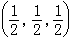 ,間隙半徑r、原子半徑rа之間有如下關係:r≈0.41rа。四面體間隙(圖1)由晶胞的一個頂角原子和相鄰的三個面心原子所組成的四面體構成,中心位於
,間隙半徑r、原子半徑rа之間有如下關係:r≈0.41rа。四面體間隙(圖1)由晶胞的一個頂角原子和相鄰的三個面心原子所組成的四面體構成,中心位於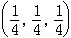 等處。四面體間隙半徑r≈0.225rа。以γ-Fe為例,八面體間隙有容納半徑為0.52┱ 的球形原子的空間。因而只要點陣適當膨脹,可以容一個碳原子(半徑0.8┱)或氮原子(半徑0.7┱)。四面體間隙半徑僅為0.28┱,很可能任何溶質原子都無法進入。
等處。四面體間隙半徑r≈0.225rа。以γ-Fe為例,八面體間隙有容納半徑為0.52┱ 的球形原子的空間。因而只要點陣適當膨脹,可以容一個碳原子(半徑0.8┱)或氮原子(半徑0.7┱)。四面體間隙半徑僅為0.28┱,很可能任何溶質原子都無法進入。
在體心立方(bcc)金屬中, 四面體間隙的中心位於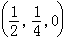 和與它相應的位置。間隙半徑r≈0.291rа。位於此中心的球形原子將與四個球形的溶劑原子相接觸(圖2b)。在α-Fe中,如球形鐵原子相互接觸,則四面體間隙能容納半徑為0.36┱ 的溶質原子。八面體間隙中心位於邊棱的中點
和與它相應的位置。間隙半徑r≈0.291rа。位於此中心的球形原子將與四個球形的溶劑原子相接觸(圖2b)。在α-Fe中,如球形鐵原子相互接觸,則四面體間隙能容納半徑為0.36┱ 的溶質原子。八面體間隙中心位於邊棱的中點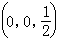 等或
等或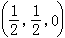 的相應點(圖2),系由稍壓扁的八面體頂角上6個原子所圍成。距上下兩原子比距其他四個原子略近。間隙半徑r=0.154rа。在 α-Fe中間隙半徑尺寸為0.19┱。因此在體心立方金屬的間隙中所能容納的溶質原子往往比面心立方金屬少,產生的歪扭更嚴重。 有很多證據說明在α-Fe中碳原子不在較大的四面體間隙存身,而存身於較小的八面體間隙。一個超尺寸的原子進入四面體位置後將使周圍四個原子都發生位移,而進入八面體間隙只需移動最近的兩個原子,使晶格在最近原子方向膨脹,因而產生非球對稱的點陣畸變。同時由於碳原子的有序化分布,晶體從體心立方變為體心正方,出現了晶體的正方度。
的相應點(圖2),系由稍壓扁的八面體頂角上6個原子所圍成。距上下兩原子比距其他四個原子略近。間隙半徑r=0.154rа。在 α-Fe中間隙半徑尺寸為0.19┱。因此在體心立方金屬的間隙中所能容納的溶質原子往往比面心立方金屬少,產生的歪扭更嚴重。 有很多證據說明在α-Fe中碳原子不在較大的四面體間隙存身,而存身於較小的八面體間隙。一個超尺寸的原子進入四面體位置後將使周圍四個原子都發生位移,而進入八面體間隙只需移動最近的兩個原子,使晶格在最近原子方向膨脹,因而產生非球對稱的點陣畸變。同時由於碳原子的有序化分布,晶體從體心立方變為體心正方,出現了晶體的正方度。
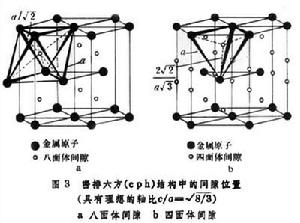
密排六方(cph)結構的八面體間隙(圖3)半徑r≈0.41rа;四面體間隙(圖3)半徑r≈0.225rа。
 點陣中間隙位置
點陣中間隙位置