簡要概述
 基因探針化學發光檢測儀
基因探針化學發光檢測儀一種來自基因組中有關的基因本身,稱為基因組探針(genomic probe);另一種是從相應的基因轉錄獲得了mRNA,再通過逆轉錄得到的探針,稱為cDNA 探針(cDNa probe)。與基因組探針不同的是,cDNA探針不含有內含子序列。此外,還可在體外人工合成鹼基數不多的與基因序列互補的DNA片段,稱為寡核苷酸探針。
探針的製備
進行分子突變需要大量的探針拷貝,後者一般是通過分子克
 基因探針
基因探針為了製備cDNA 探針,首先需分離純化相應mRNA,這從含有大量mRNA的組織、細胞中比較容易做到,如從造血細胞中製備α或β珠蛋白mRNA。有了mRNA作模板後,在逆轉錄酶的作用下,就可以合成與之互補的DNA(即cDNA),cDNA與待測基因的編碼區有完全相同的鹼基順序,但內含子已在加工過程中切除。寡核苷酸探針是人工合成的,與已知基因DNA互補的,長度可從十幾到幾十個核苷酸的片段。如僅知蛋白質的胺基酸順序量,也可以按胺基酸的密碼推導出核苷酸序列,並用化學方法合成。
探針的標記
為了確定探針是否與相應的基因組DNA雜交,有必要對探針加以標記,以便在結合部位獲得可識別的信號,通常採用放射性同位素32P標記探針的某種核苷酸α磷酸基。但近年來已發展了一些用非同位素如生物素、地高辛配體等作為標記物的方法。但都不及同位素敏感。非同位素標記的優點是保存時間較長,而且避免了同位素的污染。最常用的探針標記法是缺口平移法(nick translation)。首先用適當濃度的DNA酶Ⅰ(DNAseⅠ)在探針DNA雙鏈上造成缺口,然後再藉助於DNA聚合酶Ⅰ(DNa poly merasⅠ)的5’→3’的外切酶活性,切去帶有5’磷酸的核苷酸;同時又利用該酶的5’→3’聚酶活性,使32P標記的互補核苷酸補入缺口,DNA聚合酶Ⅰ的這兩種活性的交替作用,使缺口不斷向3’的方向移動,同時DNA鏈上的核苷酸不斷為32P標記的核苷酸所取代。
探針的標記也可以採用隨機引物法,即向變性的探針溶液加入6個核苷酸的隨機DNA小片段,作為引物,當後者與單鏈DNA互補結合後,按鹼基互補原則不斷在其3’OH端添加同位素標記的單核苷酸,這樣也可以獲得比放射性很高的DNA探針。
DNA探針
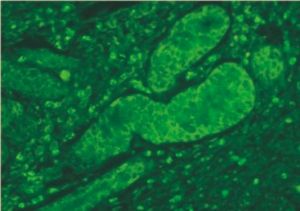 螢光間接標記dna探針檢測
螢光間接標記dna探針檢測對於基因探針的克隆尚有更快捷的途徑。這也是許多重要蛋白質的編碼基因的克隆方法。該方法的第一步是分離純化蛋白質,然後測定該蛋白的氨基或羥基末端的部分胺基酸序列,然後根據這一序列合成一套寡核苷酸探針。用此探針在DNA文庫中篩選,陽性克隆即是目標蛋白的編碼基因。值得一提的是真核細胞和原核細胞DNA組織有所不同。真核基因中含有非編碼的內含子序列,而原核則沒有。因此,真核基因組DNA探針用於檢測基因表達時雜交效率要明顯低於cDNA探針。DNA探針(包括cDNA探針)的主要優點有下面三點:①這類探針多克隆在質粒載體中,可以無限繁殖,取之不盡,製備方法簡便。②DNA探針不易降解(相對RNA而言),一般能有效抑制DNA酶活性。③DNA探針的標記方法較成熟,有多種方法可供選擇,如缺口平移,隨機引物法,PCR標記法等,能用於同位素和非同位素標記。
DNA探針可以用來診斷寄生蟲病,現場調查及蟲種鑑定,可用於病毒性肝炎的診斷,遺傳性疾病的診斷,可用於改造變異的基因,可用於檢測飲用水病毒含量。具體方法:用一個特定的DNA片段製成探針,與被測的病毒DNA雜交,從而把病毒檢測出來。與傳統方法相比具有快速、靈敏的特點。傳統的檢測一次,需幾天或幾個星期的時間,精確度不高,而用DNA探針只需一天。據報導,能從1t水中檢測出10個病毒來,精確度大大提高。
RNA探針
 高辛標記的rna探針
高辛標記的rna探針近幾年體外轉錄技術不斷完善,已相繼建立了單向和雙向體外轉錄系統。該系統主要基於一類新型載體pSP和pGEM,這類載體在多克隆位點兩側分別帶有SP6啟動子和T7啟動子,在SP6RNA聚合酶或T7RNA聚合酶作用下可以進行RNA轉錄,如果在多克隆位點接頭中插入了外源DNA片段,則可以此DNA兩條鏈中的一條為模板轉錄生成RNA。這種體外轉錄反應效率很高,在1h內可合成近10μg的RNA產生,只要在底物中加入適量的放射性或生物素標記的NTP,則所合成的RNA可得到高效標記。該方法能有效地控制探針的長度並可提高標記物的利用率。
值得一提的是,通過改變外源基因的插入方向或選用不同的RNA聚合酶,可以控制RNA的轉錄方向,即以哪條DNA鏈以模板轉錄RNA。這種可以得到同義RNA探針(與mRNA同序列)和反義RNA探針(與mRNA互補),反義RNA又稱cRNA,除可用於反義核酸研究外,還可用於檢測mRNA的表達水平。在這種情況下,因為探針和靶序列均為單鏈,所以雜交的效率要比DNA-DNA雜交高几個數量級。RNA探針除可用於檢測DNA和mRNA外,還有一個重要用途,在研究基因表達時,常常需要觀察該基因的轉錄狀況。在原核表達系統中外源基因不僅進行正向轉錄,有時還存在反向轉錄(即生成反義RNA),這種現象往往是外源基因表達不高的重要原因。另外,在真核系統,某些基因也存在反向轉錄,產生反義RNA,參與自身表達的調控。在這些情況下,要準確測定正向和反向轉錄水平就不能用雙鏈DNA探針,而只能用RNA探針或單鏈DNA探針。
探針標記
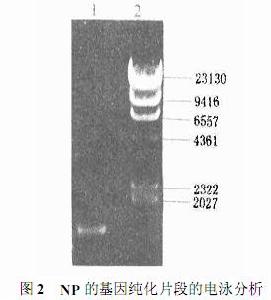 質粒的酶切分析
質粒的酶切分析探針的標記方式有放射性標記和非放射性標記。標記物質有放射性元素(如32P等)和非放射性物質(如生物素、地高辛等)。32P是最常用的核苷酸標記同位素,被標記的dNTP本身就帶有磷酸基團,便於標記。特點是比活性高,可達9000Ci/mmol;發射的β射線能量高。用它標記的探針自顯影時間短,靈敏度高。32P的半壽期短,雖使用不方便,但為廢棄物的處理減輕了壓力。非放射性標記法有酶標法和化學物標記法。酶標方法與免疫測定ELISA方法相似,只是被標記的核酸代替了被標記的抗體,事實上被標記的抗體也稱為探針,現有許多商品是生物素、地高辛標記的。血凝素與生物素有非常高的親和性,當血凝素標記上過氧化物酶或鹼性磷酸酶,經雜交反應最終形成探針-生物素-血凝素酶複合物(ABC法),酶催化底物顯色,觀察結果。ABC法底物顯色生成不溶物,以便觀測結果。酶標記法複雜、重複性差,成本高,但便於運輸、保存,靈敏度與放射物標記法相當。
探針標記方法有:①缺口平移標記法。利用的是DNA聚合酶I能修復DNA鏈的功能。該法先由DNaseI在DNA雙鏈上隨機切出切口,然後DNA聚合酶I沿缺口水解5´端核苷酸,同時在3´端修復加入被標記核苷酸,切口平行推移。缺口平移法快速、簡便、成本相對較低、比活性相對較高、標記均勻,多用於大分子DNA標記,(>1000bp最好),但單鏈DNA、RNA不能用該法標記。②隨機引物法。隨機引物是指含有各種可能排列順序的寡聚核苷酸片斷的混合物,因此它可以與任意核苷酸序列雜交,起到聚合酶反應的引物作用。將待標記的DNA探針片斷變性後與隨機引物一起雜交,然後以此雜交的寡聚核苷酸為引物,在大腸桿菌DNA聚合酶I大斷段(KlenowFragment)催化下,合成與探針DNA互補的DNA鏈,當在反應體系中含有a-32P-dNTP時,即形成放射性同位素標記的DNA探針。具有上述優點,可代替缺口平移法。此外大小、單雙DNA均可標記,標記均勻,標記率高,但也不能標記環狀DNA。隨機引物法標記探針一般長400~600bp。③末端標記法(又叫尾標)。利用末端轉移酶可進行“尾標”,尾標適用於寡核苷酸探針標記,寡核苷酸探針多用於核酸“點”突變的檢測,該探針可用核酸合成儀人工合成,克隆出的探針一般較長,特異性好,標記量大,雜交的檢出信號強。
探針合成的注意事項有:①合成探針的長短,一般在20~50個核苷酸之間。合成過長成本高,且易出現聚合酶合成錯誤,雜交時間長,合成太短則特異性下降。②鹼基組成G-C應含40%~60%,一種鹼基連續重複不超過4個,以免非特異性雜交產生。③探針自身序列內應無互補區域,以免產生“髮夾”結構,影響雜交。總之,一個好的探針最終要在實踐中才能加以確認。
實驗套用
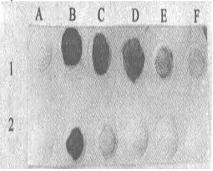 探針濃度鑑定
探針濃度鑑定將禽流感病毒H9N2亞型毒株核蛋白(NP)基因3′端較為保守的、約350bp的編碼序列通過限制性內切酶Hae¸切割、分離後,用隨機引物法製備Digoxigenin2112dUTP標記探針。測定該探針的濃度為100Lgöml。特異性試驗發現該探針只能與實驗室構建的、含有NP基因的重組載體pGEM2TE2NP和pBacPAK2NP以及A型流感病毒H9N2亞型、H3N2亞型以及H9N3亞型毒株基因組RNA結合出現特異性的顏色反應,而與實驗室常用的載體pGEM2Teasy、pBacPAK2His3、pTARGET和pGEMEX22以及新城疫病毒、傳染性支氣管炎病毒和傳染性喉氣管炎病毒基因組不發生反應。套用該探針檢測含NP基因的重組載體和重組病毒證明該探針是有效的,可用於含禽流感病毒樣品或材料的檢測。
DNA探針原位雜交
1、4—6微米切片,用防脫片膠(多聚賴氨酸)處理過的玻片貼附
2、56—60℃烤片2—16h
3、新鮮二甲苯脫蠟,10minX2(趁熱脫蠟)
4、100%乙醇5minX2次,不用浸水,直接空氣乾燥
5、加入50μl蛋白酶K工作液(蛋白酶K用蒸餾水稀釋,濃度為25μg/ml),37℃消化10—15min
6、棄去蛋白酶K工作液,0.1MTBS洗滌3minX3次逐級酒精脫水(85%,95%,100%酒精)1minX3次然後空氣乾燥
7、加入20μl探針,加蓋薄膜。(探針用預雜交液稀釋,濃度為5μg/ml)。
8、95℃變性10—12min;立刻置於冰塊上,防止復性。
9、37℃雜交16—20h
10、揭去薄膜,每張切片加入以下雜交後洗滌液:
>用2—3滴2XSSC37℃洗滌3minX2次;
>0.5XSSC37℃洗滌3minX2次;
>0.2XSSC37℃洗滌3minX2次;
11、0.1MPBS/TBS緩衝液洗滌,1minX3次
12、滴加小鼠抗地高辛生物素標記的抗體工作液,37℃孵育45—60min;
13、0.1MPBS浸洗,5minX3次
14、滴加高敏鹼性磷酸酶鏈親和素複合物工作液,37℃孵育45—60min。
15、0.1MPBS浸洗,5minX3次
16、滴加NBT/BCIP顯色6—16h,
17、雙蒸水終止反應(37℃10min—2h),雙蒸水浸洗,5minX2次
18、滴加核固紅,30秒—5min;
19、雙蒸水浸洗,5minX3次
20、脫水、透明、封片
