同位素交換
正文
兩種同位素原子在兩個不同分子或離子間或一個分子的不同位置上的化學交換,以及兩種同位素分子在不同聚集態之間的交換。類型 同位素交換反應類型主要分為三種:
① 不同取代級的同位素分子間的歧化反應,例如:
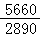
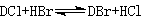
同位素交換反應是可逆的,並且和一般的化學反應一樣,其反應進行的程度可用平衡常數來表示。這是等分子反應,而且反應前後化學組分不發生變化,僅同位素的濃度在各化學組分之間重新分配。
機理 同位素交換反應機理主要分為:①電離機理,進行同位素交換的分子先解離成離子或自由基,在複合為分子時發生同位素的重新分配,例如:
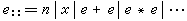
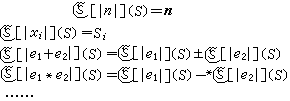
同位素交換反應已用於揭示化學反應機理及分子結構和性質的研究中,還廣泛用於輕元素的同位素分離中。
