同位素分離
正文
將某元素的一種或多種同位素與該元素的其他同位素分離或富集的過程。同位素的發現依賴於同位素分離的實現。直至20世紀30年代初,同位素分離的目的主要是為了分析、研究元素的同位素組成。1931年發現重氫後,建立了重水生產工廠。在H.C.尤里提出同位素化學交換的理論後,建立了各種化學交換法分離同位素的裝置。40年代以來,由於核工業的需要,同位素分離技術得以長足發展。鈾235、重水、鋰 6、硼 10以噸量級生產,並建立了大規模分離同位素過程的級聯理論。碳13、氮 15、氧18、硫34等以千克量生產,主要作示蹤原子。方法分類 各種分離混合物的方法均可用來分離同位素,根據分離原理可以分為五大類:①根據分子或離子的質量差而進行分離的電磁法、離心法等;②根據分子或離子的運動速度不同而進行分離的擴散、熱擴散、分子蒸餾、電泳法等;③根據熱力學同位素效應而進行分離的精餾法、化學交換法、氣相色譜法、超流動性法等;④根據動力學同位素效應而進行分離的電解、光化學法、雷射法等;⑤根據生物學同位素效應而進行的分離。
根據分離過程,各種方法可分類如下:
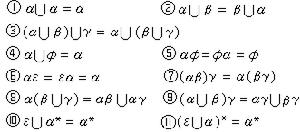
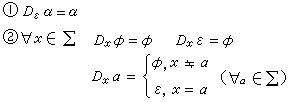
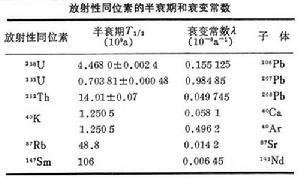 同位素分離
同位素分離分離方法 氣體擴散法 又稱孔膜擴散法。根據同位素分子通過孔膜(孔徑約0.01~0.03微米)擴散速度的不同來分離同位素。結果,輕同位素富集在隔膜一側,重組分富集在隔膜的另一側。擴散法是分離鈾 235的主要方法,以六氟化鈾為原料,分離係數α=1.0043,由幾千個級組成級聯以生產濃縮鈾。(見鈾同位素分離)
電磁分離法 它的工作原理與質譜法相類似。經第一次分離即可得到高富集的同位素,但產量很小,早期曾用於生產濃縮鈾,後來主要用於生產克量級的重同位素,供科研使用。
熱擴散法 當組成均勻的氣體或液體混合物中有溫度梯度時,輕組分將富集在熱區而重組分將富集在冷區,這就是熱擴散效應。熱擴散法就是根據這一效應發展起來的。常用的裝置為熱擴散柱,其工作原理如圖所示。
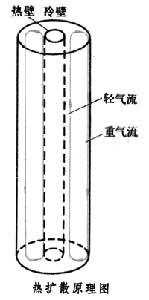 將欲分離的同位素混合物放在兩個垂直的同心圓管中間,內管加熱,外壁冷卻。由於熱擴散效應,輕組分在熱壁表面附近富集,重組分在冷壁表面富集,同時內壁附近氣體受熱上升,外管內壁附近氣體因冷卻下降。由於熱對流的結果,富集了的輕組分氣體和重組分氣體經多次逆流接觸,使得簡單熱擴散效應效果倍增。熱擴散柱結構簡單,操作方便,套用範圍廣泛,是實驗室中分離輕同位素的主要手段。
將欲分離的同位素混合物放在兩個垂直的同心圓管中間,內管加熱,外壁冷卻。由於熱擴散效應,輕組分在熱壁表面附近富集,重組分在冷壁表面富集,同時內壁附近氣體受熱上升,外管內壁附近氣體因冷卻下降。由於熱對流的結果,富集了的輕組分氣體和重組分氣體經多次逆流接觸,使得簡單熱擴散效應效果倍增。熱擴散柱結構簡單,操作方便,套用範圍廣泛,是實驗室中分離輕同位素的主要手段。 質量擴散法 根據同位素混合物的不同組分在第三種氣體(稱為分離劑)中擴散速度的不同來分離同位素。單級分離效率甚低。為得到高效分離,必須採用級聯式質量擴散柱。此法適用於小規模的中等原子量元素的同位素分離。
離心法 根據質量不同的氣體分子在離心場中的平衡分布不同來分離同位素。離心法的分離係數與絕對質量差有關,因此該法對分離重同位素(特別是鈾235)有利。離心法單級分離係數高,最高可達1.5~2,因此,生產濃縮鈾 235需要級數少。台離心機處理物料量小,需要大量離心機並聯工作。由於超速離心技術的發展,離心法分離鈾同位素可與擴散法競爭,並已建立了中間工廠。
精餾法 元素各同位素及其化合物的蒸氣壓有差別,可以用精餾法分離同位素。精餾的分離係數等於被分離二組分純蒸氣壓之比,並且隨溫度的降低和分子量的減少而增加。由於精餾法的工藝成熟、方法簡單可靠,一些輕同位素多用此法來生產,如用低溫精餾一氧化碳、一氧化氮、三氯化硼來生產碳13、氧18、氮15、硼10等同位素。工業上也曾用水的精餾來生產噸量級的重水。精餾法已用於將雙溫法生產的濃度約15%的重水富集到高於99.8%。
化學交換法 同位素化學交換法是分離輕同位素的一種特殊方法。它是基於在同位素化學交換反應中,同位素在各反應分子間的分布不是等幾率的。工業上大量生產重水,就是利用硫化氫和水之間的同位素交換反應。由於輕元素同位素分子間的零點能相差大,交換反應的分離係數大,而且交換過程在熱力學平衡條件下進行,能量消耗小。因此,化學交換法在輕同位素生產中占重要地位。一些重要的同位素如氘、氮15、硼10、鋰 6都用此法生產。
電解法 根據一元素的各同位素在電極上析出速度的不同來分離同位素。電解水時,氫同位素氕和氘的分離係數在 3~12之間。電解分離係數受電極材料、電極表面狀況、電流密度和溫度等因素的影響。工業上最初生產重水就是用電解法。氫以外其他元素的同位素在電解時分離係數都接近1,因此用電解法生產的實用價值不大。
光化學法 由於同位素核質量的不同,使原子或分子的能級發生變化,從而引起原子或分子光譜的譜線位移。光化學法就是利用同位素分子在吸收光譜上的這種差異,用一定頻率的光去激發同位素混合物中的一個組分,而不激發其他組分,然後利用處於激發態的組分和未激發組分在物理或化學性質上的不同,在激發態原子或分子能量未轉移之前,採用適當的方法把它們分離出來。在雷射出現以前,人們就利用光化學法分離汞同位素。60年代雷射出現以後,由於雷射具有單色性、強度高和連續可調等特點,使雷射同位素分離成為雷射套用的一個重要領域,已在實驗室範圍內成功地分離了十幾種同位素。鈾235的雷射分離很受重視,無論原子法或分子法在實驗室都已取得結果。原子法是在高溫下得到鈾蒸氣,再通過兩步光激發使235U電離成235U+,然後用負電場將235U+和未電離的238U分離。分子法是用惰性氣體將氣態UF6稀釋後,經過超聲絕熱膨脹,使UF6的溫度降至30~50K,從而得到良好的同位素譜線位移,再用雷射將235UF6激發和電離,而與238UF6分離。(見彩圖)
 同位素分離
同位素分離參考書目
H.London, ed.,Separation of Isotopes, George Newnes, London, 1961.
S.維拉尼著,陳聿恕等譯:《同位素分離》,原子能出版社,北京,1983。(S.Villani,Isotope Separation,American Nuclear Society, Hinsdale, 1976.)
