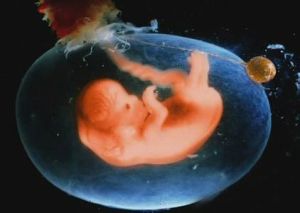
病因
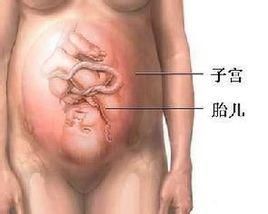 子宮和胎兒
子宮和胎兒(1)胎膜發育不良:原因很多除胎膜本身因素外,孕早期孕婦維生素C缺乏、銅缺乏和孕婦吸菸等因素與胎膜發育不良有關。
(2)感染:胎膜早破導致宮腔感染是傳統的胎膜早破和感染的因果關係,近些年已經普遍認識到感染和胎膜早破互為因果關係,而且感染是胎膜早破的最重要原因。
(3)子宮頸功能不全:在非妊娠的狀態下,子宮頸內口可以無阻力地擴大到8.0號即可以診斷子宮頸功能不全子宮頸功能不全主要表現在內口鬆弛和峽部缺欠。
(4)宮腔內壓力異常:宮腔內壓力不均常見於頭盆不稱和胎位異常;宮腔內壓力過大常見於雙胎妊娠,羊水過多,劇烈咳嗽和排便困難等。
(5)創傷和機械性刺激:主要分為醫源性和非醫源性2類。非醫源性常見的為妊娠晚期的性交活動;醫源性的包括多次羊膜腔穿刺,多次陰道檢查和剝膜引產等。
發病機制
 胎膜早破
胎膜早破2、子宮頸功能不全關於感染導致胎膜早破的研究很多,機制複雜,概括起來有如下2點:①細菌和細菌性炎症破壞胎膜的結構:細菌本身和細菌誘發的炎症反應過程可以產生大量酶類,特別是膠質酶和含金屬蛋白酶類,可以破壞胎膜的膠質,最後導致羊膜的張力強度和彈性下降;②誘發子宮收縮羊膜腔內壓力增加:誘發子宮收縮的機制主要分為細菌本身的產物和細菌誘發的母體的炎症反應過程。細菌本身產物主要指破碎或裂解的細胞壁產生的磷脂酶A2,可以誘發宮縮。母體炎症反應過程導致子宮收縮的機制相對複雜主要有:參與炎症過程中免疫應答的免疫細胞產生白介素類細胞因子白介素可以誘發宮縮;參與炎症反應過程的炎症介質如花生四烯酸系統產生的前列腺素如PGE2和PGF2,此類物質可以誘發強烈的子宮收縮。
3、胎膜被拉伸隨妊娠進展子宮增大,宮腔內壓力增加,宮頸不能承受逐漸增大的正常壓力而擴張,胎膜也隨之向宮頸外口乃至陰道方向伸展突出形成前羊膜囊,前羊膜囊的徑線逐漸增大,胎膜承受的拉力越來越大,胎膜被拉伸,最後超過胎膜的彈性強度而破裂。
4、宮腔內壓力異常包括宮腔內壓力不均和宮腔內壓力過大。
臨床表現
1、症狀有或沒有各種原因突然陰道排液,排液的量可多可少。排液通常為持續性,持續時間不等,開始量多然後逐漸減少少數為間歇性排液,陰道排液通常與孕婦體位變動、活動與否有關。
2、體徵孕婦仰臥位可能見到陰道口有液體流出,也可能無任何液體流出;如無液體流出,肛查時上托陰道後穹隆上推胎頭按壓宮底或孕婦變動體位可有液體由陰道口流出,注意這些輔助操作後可能仍不見液體流出。所流出的液體通常稀薄,可能混有胎糞或胎脂。急症住院病人可能帶內衣衛生棉或衛生紙來醫院,應該仔細檢查。
併發症
主要併發症為感染包括母體子宮盆腔和全身感染及胎兒肺部感染、敗血症和小腸結腸炎等。
診斷
根據臨床表現及必要的輔助檢查即可做出診斷。同時必須判斷是否有羊膜腔感染,是否有羊膜腔感染直接影響其後的處理方法。
1.陰道分泌物PH值測定
可用試紙法測定,如pH≥7,多已破膜,因陰道pH值為4.5~5.5,而羊水為7~7.5。
2.陰道液體塗片
待乾後鏡檢,查見羊齒狀結晶,用0.5‰美蘭染色查見淡藍色或不著色的胎兒上皮及毳毛;用0.1~0.5%硫酸尼羅蘭染色,查見桔黃色胎兒上皮細胞,均可診斷胎膜早破。
3.經腹羊膜腔穿刺
注入靛胭脂如由陰道流出,診斷可確定。
治療
足月前胎膜早破可根據情況行期待治療或終止妊娠。足月胎膜早破根據情況選擇終止妊娠的方法,引產或剖宮產。不論何種情況破膜超過12h要預防性套用抗生素。
1、胎膜早破治療原則的確定胎膜早破一旦確診需要根據病人的特點制定治療方案,決定治療方案的因素很多如孕周、是否合併感染、有無胎兒窘迫、有無羊水過少和新生兒學水平其中最重要的是孕周、是否合併羊膜腔感染。
(1)胎膜早破的重要問題是早產和早產兒的相關問題:早產兒的存活率主要由早產兒的重要臟器特別是肺的成熟度來決定,而肺的成熟度隨孕周的增加而增加。下列關於肺的成熟情況與孕齡的關係是依據孕齡制定胎膜早破的治療方案的主要依據:妊娠37周后,胎兒肺功能發育成熟;妊娠達34~36周,胎兒肺功能基本發育成熟,妊娠期糖尿病或妊娠合併糖尿病患者除外;妊娠達29~33周者,延長孕齡並套用促進胎肺成熟藥物可以提高肺的成熟度,明顯降低新生兒肺透明膜病的發生;妊娠24~28周者套用促胎肺成熟藥物,適當延長孕齡可以降低新生兒的死亡率但是否降低新生兒肺透明膜病尚不肯定;妊娠23周前研究很少,新生兒存活率幾乎為零。
(2)感染:指羊膜腔感染,胎膜早破合併羊膜腔感染是終止妊娠的指征。根據羊膜腔感染和胎膜早破的因果關係或時間次序,可以將感染分為原發感染和繼發感染原發羊膜腔感染在胎膜破裂前已經存在是胎膜早破的主要原因。繼發感染是在胎膜早破發生一定時間後出現,既可以是原有感染在胎膜破裂時未能診斷而於觀察期加重,也可以是胎膜破裂後宮頸或陰道內細菌的上行感染,其中繼發感染的出現與否是胎膜早破患者進行期待療法期間所要觀察的重要指標繼發感染通常在胎膜破裂後12h即可以出現,隨胎膜破裂的時間的延長而增加。羊膜腔感染分為亞臨床型和臨床型,具體診斷依據見羊膜腔感染綜合徵一節。
 胎膜早破
胎膜早破2、期待療法對於孕34周前,特別是孕28~34周的患者,為使胎兒宮內繼續生長發育,以提高胎兒娩出後的存活率為目的而採取的綜合治療方法的總稱。期待療法包括一般治療、抑制宮縮、促進胎肺成熟和預防感染等多種治療措施,適用於胎膜早破而無感染、無胎兒窘迫和無羊水過少者。
(1)一般治療措施:包括絕對臥床休息,平臥位或側臥位抬高床尾,保持外陰清潔避免陰道檢查和肛查等
(2)胎兒監測:定期行胎兒電子監護,必要時行生物物理評分,以判斷胎兒宮內情況;定期行B超檢查,記錄羊水量,胎兒生長發育情況。
(3)促進胎肺成熟:促進胎肺成熟的方法主要有腎上腺皮質激素、促甲狀腺激素和β受體激動劑如沙丁胺醇和利托君(羥苄羥麻黃鹼)等最常用的是2種腎上腺皮質激素類藥物地塞米松和倍他米松,2種藥物的用法和用量基本相同。地塞米松的國內外主要套用方案:①地塞米松6mg肌內注射或靜脈注射,2次/d,共2天;②地塞米松l0mg肌內注射或靜脈注射1次,共3天;③地塞米松10mg羊膜腔注入1次。
腎上腺皮質激素促胎肺成熟的注意事項:①適用於妊娠周數<34周或超過34周明確胎兒肺功能不成熟者;②激素可以掩蓋感染加重感染,套用時應嚴密監測感染的發生並預防感染;③主要套用地塞米松和倍他米松用法和用量基本相同;④給藥途徑可以肌內注射、靜脈注射或羊膜腔穿刺;⑤藥物24h後發揮作用,並持續1周;⑥1周后可以重複給藥,用法相同,但重複給藥的作用不確切;⑦妊娠期糖尿病患者34周前必須套用,建議通過羊膜腔用藥用藥期間監測血糖並調整胰島素用量以防高血糖、酮症或酮症酸中毒的發生;⑧妊高征患者用藥期間可能引起血壓波動或水電解質紊亂;⑨對新生兒腎上腺輕度抑制,但無臨床意義。
(4)抑制宮縮:抑制子宮收縮是期待療法的一項重要治療措施,分為預防性和治療性抑制宮縮治療,前者無論宮縮有無常規抑制宮縮治療,後者只有宮縮出現時才套用宮縮抑制劑。胎膜早破時宮縮抑制的方法很多,主要有硫酸鎂、β受體激動劑一氧化氮(NO)供體類藥物鈣通道阻斷劑和非甾類解熱鎮痛藥等。
①硫酸鎂:硫酸鎂抑制子宮收縮的有效血藥濃度需要達到2~4mmol/L,用量和用藥速度要求很高,常用法:首劑為衝擊量4g,靜脈;維持量1.5~2.0g/h靜脈。上述方案為國內常見的方案,國外文獻報導的方案通常為首劑為衝擊量6g靜脈;維持量2.0~3.0g/h,靜脈。由於有效劑量和中毒乃至致死劑量接近,使用時須嚴密監測,並做好解毒準備。臨床工作中發現,腎功能不全患者容易發生硫酸鎂中毒,即使該患者的尿量超過600ml/d究其原因可能是該患者腎小球濾過率低,而腎小管的濃縮能力差,所以對實際排出的尿液中硫酸鎂的總量低,最後導致硫酸鎂的體內蓄積,甚至鎂中毒相反對於腎功能正常患者,如急性闌尾炎闌尾切除術後的患者,採用硫酸鎂抑制宮縮此類患者腎功能通常正常,每天補液3000ml左右,尿量約2500ml,由於腎臟排鎂能力強,所以該類患者的血鎂又很難達到理想濃度。近些年國外的研究發現,大量使用硫酸鎂抑制子宮收縮容易導致圍生期肺水腫,該類肺水腫通常為良性肺水腫,如注意提高患者的膠體滲透壓和預防感染,通常72h內即可消退。
 胎膜早破
胎膜早破③非甾類解熱鎮痛藥:該類藥物的作用機制是通過作用於花生四烯酸系統,抑制前列腺素的生成從而抑制子宮收縮。常用的有吲哚美辛、阿司匹林和舒林酸(蘇靈大)具體用法如下:吲哚美辛25mg,3次/d;阿司匹林O.5~1.0mg,3次/d;舒林酸(蘇靈大)200mg2次/d
④一氧化氮(NO)供體藥物——硝酸甘油:硝酸甘油用於抑制子宮收縮的研究僅十幾年的歷史,可以滿足產前、產時和產後各種需要的子宮收縮抑制的套用產前套用主要用於早產和子宮頸功能不全的子宮收縮抑制,使用劑型為外用藥——硝酸甘油貼,經皮膚給藥,滲透劑量相當於0.4~0.8mg/h,通常24~48h見效,1片無效,1h可以加用1片。如果無硝酸甘油貼可以按0.4~0.8mg/h的速度靜脈點滴。產時和產後主要用於子宮收縮過強而導致的胎兒窘迫和下列情況下的手術操作如子宮內翻、胎盤滯留內或外倒轉、不協調子宮收縮等。用法:50~200μg硝酸甘油,靜脈推注1min內見效,3~5min後可以重複,套用時應該注意孕婦的頭痛症狀和低血壓反應上述劑量的硝酸甘油滴於舌下可以達到相同的效果。
⑤鈣通道阻斷劑:常用硝苯地平,每次10mg1天可以用多次。
(5)防治感染:對於感染應該包括預防和治療2種,預防感染指胎膜破裂伊始無感染套用抗生素,目的在於預防羊膜腔感染的發生或延緩出現時間;治療感染主要針對於胎膜破裂前已經存在但未診斷的羊膜腔感染、胎盤炎和宮頸和陰道的感染。胎膜破裂後12h未臨產者需要加用抗生素,所用抗生素以青黴素族、頭孢類和紅黴素為首選,注意抗菌譜廣;因為現代理論認為感染是胎膜早破的重要原因,胎膜早破多數患者可能有亞臨床感染,所以建議首先靜脈套用抗生素2~3天,然後改口服抗生素維持。
3、終止妊娠胎膜早破終止妊娠的方式以陰道分娩為主,如有產科指征可以剖宮產。
預後
1、感染感染與胎膜早破互為因果關係,羊膜腔子宮頸和胎盤胎膜的感染可以導致胎膜早破,胎膜早破還可以引起感染胎膜早破引起的感染指胎膜破裂後寄生於子宮頸管和陰道的致病菌上行通過胎膜破裂部位引起的胎兒、妊娠組織(臍帶、胎膜和胎盤)、子宮乃至盆腹腔和全身感染。胎兒感染常見肺感染、敗血症和小腸結腸炎,孕婦感染主要指分娩前的羊膜腔感染綜合徵和產後的產褥感染胎膜早破所引起的孕婦和胎兒的感染隨潛伏期的延長而增加。胎膜早破所引起的感染可能是新發感染,也可能是原有感染加重或合併新的感染。
2、臍帶異常胎膜早破引起的臍帶異常主要為臍帶脫垂和臍帶受壓。臍帶脫垂常見於胎膜早破合併頭盆不稱胎位異常,羊水過多等。臍帶受壓主要是隨著羊水不斷流出,導致羊水過少,在胎兒靜止胎兒運動和子宮收縮等各種條件下均可以導致臍帶受壓,嚴重者造成胎兒窘迫,
3、難產胎膜早破前羊水囊消失,臨產後前羊水囊擴張子宮頸的作用消失,造成難產;同時後羊水消失合併感染等因素同樣可以造成難產。
4、胎兒畸形主要見於破膜時孕齡較小,保守治療時間較長,羊水較少等情況,常見的畸形包括肢體、面部器官和呼吸系統畸形。
5、早產和早產兒胎膜早破早產占所有早產的40%胎膜早破的早產兒的病死率成倍增高,死亡的主要原因是新生兒肺透明膜病。
孕產醫學術語
| 懷孕生子對很多人來說都是頭等大事,有關孕產的醫學術語是否大家都熟知呢?本任務帶大家一起來熟悉孕產相關的醫學術語。 |