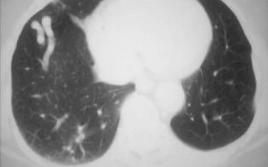
臨床要點
1.常有少量咯血,破裂後破入胸腔可致血性胸水,破入大支氣管可有大量咯血。
2.低氧血症紫紺、杵狀指、易疲勞、工作負荷能力降低。
3.異位栓塞如腦梗死、腦膿腫。
4.動靜脈畸形貼近胸壁時,能聽到雜音。
影像表現
X線:
1.胸片和透視肺野內結節狀陰影,病灶與肺門之間有粗大的血管影相連,透視下大多數病灶有搏動。
2.DSA檢查
1)單發或聚集的大小不同的或相仿的結節狀血管湖。
2)瀰漫性毛細血管擴張。
3)散在的分布與單一粗大的肺動脈連線,相應的肺靜脈提前充盈。
CT:
1.分葉狀圓形或橢圓形病灶,邊緣可見有異常血管與肺門相連的“血管蒂征”(圖8-2-3A8-2-3B8-2-3C8-2-3D8-2-3E8-2-3F)。
2.增強後病灶與肺動脈同步強化,引流的靜脈及左房提早顯影。
3.MPR示病灶與肺門相連的異常血管影。
病因
PAVMs約80%為先天性,此畸形是一種肺毛細血管的發育異常。在胚胎髮育過程中肺芽周圍的靜脈叢與第六對主動脈弓衍生來的肺動脈樹相吻合。隨著胚胎的發育,此處的血管床出現血管間隔,形成肺毛細血管,於是將肺芽水平的原始動靜脈叢分隔開,一旦上述血管間隔的形成發生障礙,肺毛細血管的發育不完全即出現一種或多處肺動靜脈瘺。研究發現大多數先天性PAVMs伴發HHT,後者是一種常染色體顯性遺傳病。目前已知HHT至少與三種染色體上的基因位點相關,後者HHT1是由染色體9q3位點上的基因突變所致,HHT2由染色體位點上的基因突變所致。同時發現大約15%-35%的HHT伴發PAVMs,因此有人推測PAVMs也是一種基因突變所致的遺傳性疾病。
PAVMs亦可由後天性病變引起,如肝硬化,外傷,手術,二尖瓣狹窄,結核病、血吸蟲病、轉移性甲狀腺癌。此外,懷孕可導致PAVMS的生長速度加快,引發相關的併發症。
病理
PAVMs好發於兩肺的下葉,多為單側病變,僅8-10%為雙側病變。大約50-75%為單發,30%為多發性。單發病變最多見於左肺的下葉,其次為右肺下葉,左肺上葉、右肺中葉、右肺上葉,多發病變多見於雙下肺,雙側同時受累的約占8-20%,瘺口多接受胸膜,在肺實質者少見。
在病理上可分兩型,即囊型和瀰漫型。前者瘺道部形成紆曲的團狀血管瘤囊,瘤壁厚薄不均,又分為單純型和複雜型。單純型為1支供血肺動脈與1支引流肺靜脈直接溝通,瘤囊無分隔;複雜型為2支以上的供血肺動脈與引流肺靜脈直接溝通,囊腔常有分隔。瀰漫型可局限於一個肺葉或遍及兩肺,動靜脈之間僅有多數細小瘺道相連,而無瘤囊形成。研究發現大約(80-90%)的PAVMs屬單純型,約95%的PAVMs由肺動脈供血,其餘的由體循環動脈或兩者同時供血。參與體循環供血的動脈包括胸主動脈,乳內動脈、肋間動脈、冠狀動脈等異常分支。少數病為兼有肺靜脈異常。
肺動靜脈的異常結構生後早期常處於潛伏狀態,而後在肺動脈壓力作用下病變逐漸發展擴大,瘤壁亦有相應的繼發退形性改變。如遇胸部外傷,菲薄變性的囊瘺易破裂,導致大出血,血胸或大咯血,繼而形成局限性含鐵血黃素沉著症。
病理生理
PAVMs一般不影響心臟的血液動力學、心輸出量,心臟指數及肺毛細血管楔入壓等多在正常範圍,故心率、血壓、心電圖大多正常。但個別報導心臟指數可增加或降低。部分肺動脈血未經肺泡進行氣體交換,直接進入肺靜脈,回至左心,並進入體循環,形成病理性動靜脈分流,血流動力學上屬於心外右向左分流,使PAVMsSaO2和氧飽和度皆有不同程度的下降。
由於正常動靜脈血間的氧分壓達50mmHg,而二氧化碳分壓並僅6mmHg,所以動靜脈分流時靜脈血進入動脈系後,混合血中氧分壓下降程度大於二氧化碳分壓升高的程度。而且由於氧氣和二氧化碳解離曲線的不同,機體對缺氧和二氧化碳瀦留產生不同的代償效果。缺氧反射性地引起呼吸加深加快,但流經通氣肺泡的毛細血管內的血液已達到很高的氧飽和度,血氧氣含量亦不會再明顯增加。而二氧化碳解離曲線則在生理範圍內基本上呈直線式,故通氣增加後就可排出更多的二氧化碳。此外,由於二氧化碳分子經肺泡膜彌散較氧氣大20倍,因此PAVMs患者的動脈血二氧化碳分壓可以正常,甚至有所下降。微小的PAVMS造成的二氧化碳分壓輕微下降臨床上不易測出。大的PAVMS使氧分壓明顯下降,並常繼發紅細胞增多症,因此,雖然氧分壓及飽和度低於正常,而血氧含量仍可正常或接近正常。
臨床表現
PAVMs雖然是先天性疾病,但很少在嬰幼兒時期發病,相關症狀常常在40-60歲時出現,但可能是由於幼兒時期PAVMs微小,不引起明顯的血流動力學改變,而且X線檢查也不易發現。
PAVMs症狀的嚴重程度與病變大小密切相關。部分患者(13-55%)無明顯症狀,偶爾在X線檢查時才被發現。伴發HHT的患者,常為多發性PAVMs,病變多為快速進展型,瘺囊可增多,症狀更常見,併發症發生率高。
通常,單個孤立的PAVMS直徑<2cm時不引起症狀,多發性患者出現臨床症狀的幾率大於單發者,而瀰漫性PAVMs患者無例外都有症狀。
當分流量大於20%及病史長者可出現呼吸困難,它是臨床最常見的且早期出現的症狀,靜息時稍好,活動後加重;在大的或多發性PAVMS患者常見,而在有杵狀指患者中幾乎都存在。呼吸困難的程度與低氧血症的嚴重程度和右向左分流量的大小有關。大多數患者對低氧血症耐受性好,一般只有在氧分壓低於60mmHg時才有乏氧症狀,其次是鼻出血,它以自發性或輕微觸碰即可引發為特徵,系由鼻黏膜毛細血管擴張出血所致,這一表現反映了PAVMs患者中HHT的高發病率;第三是咯血,大咯血不少見,但很少致病;再次是皮膚,胃腸道的毛細血管擴張出血、胸痛、咳嗽、偏頭疼、耳鳴、頭暈等。
常見的體徵有紫紺、杵狀指(趾),病變部位的雜音出現於右向左分流量較大時,偶可觸及震顫。有報導稱,通過認真仔細的體格檢查,75%以上的患者可有異常發現。約46%的PAVMS可在胸部聽到連續性或收縮期血管性雜音,雜音響亮程度較多地取決於動、靜脈之間的壓力差,不一定和瘺口大小有關。該雜音吸氣時增強,呼氣時減弱(原因為吸氣時胸膜腔負壓增大,肺內毛細血管含血量增多,由肺靜脈回到體循環的血量少於右心室進入肺循環的血量,體循環的動脈血壓降低,體循環與肺循環的動脈壓差別減小,肺動靜脈畸形的血流量增多,而呼氣時情況相反)。由於PAVMs主要是肺部下葉病變,患者可表現直立性低氧血症。
併發症
PAVMs可以引起嚴重的併發症,但是適當的治療常常可以預防它們的發生。最常見是神經系統的併發症,發生率約為30%,尤其多見於瀰漫性PAVMS患者。包括中風(18%)、偏頭痛(43%)、短暫性腦缺血發作(37%),腦膿腫(9%),癲癇發作(8%)。文獻報導稱神經系統的併發症幾乎全部發生於供血動脈直徑>3mm者。
另外還可並發肺動脈高壓,矛盾性栓塞,感染性心內膜炎,貧血、咯血、血胸、紅細胞增多症等,其中血胸一般是胸膜下的PAVMs破裂至胸膜腔所致,而咳血一般是PAVMS破裂至支氣管或支氣管內擴張的毛細血管破裂所致,兩者均是可危及生命的併發症。矛盾性栓塞是最常見的引起非感染性腦血管意外的原因。紅細胞增多症和貧血的發生率分別為25%和17%,紅細胞增多症及合併存在的腦AVMs是少見的腦血管意外發生的原因。肺動脈高壓的原因尚不明確,有文獻認為與慢性低氧血症有關,可促使PAVMS很快增大,使病情加重。個別伴有肺性骨關節病。
診斷
診斷PAVMs的方法很多,現將目前臨床常用的較敏感的幾種方法綜述如下:
胸部X線檢查簡便易行、敏感、無創且經濟,目前作為PAVMS的一線篩選檢查。有報導約98%患者的胸片有異常表現。囊狀PAVMs通常具有典型X線平片徵象,表現為孤立或多發的類圓形陰影,陰影直徑通常在1-5cm範圍,大小不等,密度均勻,邊緣清晰,或有淺分葉;擴張增粗的供血動脈和引流靜脈連於陰影,供血動脈與肺門相連,一般直徑為4-7mm,偶爾有大於2cm者;該陰影一般不增大或緩慢增大,約66%的陰影位於下肺。透視下,深吸氣時病灶增大,呼氣時病灶縮小。根據上述特點,結合臨床資料多數可作出明確診斷。不典型者有進僅表現為大片緻密影,類似炎症表現,平片診斷有一定困難。瀰漫型PAVMS多缺乏典型X線徵象,可表現為肺葉或肺段分布瀰漫型結節網狀、斑點狀陰影,也可表現為肺紋理增多、扭曲,有的平片無陽性所見。因此診斷困難,需進一步做其他檢查。
超聲心動圖聲學造影診斷有臨床意義的PAVMs的敏感性幾乎為100%,甚至能發現那些很少的沒有臨床意義的PAVMs。同時因為它是無創檢查,目前廣泛地被套用。具體方法如下:從外周靜脈注射振盪過的生理鹽水或碳酸氫鈉(此時可產生小氣泡),然後做超聲心動圖檢查。正常情況下小氣泡將完全被阻止在肺毛細血管中,不會進入左房。但是當有PAVMs存在時左房內很快出現氣泡。超聲心動圖聲學造影對判斷心外右向左分流非常有用,可用於栓塞治療後的療效評價及HHT患者家庭成員的篩檢工作。它的缺點是不能確定病變的部位和範圍,不能判定分流要數。
肺灌注核素掃描是診斷PAVMs的一種敏感性很高的方法,能確定病變的部位和範圍,並能測定分流分數。方法如下:從外周靜脈注射99mTc-白蛋白(微粒直徑7-25UM)。正常情況下這些微粒不能通過肺毛細血管,當PAVMs存在進它們可經肺臟隨血流到達腦腎等器官。通過肺臟和腎臟的核素掃描可測定分流分數。Whyte等發現該方法和純氧試驗的結果有很好的相關性,而且後者相比有以下優點:不需要取動脈血樣:更適於運動時的分流測定。缺點是不能區分肺內和心內的分流,無法觀察具體的解剖細節,同時價格較高。
螺旋CT及電子束CT(EBCT)是診斷PAVMs的一種有效手段。隨PAVMS類型的不同,CT表現有所不同。單發或多發具有瘤囊者平掃可顯示大小不等呈中等密度的圓形、橢圓形或分葉多囊狀影,CT值與血管一致。明顯者可見與其相連的迂曲、擴張的血管影。增強後瘤囊迅速強化,峰值與右心-肺動脈充盈期一致。至左心期強化程度下降。同時,還觀察到供血、引流的肺動、靜脈,“團注”的速度增強掃描效果更好。多發或瀰漫型PAVMS主要右下葉表現眾多小結節網狀結構,造影可見增強和擴張的血管影,但很難看到動、靜脈的連通。Remy等研究發現對比增強EBCT在PAVMs的正確診斷及解剖結構顯示方面明顯優於肺動脈造影。
3-D螺旋CT採用表面陰影顯示法可以從各個角度顯示血管結構,準確性高。一項研究表明3-D螺旋CT對PAVMS的檢出率較肺動脈造影高2倍多。3-D螺旋成像與橫斷位成像聯合診斷PAVMS的準確性可達95%。但為手術或介入治療選擇適應證,明確本畸形的形態細節,葉、段、亞段支以遠分支的多發或瀰漫型PAVMs,仍需造影檢查。最近研究表明,在診斷肺動靜脈瘺方面,胸部CT在敏感性和特異性方面不亞於肺動脈造影。隨著64排螺旋CT在臨床的普及,其在PAVMs診斷中的優勢及發生漏診的可能原因也得到了進一步研究,王克等的研究表明,如果掃描技術和後處理技術套用不當,也會造成誤診和漏診的發生。
磁共振是一種無創的檢查方法,特別適合於使用含碘造影劑禁忌證、不能做增強CT檢查者。但由於含氣肺組織的影響,對主要位於肺外圍部分的PAVMs診斷受限,個別較大瘤囊可表現為無至低信號的囊狀結構(血液流空效應)。有研究表明自旋迴波脈衝序列,梯度回波脈衝序列對PAVMs診斷的敏感性和特異性均不高,相位對比電影序列是核磁共振技術中診斷PAVMs最準確的方法,可明確病變部位、形態、累及的範圍。近年來對對增強磁共振血管成像(CEMRA)套用更增加了診斷的準確性,對觀察血管構築,區分複雜型和簡單型有重要價值,但對診斷瀰漫型價值有限。Khail等研究表明此方法對發現有臨床意義的PAVMs的敏感性和特異性都很高。
肺動脈造影的時間及空間解析度高,可明確PAVMs的部位,形態、累及的範圍及程度,特別是進行超選擇動脈造影時敏感性可達100%,目前仍是診斷PAVMS的金標準。
造影方法分為選擇性或非選擇性。一般先進行選擇性主肺動脈造影,正位投照。投照時相包括兩肺整個肺野,以免遺漏病變。其後,視情況決定選擇性肺動脈造影。造影主要表現:單純型囊狀PAVMs可見瘤囊隨肺動脈的充盈顯影,引流肺靜脈顯影早於正常肺靜脈,供血動脈及引流靜脈均為一支,並見不同程度的迂曲、擴張。較大的瘤囊可見對比劑排空延遲。複雜型囊狀PAVMs可見兩支或多支供血動脈及引流靜脈,瘤囊內可見分隔,對比劑排空明顯延遲。瀰漫型PAVMs表現為多發葡萄串樣小血池充盈,有時難以觀察到與肺小靜脈支的連通,但DSA或電影連續攝影觀察,相應區域無毛細血管前期(實質充盈期),或病變部位肺靜脈提前顯影,有助於診斷。
近10多年來數字減影血管造影已取代了普通心血管造影,但目前還沒有關於這兩種技術的系統對比研究。因為血管造影是有創性的檢查,故主要用於PAVMs治療前確診和作為介入治療的組成部分,而治療後隨訪時一般不用此方法。
最近研究表明,聯合套用後前位胸片和超聲造影可獲得100%的敏感性和陰性預測值,因而,合理的檢查程式為聯合套用對比超聲和後前位胸片,如果二者皆陽性,可行CT檢查,如果可行栓塞治療,則在治療過程中行肺動脈造影。思維程式的最佳化問題。
治療措施
傳統認為不是所有的PAVMs都需要治療。只有那些病變進行性增大的、發生了矛盾性栓塞的以及有症狀的低氧血症患者才有必要治療。但近來的研究發現很多無症狀的或病變很少的患者也可發生嚴重的神經系統併發症(如中風、腦膿腫等),因此White等人主張所有供血動脈直徑≥3mm的PAVMs患者不論有無症狀都應治療。治療目的改善缺氧症狀,預防中風、腦膿腫、咯血等嚴重併發症的出現。目前治療PAVMs的方法有外科手術,經導管栓塞治療、藥物治療,現將各種方法綜述如下:
外科手術是根治性治療措施。其手術適應證包括:有症狀、分流量大和伴有HHT的單發孤立性PAVMs,不管有無併發症者;多發性PAVMs,病變局限於一個肺葉或一側肺臟者;直徑A2。雜音:心尖部及L2可聞及3/6SM。血常規:白細胞:2.04/L,重度貧血。
X:右肺中葉及下葉後基底段可見囊狀團塊影,邊緣光滑,多分葉,與肺血管關係密切,余肺未見實變。心胸比:0.65。考慮為多發肺動靜脈瘺。02年2月21日行右下肺動靜脈瘺封堵術。
封堵過程:局麻下穿刺右股靜脈,送入12F輸送鞘管入右下肺動脈乾,選擇直徑30mm國產先健公司ASD封堵器封堵右下肺動脈近段、巨大瘤囊動脈端,股動脈血氧飽和度立即由術前65%上升至93%。然後行肺動脈造影,可見右上肺前段仍有一肺動脈分支受累,可見瘤囊顯影,近端肺動脈直徑約13mm,遂將9F輸送鞘置於該分支近端,瘤囊近端,選擇直徑14/12國產先健公司PDA封堵器封堵該分支遠端,股動脈血氧飽和度再次上升至97%;重複肺動脈造影,未見該瘤囊顯影。術中經過順利,患者未訴不適,共用碘比樂150ml.
血氧飽和度:封堵前:65%;封堵後97%。
肺動脈壓力:封堵前:30/10(18);封堵後37/17(25)。
二張歡:女,16歲,自幼心臟雜音,紫紺。於1997-2002年間先後三次行肺動脈瘺栓塞術,02年元月以AGA16/14mm封堵器封堵右肺動脈(右下肺動脈乾),封堵後血氧飽和度為84%。今發作性胸悶氣短症狀加重,遂再次求治。於2004年4再次以AGA26mmASD封堵器封堵。
局麻下行肺動脈造影+右肺動脈瘺栓塞術。經雙側右股靜脈穿刺,送入6F鞘,經右側股靜脈行造影,造影示右肺動脈廣泛動靜脈瘺。後經左側股靜脈送入6F豬尾管造影后,選用26mmASD封堵器。試封堵中無不良反應,肺動脈壓無升高。
肺動脈壓:前20/16(19),栓塞後35/10(22)
肺動脈血氧:栓塞前75.6%;栓塞後90%。