簡介
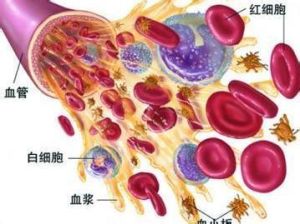 障礙性貧血
障礙性貧血治療
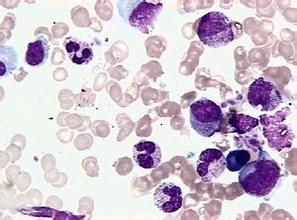 障礙性貧血
障礙性貧血(一)支持療法凡有可能引起骨髓損害的物質均應設法去除,禁用一切對骨髓有抑制作用的藥物。積極做好個人衛生和護理工作。對粒細胞缺乏者宜保護性隔離,積極預防感染。輸血要掌握指征,準備做骨髓移植者,移植前輸血會直接影響其成功率,尤其不能輸家族成員的血。一般以輸入濃縮紅細胞為妥。嚴重出血者宜輸入濃縮血小板,採用單產或HLA相合的血小板輸注可提高療效。反覆輸血者宜套用去鐵胺排鐵治療。
(二)雄激素為治療慢性再障首選藥物。常用雄激素有四類:①17α-烷基雄激素類:如司坦唑(康力龍,Stanozolone)、甲氧雄烯醇酮、羥甲烯龍(oxymetholonE)、氟甲睪酮(fluoxymetholonE)、大力補(Dianabol)等;②睪丸素酯類:如丙酸睪酮、庚酸睪酮、環戊丙酸睪酮、十一酸睪酮(安雄)和混合睪酮酯(丙酸睪酮、戊酸睪酮和十一烷酸睪酮)又稱"巧理寶";③非17α-烷基雄激素類:如苯丙酸諾龍和葵酸諾龍等;④中間活性代謝產物:如本膽脘醇酮和達那唑(Danazol)等。睪酮進入體內,在腎組織和巨噬細胞內,通過5α-降解酶的作用,形成活力更強的5α-雙氫睪酮,促使腎臟產生紅細胞生成素,巨噬細胞產生粒巨噬細胞集落刺激因子;在肝臟和腎髓質記憶體在5β-降解酶,使睪酮降解為5β-雙氫睪酮和本膽烷醇酮,後兩者對造血幹細胞具有直接刺激作用,促使其增殖和分化。因此雄激素必須在一定量殘存的造血幹細胞基礎上,才能發揮作用,急性、嚴重再障常無效。慢性再障有一定的療效,但用藥劑量要大,持續時間要長。丙酸睪丸酮50~100Mg/d肌肉注射,康力龍6~12mg/D口服,安雄120~160mg/d口服,巧理寶250mG每周二次肌肉注射,療程至少6個月以上。國內報告的有效率為34.9%~81%,緩解率19%~54%。紅系療效較好,一般治後一個月網織紅細胞開始上升,隨後血紅蛋白上升,2個月後白細胞開始上升,但血小板多難以恢復。部分患者對雄激素有依賴性,停藥後復發率達25%~50%。復發後再用藥,仍可有效。丙酸睪酮的男性化副作用較大,出現痤瘡、毛髮增多、聲音變粗、女性閉經、兒童骨成熟加速及骨骺早期融合,且有一定程度的水鈉瀦留。丙睪肌注多次後局部常發生硬塊,宜多處輪換注射。17α烷基類雄激素男性化副反應較丙睪為輕,但肝臟毒性反應顯著大於丙睪,多數病人服藥後出現谷丙轉氨酶升高,嚴重者發生肝內膽汁瘀積性黃疸,少數甚至出現肝血管肉瘤和肝癌,但停藥後可消散。
(三)骨髓移植是治療幹細胞缺陷引起再障的最佳方法,且能達到根治的目的。一旦確診嚴重型或極嚴重型再障,年齡<20歲,有HLA配型相符供者,在有條件的醫院應首選異基因骨髓移植,移植後長期無病存活率可達60%~80%,但移植需儘早進行,因初診者常輸紅細胞和血小板,這樣易使受者對獻血員次要組織相容性抗原致敏,導致移植排斥發生率升高。對確診後未輸過血或輸血次數很少者,預處理方案可用環磷醯胺每天50mg/kG連續靜滴4天。國內已開始套用異基因骨髓移植治療嚴重再障,並已有獲得成功報導。凡移植成功者則可望治癒。胎肝細胞懸液輸注治療再障國內已廣泛開展,有認為可促進或輔助造血功能恢復,其確切的療效和機理尚有待於進一步研究。
(四)免疫抑制劑適用於年齡大於40歲或無合適供髓者的嚴重型再障。最常用的是抗胸腺球蛋白(ATG)和抗淋巴細胞球蛋白(ALG)。其機理主要可能通過去除抑制性T淋巴細胞對骨髓造血的抑制,也有認為尚有免疫刺激作用,通過產生較多造血調節因子促進幹細胞增殖,此外可能對造血幹細胞本身還有直接刺激作用。劑量因來源不同而異,馬ALG10~15mg/(kg?d),兔ATG2.5~4.0mg/(kg?D),共5天,用生理鹽水稀釋後,先皮試,然後緩慢從大靜脈內滴注,如無反應,則全量在8~12小時內滴完;同時靜滴氫化考的松,1/2劑量在ALG/ATG滴注前,另1/2在滴注後用。患者最好給予保護性隔離。為預防血清病,宜在第5天后口服強的松1mg/(kg?d),第15天后減半,到第30天停用。不宜套用大劑量腎上腺皮質激素,以免引起股骨頭無菌性壞死。療效要1個月以後,有的要3個月以後才開始出現。嚴重型再障的有效率可達40%~70%,有效者50%可獲長期生存。不良反應有發熱、寒顫、皮疹等過敏反應,以及中性粒細胞和血小板減少引起感染和出血,滴注靜脈可發生靜脈炎,血清病在治療後7~10天出現。環孢菌素A(CSA)也是治療嚴重型再障的常用藥物,由於套用方便、安全,因此比ALG/ATG更常用,其機理可能選擇性作用於T淋巴細胞亞群,抑制T抑制細胞的激活和增殖,抑制產生IL-2和γ干擾素。劑量為10~12mg/(kg?d),多數病例需要長期維持治療,維持量2~5mg/(kg?d)。對嚴重再障有效率也可達50%~60%,出現療效時間也需要1~2月以上。不良反應有肝腎毒性作用、多毛、牙齦腫脹、肌肉震顫,為安全用藥宜採用血藥濃度監測,安全有效血濃度範圍為300~500ng/ml。現代免疫抑制劑治療嚴重型再障療效已可和骨髓移植相近,但前者不能根治,且有遠期併發症,如出現克隆性疾病,包括MDS、PNH和白血病等。
(五)中醫藥治宜補腎為本,兼益氣活血。常用中藥為鹿角膠、仙茅、仙靈脾、黃芪、生熟地、首烏、當歸、蓯蓉、巴戟、補骨脂、菟絲子、枸杞子、阿膠等。國內治療慢性再障常用雄激素合併中醫補腎法治療。
(六)造血細胞因子和聯合治療再障是造血幹細胞疾病引起的貧血,內源性血漿EPO水平均在500u/L以上,採用重組人EPO治療再障必需大劑量才可能有效,一般劑量是不會取得任何效果。重組人集落刺激因子包括G-CSF、GM-CSF或IL-3治療再障對提高中性粒細胞,減少感染可能有一定效果,但對改善貧血和血小板減少效果不佳,除非大劑量套用。但造血細胞因子價格昂貴,因此目前僅限於重型再障免疫抑制劑治療時的輔助用藥,如套用ALG/ATG治療重型再障,常因出現嚴重粒細胞缺乏而並發感染,導致早期死亡。若該時合併套用rHG-CSF可改善早期粒缺,降低病死率。聯合治療可提高對重型再障治療效果,包括ALG/ATG和CSA聯合治療,CSA和雄激素聯合治療等,歐洲血液和骨髓移植組採用ALG、CSA、甲基強的松龍和rhG-CSF聯合治療,對重型再障有效率已提高到82%。
病因學
再障的發病可能和下列因素有關:(一)藥物藥物是最常見的發病因素。藥物性再障有兩種類型:①和劑量有關,系藥物毒性作用,達到一定劑量就會引起骨髓抑制,一般是可逆的,如各種抗腫瘤藥。細胞周期特異性藥物如阿糖胞苷和甲氨蝶呤等主要作用於容易分裂的較成熟的多能幹細胞,因此發生全血細胞減少時,骨髓仍保留一定量的多能幹細胞,停藥後再障可以恢復;白消安和亞硝脲類不僅作用於進入增殖周期的幹細胞,並且也作用於非增殖周期的幹細胞,因此常導致長期骨髓抑制難以恢復。此外,苯妥英鈉、吩噻嗪、硫尿嘧啶及氯黴素等也可以引起與劑量有關的骨髓抑制。②和劑量關係不大,僅個別患者發生造血障礙,多系藥物的過敏反應,常導致持續性再障。這類藥物種類繁多,常見的有氯(合)黴素、有機砷、阿的平、三甲雙酮、保泰松、金製劑、氨基比林、吡羅昔康(炎痛喜康)、磺胺、甲碸黴素、卡比馬唑(甲亢平)、甲巰咪唑(他巴唑)、氯磺丙脲等。藥物性再障最常見是由氯黴素引起的。據國內調查,半年內有服用氯黴素者發生再障的危險性為對照組的33倍,並且有劑量-反應關係。氯黴素可發生上述二種類型的藥物性再障,氯(合)黴素的化學結構含有一個硝基苯環,其骨髓毒性作用與亞硝基-氯黴素有關,它可抑制骨髓細胞內線粒體DNA聚合酶,導致DNA及蛋白質合成減少,也可抑制血紅素的合成,幼紅細胞漿內可出現空泡及鐵粒幼細胞增多。這種抑制作用是可逆性的,一旦藥物停用,血象即恢復。氯黴素也可引起和劑量關係不大的過敏反應,引起骨髓抑制多發生於服用氯黴素後數周或數月,也可在治療過程中突然發生。其機理可能是通過自身免疫直接抑制造血幹細胞或直接損傷幹細胞的染色體所致。這類作用往往是不可逆的,即使藥物停用。凡幹細胞有遺傳性缺陷者,對氯黴素的敏感性增加。
(二)化學毒物苯及其衍化物和再障關係已為許多實驗研究所肯定,苯進入人體易固定於富含脂肪的組織,慢性苯中毒時苯主要固定於骨髓,苯的骨髓毒性作用是其代謝產物所致,後者可作用於造血祖細胞,抑制其DNA和RNA的合成,並能損害染色體。改革開放以來,鄉鎮企業興起,由於不注意勞動保護,苯中毒致再障發病率有所上升。苯中毒再障可呈慢性型,也可呈急性嚴重型,以後者居多。
(三)電離輻射X線、γ線或中子可穿過或進入細胞直接損害造血幹細胞和骨髓微環境。長期超允許量放射線照射(如放射源事故)可致再障。
(四)病毒感染病毒性肝炎和再障的關係已較肯定,稱為病毒性肝炎相關性再障,是病毒性肝炎最嚴重的併發症之一,發生率不到1.0%,占再障患者的3.2%。引起再障的肝炎類型至今尚未肯定,約80%由非甲非B型肝炎引起,可能為C型肝炎,其餘由B型肝炎引起。肝炎相關性再障臨床上有兩種類型:急性型居多數,起病急,肝炎和再障發病間期平均10周左右,肝炎已處於恢復期,但再障病情重,生存期短,發病年齡輕,大多系在非甲非B型肝炎基礎上發病;慢性型屬少數,大多在慢性B型肝炎基礎上發病,病情輕,肝炎和再障發病間期長,生存期也長。其發病機理仍不清楚。肝炎病毒對造血幹細胞有直接抑制作用,還可致染色體畸變,並可通過病毒介導的自身免疫異常。病毒感染尚可破壞骨髓微循環。
(五)免疫因素再障可繼發於胸腺瘤、系統性紅斑狼瘡和類風濕性關節炎等,患者血清中可找到抑制造血幹細胞的抗體。部分原因不明的再障可能也存在免疫因素。
(六)遺傳因素Fanconi貧血系常染色體隱性遺傳性疾病,有家族性。貧血多發現在5~10歲,多數病例伴有先天性畸形,特別是骨骼系統,如拇指短小或缺如、多指、橈骨縮短、體格矮小、小頭、眼裂小、斜視、耳聾、腎畸形及心血管畸形等,皮膚色素沉著也很常見。本病HBF常增高,染色體異常發生率高,DNA修復機制有缺陷,因此惡性腫瘤,特別是白血病的發生率顯著增高。10%患兒雙親有近親婚配史。
(七)陣發性睡眠性血紅蛋白尿(PNH)PNH和再障關係相當密切,20%~30%FNH可伴有再障,15%再障可發生顯性PNH,兩者都是造血幹細胞的疾病。明確地從再障轉為PNH,而再障表現已不明顯;或明確地從PNH轉為再障,而PNH表現已不明顯;或PNH伴再障及再障伴PNH紅細胞,都可稱謂再障-PNH綜合徵。
(八)其他因素罕有病例報告,再障在妊娠期發病,分娩或人工流產後緩解,第二次妊娠時再發,但多數學者認為可能是巧合。此外,再障尚可繼發於慢性腎功能衰竭、嚴重的甲狀腺或前(腺)腦垂體功能減退症等。
症狀體徵
分先天性和獲得性兩大類,以獲得性居絕大多數。先天性再障甚罕見,其主要類型為Fanconi貧血。獲得性再障可分原發和繼發性兩型,前者系原因不明者,約占獲得性再障的50%;又可按臨床表現、血象和骨髓象不同綜合分型,分為急性和慢性兩型;國外按嚴重度劃分出嚴重型再障,後者劃分標準須血象具備以下三項中之二項:①中性粒細胞絕對值<500/mm3,②血小板數<2萬/mm3,③網織紅細胞(紅細胞壓積糾正值)<1%;骨髓細胞增生程度低於正常的25%,如<50%,則造血細胞<30%。其中中性粒細胞絕對值<200/mm3者稱極重型再障。1987年第四屆全國再障學術會議上將急性再障稱重型再障I型,慢性再障後期發生急變者稱重型再障Ⅱ型。(一)急性型再障 起病急,進展迅速,常以出血和感染髮熱為首起及主要表現。病初貧血常不明顯,但隨著病程發展,呈進行性進展。幾乎均有出血傾向,60%以上有內臟出血,主要表現為消化道出血、血尿、眼底出血(常伴有視力障礙)和顱內出血。皮膚、黏膜出血廣泛而嚴重,且不易控制。病程中幾乎均有發熱,系感染所致,常在口咽部和肛門周圍發生壞死性潰瘍,從而導致敗血症。肺炎也很常見。感染和出血互為因果,使病情日益惡化,如僅採用一般性治療多數在一年內死亡。
(二)慢性型再障 起病緩慢,以分血為首起和主要表現;出血多限於皮膚黏膜,且不嚴重;可並發感染,但常以呼吸道為主,容易控制。若治療得當,堅持不懈,不少患者可獲得長期緩解以至痊癒,但也有部分病人遷延多年不愈,甚至病程長達數十年,少數到後期出現急性再障的臨床表現,稱為慢性再障急變型。
預防
一、防止濫用對造血系統有損害的藥物,特別是氯黴素、保泰松等一類藥物,必須使用時,加強觀察血象,及時採取適當措施。
二、長期接觸能引起本病的化學、物理因素的人員,應嚴格執行防護措施,嚴格遵守操作規程,防止有害的化學和放射性物質污染周圍環境。
預防常識:
再生障礙性貧血,可由於化學、物理或生物因素對骨髓毒性作用所引起。因此在有關的工農業生產中,要嚴格執行勞動防護措施,嚴格遵守操作規程,防止有害的化學和放射性物質污染周圍環境。本病患者機體抵抗力較低,因此要重視個人和環境的清潔衛生。一旦感染髮生,應及早到醫院診治。輸血對本病是一種支援手段,但不應濫用。為防止血色病,一般血紅蛋白在6g/L以上不宜輸血。目前對慢性再生障礙性貧血主要用雄性激素治療,中藥對部分病人有效,對急重症再障可行異體骨髓移植或用於抗淋巴細胞球蛋白。
注意事項
1、注意生活規律,保持心情舒暢,勞逸結合,加強鍛鍊,養成良好的衛生習慣,早晚刷牙,少到或不到公共場所,以免感染疾病;禁劇烈運動,防止意外情況導致出血。2、對於急性型及重型者須絕對臥床休息;慢性再障患者如無自發性出血,血色素已升到能耐受一般活動者,可參加一定的體力活動而不必過分地限制,如可參加家庭輕體力勞動,同時可適當地參加一般的體育活動如散步、太極拳、保健按摩,以強壯身體,使造血功能恢復。{再生障礙性貧血的注意事項}
3、按醫囑進食:忌辛辣刺激性食物(生蔥、生薑、生蒜、辣椒等)、海鮮羊肉狗肉等熱性食物,忌菸酒,忌生冷油膩;給予高蛋白、高維生素、易消化食物,如瘦肉、蛋類、乳類、雞肉、排骨湯、動物肝臟、新鮮蔬菜及水果,多食大棗、桂園、花生、核桃、藕等以生血止血;對於有出血傾向者給予無渣半流質飲食,少進食帶刺、骨的食物,以防因刺傷而引起出血和感染。{再生障礙性貧血的注意事項}
4、注意患者的出血傾向,如皮膚黏膜出血、鼻衄、牙齦出血、眼底出血等,給予對症和止血處理;發生胃腸道大出血或存在顱內出血的危險時,應立即報告醫生,同時準備好各種搶救藥物及用物,協助搶救。
5、保持病室清潔,每天空氣消毒,白細胞下降者應行保護性隔離以減少感染。
6、注意口腔清潔及肛門衛生。堅持飯後、睡前漱口,防止口咽部潰瘍,常用漱口液有生理鹽水、複方硼酸溶液、1%雙氧水、碳酸氫鈉溶液等;堅持便後用1/5000高錳酸鉀溶液坐浴,防止肛門周圍發生壞死性潰瘍而導致敗血症。
7、皮膚、黏膜廣泛出血者注意保持皮膚、黏膜的完整性以防止感染,高熱大汗者及時更衣,避免受涼感冒。
鑑別診斷
診斷
(1)全血細胞減少,網織紅細胞<0.01,淋巴細胞比例增高。血象滿足至少下列2項:(1)血紅蛋白<100g/l(2)血小板<50×10^9/L(3)中性粒細胞<1.5×10^9/L。(2)一般無肝脾腫大。(3)骨髓多部位增生減低(<正常的50%)或重度減低(<正常的25%),造血細胞減少,非造血細胞比例增高,骨髓小粒空虛,骨髓活檢示造血組織減少。(4)除外引起全血細胞減少的其它疾病,如急性造血功能停滯、骨髓增生異常綜合症、范科尼貧血、PNH、Evans綜合徵、免疫相關性全血細胞減少、骨髓纖維化、毛細胞白血病、低增生性白血病、間變性T細胞淋巴瘤等。
鑑別診斷
(1)血清維生素B12、葉酸水平及鐵含量測定
嚴重的鐵缺乏、維生素B12和葉酸不足,亦可引起全血細胞減少。若存在鐵、維生素B12和葉酸缺乏,須糾正之後在評價造血功能。
(2)自身抗體篩選
B細胞功能亢進的疾病,如系統性紅斑狼瘡、免疫相關性血細胞減少症,可以產生抗造血的自身抗體,引發造血功能衰竭。系統性紅斑狼瘡還可引起骨髓纖維化、疑為系統性紅斑狼瘡等結締組織病應檢查抗核抗體及抗DNA抗體等。免疫相關性血細胞減少症應檢測骨髓細胞膜上自身抗體。
(3)溶血性疾病
最主要的是陣發性睡眠性血紅蛋白尿症(PNH),典型PNH有血紅蛋白尿發作,易鑑別。不典型者無血紅蛋白尿發作,全血細胞減少,骨髓可增生減低,易誤診為再障。但該病主要特點是:動態隨訪,終能發現PNH造血克隆。流式細胞術檢測CD55、CD59是診斷PNH的敏感方法。部分再障患者會出現少量PNH克隆,可以保持不變、減少、消失或是增加。這是PNH患者的早期表現,還是提示該再障患者易轉化為AA-PNH綜合徵,尚不清楚。但若這些患者有實驗室或臨床證據表明存在溶血,應診斷為PNH。尿含鐵血黃素試驗陽性提示存在長期血管內溶血,有利於PNH的診斷。網織紅細胞計數、間接膽紅素水平、轉氨酶和乳酸脫氫酶定量對於評價PNH的溶血有一定作用。
Evans綜合徵和免疫相關性全血細胞減少症。前者可測及外周成熟血細胞自身抗體,後者可測及骨髓未成熟血細胞自身抗體。這兩類血細胞減少患者Th2細胞比例增高、CD5+的B淋巴細胞比例增高、血清IL-4水平增高,對腎上腺皮質激素和/或大劑量靜脈丙種球蛋白治療反應好。
(4)骨髓增生異常綜合徵(MDS)
MDS,尤其低增生性者,亦有全血細胞減少,網織紅細胞有時不高甚至降低,骨髓低增生,易與再障混淆,但MDS有以下特點:粒細胞和巨核細胞病態造血,血片或骨髓塗片中出現異常核分裂象。MDS可伴骨髓纖維化,骨髓活檢示網硬蛋白增加,而再障不會伴骨髓纖維化。骨髓活檢中灶性的髓系未成熟前體細胞異常定位非MDS所特有,因再障患者骨髓的再生灶時也可以出現不成熟粒細胞。紅系病態造血再障中亦可見,不做為與MDS鑑別的依據。
骨髓細胞遺傳學檢查對於再障與MDS鑑別很重要,若因骨髓增生低下,細胞數少,難以獲得足夠的中期分裂象細胞,可以採用FISH。CEP7、7q31、CEP8、20q、CEPY和p53。值得注意的是,那么這是真正的再障還是MDS,有待探討。但是2008年WHO的MDS診斷分型標準中認為,單有-Y,+8或20q-者的難治性血細胞減少者,若無明確病態造血,不能依遺傳學異常而診斷為MDS。對此的解釋是,這些患者常常對免疫抑制治療有較好效果,那么這些患者是不是診斷為再障更合適。
在兒童再障中出現遺傳學異常,尤其是+7常提示為MDS。在疾病的過程中可能會出現異常細胞遺傳學克隆。
(5)低增生性白血病
特別是白細胞減少的白血病和低增生性白血病,早期肝、脾、淋巴結不腫大,外周全血細胞減少,易與再障混淆。仔細觀察血象及多部位骨髓,可發現原始粒、單、或原(幼)淋巴細胞明顯增多。部分急性早幼粒細胞白血病、伴t(8;21)易位的急性粒細胞白血病M2可有全血細胞減少,骨髓分類多可鑑別之。
(6)毛細胞白血病
會出現全血細胞減少伴單核細胞減少,骨髓常乾抽。骨髓活檢可見到毛細胞呈“煎蛋”樣浸潤骨髓間質、網硬蛋白增加。免疫表型顯示CD20+,CD11c+,CD25+,FMC7+,CD103+,CD5-,CD10-和CD23-腫瘤細胞。脾腫大常見,毛細胞白血病者經切脾和干擾素治療能有很好效果。
(7)轉移性腫瘤
腫瘤骨轉移可以導致全血細胞減少和骨髓增生減低,但骨髓塗片和活檢中能見到轉移的腫瘤細胞,有時血片可以見到不成熟造血細胞。骨髓淋巴細胞免疫表型、基因重排可以用於再障增多的淋巴細胞與淋巴瘤骨浸潤的鑑別。腫瘤骨轉移者骨髓活檢常伴骨髓纖維化。詳細病史和體格檢查能提供腫瘤的一些跡象,並指導相關的腫瘤檢查,利於尋找原發病灶和指導治療。
(8)骨髓纖維化
常出現全血細胞減少和骨髓增生減低,骨髓常乾抽。骨髓活檢見到網硬蛋白增加和纖維細胞。骨髓纖維化因出現髓外造血,血塗片可以見到不成熟造血細胞,伴脾腫大,常為巨脾。無脾腫大的骨髓纖維化繼發於惡性腫瘤可能性大。
(9)急性造血功能停滯
常在溶血性貧血、接觸某些危險因素或感染髮熱的患者中發生,全血細胞尤其是紅細胞驟然下降,網織紅細胞可降至零,骨髓三系減少,與SAA-I型相似。但骨髓塗片尾部可見巨大原始紅細胞,在充足支持治療下呈自限性,約經1月可自然恢復。
(10)低增生性急性淋巴細胞白血病
占兒童急淋的1%-2%。通常在兒童骨髓衰竭後的3-9個月出現急淋,中性粒細胞減少較血小板減少更嚴重。有報導兒童重型再障者轉化為急淋,這些患者的骨髓衰竭是再障,還是急淋的白血病前期,有待討論。完善形態學、細胞遺傳學和白血病免疫表型有助於確定診斷。
(11)先天性再障
范科尼貧血(FA)常稱為先天性再障,是一種遺傳性幹細胞質異常性疾病。表現為一系/兩系或全血細胞減少、可伴發育異常(皮膚色素沉著、骨骼畸形、器官發育不全等)、高風險發展為MDS、AL及其它各類腫瘤性疾病;實驗室檢查可發現“范科尼基因”、細胞染色體受絲裂酶素C或DBA試劑作用後極易斷裂。因為較大年齡的范科尼貧血病例報導,其篩查的上限年齡尚難確定。先天性角化不良可以通過典型臨床特徵和基因突變加以鑑別。
(12)感染
肝炎後再障多發生在肝炎後2-3月的恢復期,且已知的肝炎病原學檢查多為陰性。病毒感染,如EBV、CMV很少引起造血功能衰竭,但慢性活動性EBV感染致淋巴細胞增殖性疾病者,會發生造血功能衰竭。微小病毒B19可導致紅細胞造血障礙但不會引發再障。
分支桿菌,尤其是非典型分支桿菌感染會出現全血細胞減少和骨髓增生低下。骨髓檢查還可發現肉芽腫、纖維化、骨髓壞死等。嗜酸性壞死常見於非典型結核桿菌感染,結核分枝桿菌感染少有嗜酸性壞死和肉芽腫。疑為結核者,應送骨髓液行分支桿菌培養。
上文提及的急性造血功能停滯亦常常是呼吸道病毒或細菌感染所誘發。
(13)嚴重營養不良
神經性厭食或是長時間飢餓可能與全血細胞減少有關。由於脂肪細胞和造血細胞減少骨髓塗片顯示細胞少並且形成膠狀,基質HE染色顯示為淡粉色。在再障中可見不同程度的脂肪變性,尤其是早期演變階段。
疾病治療
“生物細胞再生療法”治療是生物醫學新技術,是一種綜合、整體、系統的全新療法,是把來源於臍帶血“臍血”、外周血跟脊髓中的造血生長因子,具有自我更新增殖能力並能分化成各種血細胞(紅細胞、白細胞和血小板)的前體細胞,通過實驗室培養擴增到足夠數量和質量採取微創介入、穿刺、局部動脈注射等方式,快速到達病灶部位,以激活機體造血細胞或基質細胞再生,發揮骨髓造血細胞功能。增強機體細胞免疫能力,恢復完整的免疫系統,有效抵制疾病再次復發。
現代病理學研究表明,“生物細胞再生療法”具有調理氣血,改善造血微環境,消除造血細胞和造血微環境功能障礙,補腎生髓生血作用,明顯提高了再生障礙性貧血的療效,臨床有效率在95%以上,已達國際領先水平。