基本簡介
【英文名稱】 Doxorubicin 【其他名稱】 14-羥基柔紅黴素,14-羥基正定黴素,阿得里亞黴素,阿黴素-威力,多索柔比星,羥基紅比黴素,羥基柔紅黴素,威力啊黴素,亞德里亞黴素,亞法里亞黴素,阿黴素,14-羥正定黴素,14-羥柔紅黴素,Adri
【適應證】該品抗瘤譜較廣,適用於急性白血病(淋巴細胞性和粒細胞性)、惡性淋巴瘤、乳腺癌、支氣管肺癌(未分化小細胞性和非小細胞性)、卵巢癌、軟組織肉瘤、成骨肉瘤、橫紋肌肉瘤、尤文肉瘤。腎母細胞瘤、神經母細胞瘤、膀胱癌、甲狀腺癌、前列腺癌、頭頸部鱗癌、睪丸癌、胃癌、肝癌等。
【藥品分類】抗腫瘤藥-細胞毒類藥物-作用於DNA化學結構的藥物
【劑量與用法】40mg~60mg/m2,3周1次。
或每日20mg/m2連續3日,間隔3周再給藥。
目前認為總量不宜超過450mg~550mg/m2,以免發生嚴重心臟毒性。
【副作用】
1 骨髓造血功能,表現為血小板及白細胞減少。
2 心臟毒性,嚴重時可出現心力衰竭。
3 可見到噁心、嘔吐、口腔炎、脫髮、高熱、靜脈炎及皮膚色素沉著等。
4 少數患者有發熱、出血性紅斑及肝功能損害。
成分
【化學名稱】 (2R,4S)-4-(3-Amino-2,3,6-trideoxy-α-L-lyxo-hexopyranosyloxy)-2-hydroxyacetyl-1,2,3,4-tetrahydro-2,5,12-trihydroxy-7-methoxynaphthacene-6,11-dione
【CA登記號】[23214-92-8]
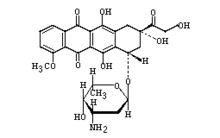 結 構 式
結 構 式【結 構 式】
【分 子 式】C27H29NO11
【分 子 量】543.52
【水 溶 性】阿黴素純品可溶於水
【收錄藥典】JP14
【性狀】為桔紅色的凍乾粉劑。每瓶含10mg鹽酸多柔比星及適量乳糖和對羥基苯甲酸甲酯。
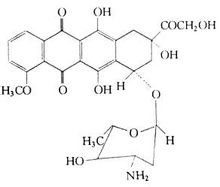 阿黴素
阿黴素【作用與用途】阿黴素是一種抗腫瘤抗生素,可抑制RNA 和DNA的合成,對RNA的抑制作用最強,抗瘤譜較廣,對多種腫瘤均有作用,屬周期非特異性藥物,對各種生長周期的腫瘤細胞都有殺滅作用。主要適用於急性白血病,對急性淋巴細胞白血病及粒細胞白血病均有效,一般作為第二線藥物,即在首選藥物耐藥時可考慮套用此藥。惡性淋巴瘤,可作為交替使用的首選藥物。乳腺癌、肉瘤、肺癌、膀胱癌等其他各種癌症都有一定療效,多與其他抗癌藥聯合使用。主要的毒性反應有,白細胞和血小板減少,約60%~80%的病人可發生;100%的病人有不同程度的毛髮脫落,停藥後可以恢復生長;心臟毒性,
表現為心律失常,ST-T改變,多出現在停藥後的1~6個月,及早套用維生素B6和輔酶Q10可減低其對心臟的毒性;噁心、食慾減退;藥物溢出血管外可引起組織潰瘍及壞死。另外,用藥後尿液可出現紅色。
該品為廣譜抗腫瘤藥,對機體可產生廣泛的生物化學效應,具有強烈的細胞毒性作用。其作用機理主要是該品嵌入DNA而抑制核酸的合成。臨床上用於治療急性淋巴細胞白血病、急性粒細胞性白血病、霍奇金和非霍奇金淋巴瘤、乳腺癌、肺癌、卵巢癌、軟組織肉瘤、成骨肉瘤、橫紋肌肉瘤、腎母細胞瘤、神經母細胞瘤、膀胱瘤、甲狀腺瘤、絨毛膜上皮癌、前列腺癌、睪丸癌、胃癌、肝癌等。
套用
【藥物相互作用】
1.各種骨髓抑制劑特別是亞硝脲類、大劑量環磷醯胺或甲氨蝶呤、絲裂黴素或放射治療,如與該品同用,後者一次量與總劑量均應酌減。
2.該品如與鏈佐星(streptozotocin)同用,後者可延長該品的半衰期,因此前者劑量應予酌減。
3.任何可能導致肝臟損害的藥物如與該品同用,可增加該品的肝毒性;與肝素、頭孢菌素等混合套用易產生沉澱。
4.該品與柔紅黴素呈交叉耐藥性。與甲氨蝶呤、氟尿嘧啶、阿糖胞苷、氮芥、絲裂黴素、博來黴素、環磷醯胺以及亞硝脲類等則不呈交叉耐藥性,且與環磷醯胺、氟尿嘧啶、甲氨蝶呤、順鉑以及亞硝脲類藥物同用,有不同程度的協同作用。
5.用藥期間慎用活病毒疫苗接種。
6.該品可降低肝素抗凝作用。ACD及普卡黴素與該品同用,有可能導致致死性心臟毒性;該品與普萘洛爾合用,可加強抑制線粒體呼吸酶活性,增加心臟毒性。
【給藥說明】
1.與大劑量的環磷醯胺合用,該品的分次和總量應酌減。
2.在進行縱隔或胸腔放療期間禁用該品,以往接受過縱隔放射治療者,阿黴素的每次用量和總劑量亦應酌減。
3.過去曾用過足量柔紅黴素或該品、表柔比星者不能再用該品。
4.該品可用於漿膜腔內給藥和膀胱灌注,但不能用於鞘內注射。
5.嚴防該品漏出血管外。一旦發生,應儘量抽出局部滲藥,局部立即注射50~100mg氫化可的松,或碳酸氫鈉及冷敷。
【用法與用量】臨用前加氯化鈉注射液溶解,濃度一般為2mg/ml。緩慢靜脈或動脈注射。
1.成人常用量:一次50~60mg,每3~4周1次或每周20~30mg,連用3周,停用2~3周后重複。每周分次用藥的心肌毒性、骨髓抑制和胃腸道反應(包括口腔潰瘍)較每3周用藥一次為輕。兒童用量約為成人的一半。總劑量按體表面積不宜超過400mg/m2。膀胱內或胸腔內可每次用30~40mg。
2.聯合化療:①ABVD(阿黴素、博來黴素、長春鹼和達卡巴嗪),主要用於霍奇金淋巴瘤;②CAF(環磷醯胺、該品和氟尿嘧啶),主要用於乳腺癌;③CAOP(環磷醯胺、阿黴素、長春新鹼和潑尼松),主要用於惡性淋巴瘤;④FAM(氟尿嘧啶,該品和絲裂黴素),主要用於胃癌;⑤AC(該品和阿糖胞苷),主要用於成人急性髓細胞性白血病;⑥AOP(該品、長春新鹼和潑尼松),主要用於淋巴母細胞型急性白血病的誘導緩解;⑦ACP(該品、環磷醯胺和順鉑),主要用於卵巢癌和支氣管肺癌以及頭頸部癌、膀胱癌等;⑧CY-VA-DIC(環磷醯胺、長春新鹼、該品和達卡巴嗪),主要用於軟組織肉瘤和成骨肉瘤;⑨MACC(甲氨蝶呤、該品、環磷醯胺和環己亞硝脲),主要用於未分化小細胞型肺癌或肺腺癌。
【製劑與規格】 注射用阿黴素:①10mg;②50mg。
【不良反應】
1.常見脫髮(約見於90%的患者)、骨髓抑制(白細胞約於用藥後10~14日下降至最低點,大多在3周內逐漸恢復至正常水平,貧血和血小板減少較少見)、口腔潰瘍、食慾減退、噁心甚或嘔吐。
2.少數患者注射該品後原先的放射野可出現皮膚發紅或色素沉著。如注射處藥液外溢,可導致紅腫疼痛甚或蜂窩組織炎和局部壞死。
3.白血病和惡性淋巴瘤患者套用該品時,特別是初次用該品者,可因瘤細胞大量破壞引起高尿酸血症,而致關節疼痛或腎功能損害。
4.該品具有心臟毒性,可引起遲發性嚴重心力衰竭,有時可在停藥半年後發生。有心肌損害時可出現心率增快,心律失常,傳導阻滯或噴射性心力衰竭,這些情況偶可突然發生而常規心電圖無異常跡象。心肌毒性和給藥累積量密切相關。總量達450~550mg/m2者,發生率約1%~4%,總量超過550mg/m2者,發生率明顯增加,可達30%。心臟毒性可因聯合套用其他藥物加重,比較新的資料說明高劑量的環磷醯胺和群司珠單抗都有類似作用。
【禁忌證】
1.該品能透過胎盤,有引致流產的可能,因此嚴禁在妊娠初期的3個月內套用。妊娠期婦女用該品後,對胎兒的毒性反應有時可長達數年後才出現。
2.在進行縱隔或胸腔放療期間禁用該品。
3.下列情況應禁用:周圍血象中白細胞低於3500/μl或血小板低於5萬/μl、明顯感染或發熱、惡液質、失水、電解質或酸鹼平衡失調、胃腸道梗阻、明顯黃疽或肝功能損害者,心肺功能失代償患者、水痘或帶狀皰疹患者。
4.對該品過敏者禁用。
注意事項
1.該品在動物中有致癌作用,在人體也有潛在的致突變和致癌作用。該品對動物生殖功能有明顯影響,但在人類,其抑制作用較大白鼠實驗大為減輕。
2.該品的。腎排泄雖較少,但在用藥後1~2日內可出現紅色尿,一般都在2日後消失。腎功能不全者用該品後要警惕高尿酸血症的出現;痛風患者,如套用該品,別嘌醇用量要相應增加。
3.老年患者、2歲以下幼兒和原有心臟病患者要特別慎用。
4.少數患者用藥後可引起黃疸或其他肝功能損害,有肝功能不全者,用量應予酌減。
5.用藥期間需檢查:①用藥前後要測定心臟功能、監測心電圖、超聲心動圖、血清酶學和其他心肌功能試驗;②隨訪檢查周圍血象(每周至少一次)和肝功能試驗;③應經常查看有無口腔潰瘍、腹瀉以及黃疸等情況,應勸病人多飲水以減少高尿酸血症的可能,必要時檢查血清尿酸或腎功能。
6.阿黴素的心臟毒性多出現在停藥後的1~6個月,應及早套用維生素B6和輔酶Q10以減低其對心臟的毒性。
7.在用藥期間應定期複查血象,避免造成骨髓抑制。
物質毒性
| 編號 | 毒性類型 | 測試方法 | 測試對象 | 使用劑量 | 毒性作用 |
|---|---|---|---|---|---|
| 1 | 急性毒性 | 靜脈注射 | 人類 | 15 mg/kg/D | 1.心臟毒性——心肌病包括梗死 2.胃腸道毒性——噁心、嘔吐 3.皮膚和附屬檔案毒性——毛髮變化 |
| 2 | 急性毒性 | 靜脈注射 | 人類 | 400 ug/kg | 1.胃腸道毒性——其他變化 2.血液毒性——白細胞減少 3.皮膚和附屬檔案毒性——毛髮變化 |
| 3 | 急性毒性 | 靜脈注射 | 人類 | 380 mg/kg/31W | 1.心臟毒性——心肌病包括梗死 2.胃腸道毒性——噁心、嘔吐 3.皮膚和附屬檔案毒性——毛髮變化 |
| 4 | 急性毒性 | 未報告 | 成年男性 | 243 ug/kg | 1.心臟毒性——其他變化 2.血管毒性——血壓調節能力下降 |
| 5 | 急性毒性 | 腹腔注射 | 大鼠 | 16 mg/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 6 | 急性毒性 | 靜脈注射 | 大鼠 | 10510 ug/kg | 1.營養和代謝系統毒性——體重下降或體重增加速率下降 |
| 7 | 急性毒性 | 未報告 | 大鼠 | 7 mg/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 8 | 急性毒性 | 口服 | 小鼠 | 570 mg/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 9 | 急性毒性 | 腹腔注射 | 小鼠 | 10700 ug/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 10 | 急性毒性 | 靜脈注射 | 小鼠 | 10 mg/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 11 | 急性毒性 | 氣管 | 小鼠 | 2400 ug/kg | 1.營養和代謝系統毒性——體重下降或體重增加速率下降 |
| 12 | 急性毒性 | 未報告 | 小鼠 | 21900 ug/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 13 | 急性毒性 | 靜脈注射 | 狗 | 2400 ug/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 14 | 急性毒性 | 靜脈注射 | 兔 | 5 mg/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 15 | 急性毒性 | 胸腔注射 | 兔 | 400 ug/kg | 1.心臟毒性——其他變化 2.肺部、胸部或者呼吸毒性——肺間質纖維化、肺病(包括塵肺) 3.肺部、胸部或者呼吸毒性——胸膜增厚 |
| 16 | 急性毒性 | 腸外 | 倉鼠 | 3500 ug/kg | 1.致癌性——有抗腫瘤、抗癌活性 |
| 17 | 急性毒性 | 腹腔注射 | 哺乳動物 | 8500 ug/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 18 | 慢性毒性 | 腹腔注射 | 大鼠 | 15 mg/kg/3W-I | 1.心臟毒性——其他變化 2.血液毒性——血清成分發生變化 (如TP、膽紅素、膽固醇) 3.生化毒性——抑制或誘導磷酸酶 |
| 19 | 慢性毒性 | 腹腔注射 | 大鼠 | 12 mg/kg/7D-I | 1.心臟毒性——傳導速度變化 2.心臟毒性——其他變化 3.生化毒性——抑制或誘導其他酶 |
| 20 | 慢性毒性 | 腹腔注射 | 大鼠 | 21 mg/kg/8W-I | 1.肝毒性——肝功能下降 2.生化毒性——抑制或脫氫酶誘導 |
| 21 | 慢性毒性 | 腹腔注射 | 大鼠 | 24 mg/kg/2W-I | 1.心臟毒性——心電圖發生變化 2.血液毒性——白細胞計數發生變化 3.慢性病相關毒性——死亡 |
| 22 | 慢性毒性 | 皮下注射 | 大鼠 | 24 mg/kg/12W-I | 1.生化毒性——抑制或脫氫酶誘導 2.生化毒性——抑制或誘導磷酸激酶 |
| 23 | 慢性毒性 | 腹腔注射 | 大鼠 | 20 mg/kg/6W-I | 1.心臟毒性——心臟重量發生變化 2.內分泌毒性——其他變化 3.血液毒性——白細胞計數發生變化 |
| 24 | 慢性毒性 | 靜脈注射 | 大鼠 | 12 mg/kg/3W-I | 1.心臟毒性——心肌病包括梗死 2.心臟毒性——心電圖發生變化 3.營養和代謝系統毒性——體重下降或體重增加速率下降 |
| 25 | 慢性毒性 | 靜脈注射 | 大鼠 | 20 mg/kg/10W-I | 1.心臟毒性——心肌病包括梗死 2.慢性病相關毒性——死亡 |
| 26 | 慢性毒性 | 靜脈注射 | 大鼠 | 12 mg/kg/12W-I | 1.心臟毒性脈衝率發生變化 2.腎、輸尿管和膀胱毒性——腎小管發生變化 (包括急性腎功能衰竭,急性腎小管壞死) 3.血液毒性——紅細胞計數發生變化 |
| 27 | 慢性毒性 | 靜脈注射 | 大鼠 | 12 mg/kg/52D-I | 1.心臟毒性——心臟重量發生變化 2.腎、輸尿管和膀胱毒性——膀胱重量發生變化 3.生化毒性——抑制或誘導過氧化氫酶 |
| 28 | 慢性毒性 | 靜脈注射 | 大鼠 | 12 mg/kg/6W-I | 1.心臟毒性——其他變化 2.生化毒性——抑制或誘導磷酸酶 3.生化毒性——抑制或脫氫酶誘導 |
| 29 | 慢性毒性 | 靜脈注射 | 大鼠 | 12500 ug/kg/5D-I | 1.血液毒性——白細胞減少 2.營養和代謝系統毒性——體重下降或體重增加速率下降 |
| 30 | 慢性毒性 | 靜脈注射 | 大鼠 | 7 mg/kg/7W-I | 1.心臟毒性——心肌病包括梗死 2.營養和代謝系統毒性——體重下降或體重增加速率下降 3.慢性病相關毒性——死亡 |
| 31 | 慢性毒性 | 靜脈注射 | 大鼠 | 12 mg/kg/4W-I | 1.心臟毒性——心肌病包括梗死 2.心臟毒性——心電圖發生變化 3.營養和代謝系統毒性——體重下降或體重增加速率下降 |
| 32 | 慢性毒性 | 腹腔注射 | 小鼠 | 10 mg/kg/9D-I | 1.肝毒性——肝功能下降 2.生化毒性——抑制轉氨酶活性、改變了轉氨酶空間結構 3.營養和代謝系統毒性——鈣濃度發生變化 |
| 33 | 慢性毒性 | 皮下注射 | 小鼠 | 27500 ug/kg/5D-I | 1.慢性病相關毒性——死亡 |
| 34 | 慢性毒性 | 靜脈注射 | 小鼠 | 22600 ug/kg/2D-I | 1.慢性病相關毒性——死亡 |
| 35 | 慢性毒性 | 靜脈注射 | 小鼠 | 9 mg/kg/5D-I | 1.血液毒性——紅細胞染色異常或影響有核紅細胞 2.血液毒性——白細胞減少 3.血液毒性——紅細胞計數發生變化 |
| 36 | 慢性毒性 | 靜脈注射 | 狗 | 17500 ug/kg/36W-I | 1.心臟毒性——心律失常 2.肺部、胸部或者呼吸毒性——急性肺水腫 3.皮膚和附屬檔案毒性——毛髮變化 |
| 37 | 慢性毒性 | 靜脈注射 | 狗 | 7250 ug/kg/5D-I | 1.行為毒性——影響食物攝入量 (動物) 2.胃腸道毒性——運動過度、腹瀉 3.慢性病相關毒性——死亡 |
| 38 | 慢性毒性 | 靜脈注射 | 狗 | 13750 ug/kg/26W-I | 1.心臟毒性——心電圖發生變化 2.血管毒性——血壓調節能力下降 3.血液毒性——骨髓發生變化 |
| 39 | 慢性毒性 | 靜脈注射 | 狗 | 6250 ug/kg/18W-I | 1.心臟毒性——心電圖發生變化 |
| 40 | 慢性毒性 | 靜脈注射 | 猴 | 23360 ug/kg/36W-I | 1.心臟毒性——其他變化 2.肺部、胸部或者呼吸毒性——急性肺水腫 3.肝毒性——其他變化 |
| 41 | 慢性毒性 | 靜脈注射 | 猴 | 20800 ug/kg/5D-I | 1.心臟毒性——心電圖發生變化 2.胃腸道毒性——運動過度、腹瀉 3.慢性病相關毒性——死亡 |
| 42 | 慢性毒性 | 靜脈注射 | 兔 | 20 mg/kg/8W-I | 1.心臟毒性——心輸出量發生變化 2.血管毒性——血壓調節能力下降 3.營養和代謝系統毒性——鈣濃度發生變化 |
| 43 | 慢性毒性 | 腹腔注射 | 倉鼠 | 27 mg/kg/3W-I | 1.心臟毒性——心肌病包括梗死 2.皮膚和附屬檔案毒性——皮炎 (全身暴露後) 3.營養和代謝系統毒性——體重下降或體重增加速率下降 |
| 44 | 眼部毒性 | 皮膚表面 | 兔 | 15 mg/24H | |
| 45 | 突變毒性 | | 鼠傷寒沙門氏菌 | 2560 ng/plate | |
| 46 | 突變毒性 | | 鼠傷寒沙門氏菌 | 1 ug/plate | |
| 47 | 突變毒性 | | 鼠傷寒沙門氏菌 | 600 ug/L | |
| 48 | 突變毒性 | | 鼠傷寒沙門氏菌 | 6 ug/plate | |
| 49 | 突變毒性 | | 大腸桿菌 | 50 mg/L | |
| 50 | 突變毒性 | | 大腸桿菌 | 10 umol/L | |
| 51 | 突變毒性 | | 大腸桿菌 | 10 umol/L | |
| 52 | 突變毒性 | | 大腸桿菌 | 10 umol/L | |
| 53 | 突變毒性 | | 大腸桿菌 | 1 ug/plate | |
| 54 | 突變毒性 | | 枯草芽孢桿菌 | 500 ng/plate | |
| 55 | 突變毒性 | | Microorganism ed | 5 umol/L | |
| 56 | 突變毒性 | | Microorganism ed | 10 umol/L | |
| 57 | 突變毒性 | 口服 | 黑腹果蠅 | 1 gm/L | |
| 58 | 突變毒性 | 腸外 | 黑腹果蠅 | 250 mg/L | |
| 59 | 突變毒性 | | 釀酒酵母 | 184 umol/L | |
| 60 | 突變毒性 | | 構巢麴黴 | 100 mg/L | |
| 61 | 突變毒性 | | 草蜢細胞 | 250 nmol/L | |
| 62 | 突變毒性 | | 草蜢細胞 | 125 nmol/L | |
| 63 | 突變毒性 | | 非哺乳動物睪丸 | 1 umol/L | |
| 64 | 突變毒性 | | 人類淋巴細胞 | 20 ug/L | |
| 65 | 突變毒性 | | 人類卵巢 | 10 umol/L | |
| 66 | 突變毒性 | | 人類 細胞 | 1250 ug/L | |
| 67 | 突變毒性 | | 人類 細胞 | 250 ug/L | |
| 68 | 突變毒性 | | 人類 細胞 | 500 nmol/L | |
| 69 | 突變毒性 | | 人類淋巴細胞 | 50 ug/L | |
| 70 | 突變毒性 | | 人類 細胞 | 700 nmol/L | |
| 71 | 突變毒性 | | 人類成纖維細胞 | 100 umol/L | |
| 72 | 突變毒性 | | 人類成纖維細胞 | 500 ug/L | |
| 73 | 突變毒性 | | 人類淋巴細胞 | 100 ug/L | |
| 74 | 突變毒性 | | 人類淋巴細胞 | 1 mg/L | |
| 75 | 突變毒性 | | 人類淋巴細胞 | 10 umol/L | |
| 76 | 突變毒性 | | 人類白細胞 | 10 umol/L | |
| 77 | 突變毒性 | | 海拉細胞 | 1 umol/L | |
| 78 | 突變毒性 | | 人類 細胞 | 1 umol/L | |
| 79 | 突變毒性 | | 人類 細胞 | 10 nmol/L/2H | |
| 80 | 突變毒性 | | 人類 細胞 | 10 nmol/L/2H | |
| 81 | 突變毒性 | | 人類淋巴細胞 | 500 ug/L | |
| 82 | 突變毒性 | | 人類 細胞 | 30 nmol/L | |
| 83 | 突變毒性 | | 人類 細胞 | 150 ug/L | |
| 84 | 突變毒性 | | 人類 細胞 | 150 ug/L | |
| 85 | 突變毒性 | | 人類 細胞 | 50 nmol/L | |
| 86 | 突變毒性 | | 人類 細胞 | 400 ug/L | |
| 87 | 突變毒性 | | 人類 細胞 | 800 ug/L | |
| 88 | 突變毒性 | | 人類 細胞 | 1 umol/L | |
| 89 | 突變毒性 | | 人類白細胞 | 20 ug/L | |
| 90 | 突變毒性 | | 人類淋巴細胞 | 10 ug/L | |
| 91 | 突變毒性 | | 人類成纖維細胞 | 10 ug/L/1H | |
| 92 | 突變毒性 | | 人類 細胞 | 50 nmol/L | |
| 93 | 突變毒性 | | 人類淋巴細胞 | 5 ng/L/48H | |
| 94 | 突變毒性 | | 人類 細胞 | 1 umol/L | |
| 95 | 突變毒性 | | 人類 細胞 | 1 umol/L | |
| 96 | 突變毒性 | 腹腔注射 | 大鼠 | 5 mg/kg | |
| 97 | 突變毒性 | 腸外 | 大鼠 | 1250 ug/kg/2D (間斷) | |
| 98 | 突變毒性 | | 大鼠 細胞 | 1 ug/L | |
| 99 | 突變毒性 | | 大鼠胎兒 | 150 ug/L | |
| 100 | 突變毒性 | | 大鼠 細胞 | 6800 ug/L | |
| 101 | 突變毒性 | | 大鼠肝 | 6100 nmol/L | |
| 102 | 突變毒性 | | 大鼠 細胞 | 1150 ug/L | |
| 103 | 突變毒性 | | 大鼠 細胞 | 1 mg/L | |
| 104 | 突變毒性 | 靜脈注射 | 大鼠 | 5 mg/kg/8H (間斷) | |
| 105 | 突變毒性 | | 大鼠肝 | 50 nmol | |
| 106 | 突變毒性 | | 大鼠肝 | 2910 pmol/L | |
| 107 | 突變毒性 | | 大鼠乳腺 | 100 nmol/L | |
| 108 | 突變毒性 | | 大鼠乳腺 | 10 umol/L | |
| 109 | 突變毒性 | | 大鼠 鼠傷寒沙門氏菌 | 200 mg/kg | |
| 110 | 突變毒性 | 腹腔注射 | 大鼠 | 2 mg/kg | |
| 111 | 突變毒性 | 腹腔注射 | 小鼠 | 2 mg/kg/24H | |
| 112 | 突變毒性 | | 小鼠淋巴細胞 | 5 ug/L | |
| 113 | 突變毒性 | | 小鼠淋巴細胞 | 100 ug/L | |
| 114 | 突變毒性 | | 小鼠成纖維細胞 | 1 ug/L | |
| 115 | 突變毒性 | | 小鼠 細胞 | 5 umol/L | |
| 116 | 突變毒性 | | 小鼠 細胞 | 2 umol/L | |
| 117 | 突變毒性 | 腹腔注射 | 小鼠 | 5 mg/kg | |
| 118 | 突變毒性 | | 小鼠白細胞 | 260 nmol/L | |
| 119 | 突變毒性 | | 小鼠腹水瘤細胞 | 600 ug/kg | |
| 120 | 突變毒性 | | 小鼠 細胞 | 4 umol/L | |
| 121 | 突變毒性 | | 小鼠 細胞 | 5 ug/L | |
| 122 | 突變毒性 | | 小鼠白細胞 | 10 mg/L | |
| 123 | 突變毒性 | | 小鼠乳腺 | 400 ug/L | |
| 124 | 突變毒性 | | 小鼠淋巴細胞 | 20 ug/L | |
| 125 | 突變毒性 | 靜脈注射 | 小鼠 | 15 mg/kg | |
| 126 | 突變毒性 | | 小鼠 細胞 | 100 nmol/L | |
| 127 | 突變毒性 | | 小鼠白細胞 | 2900 nmol/L | |
| 128 | 突變毒性 | 腹腔注射 | 小鼠 | 5 mg/kg | |
| 129 | 突變毒性 | | 小鼠白細胞 | 10 mg/L | |
| 130 | 突變毒性 | 腹腔注射 | 小鼠 | 10 mg/kg | |
| 131 | 突變毒性 | | 小鼠 細胞 | 150 ug/L | |
| 132 | 突變毒性 | | 小鼠淋巴細胞 | 6600 ug/L | |
| 133 | 突變毒性 | | 小鼠 細胞 | 1800 nmol/L | |
| 134 | 突變毒性 | | 小鼠 細胞 | 18 umol/L | |
| 135 | 突變毒性 | | 小鼠淋巴細胞 | 5 ug/L | |
| 136 | 突變毒性 | | 小鼠白細胞 | 400 ug/L | |
| 137 | 突變毒性 | 腹腔注射 | 小鼠 | 500 ug/kg | |
| 138 | 突變毒性 | | 小鼠成纖維細胞 | 50 ug/L | |
| 139 | 突變毒性 | 靜脈注射 | 小鼠 | 500 ug/kg | |
| 140 | 突變毒性 | | 小鼠白細胞 | 100 ug/L | |
| 141 | 突變毒性 | 腸外 | 小鼠 | 5 mg/kg | |
| 142 | 突變毒性 | 腹腔注射 | 小鼠 | 250 ug/kg | |
| 143 | 突變毒性 | 靜脈注射 | 小鼠 | 12 mg/kg | |
| 144 | 突變毒性 | | 小鼠腹水瘤細胞 | 5 mg/kg | |
| 145 | 突變毒性 | | 小鼠淋巴細胞 | 3 mg/kg | |
| 146 | 突變毒性 | | 小鼠淋巴細胞 | 5 gm/L | |
| 147 | 突變毒性 | 靜脈注射 | 小鼠 | 8 mg/kg | |
| 148 | 突變毒性 | 腹腔注射 | 小鼠 | 3 mg/kg | |
| 149 | 突變毒性 | | 小鼠淋巴細胞 | 5 ug/L | |
| 150 | 突變毒性 | | 小鼠 細胞 | 1 mg/kg | |
| 151 | 突變毒性 | 靜脈注射 | 小鼠 | 6 mg/kg | |
| 152 | 突變毒性 | | 倉鼠肺 | 100 ug/L | |
| 153 | 突變毒性 | | 倉鼠卵巢 | 1 mg/L | |
| 154 | 突變毒性 | | 倉鼠 細胞 | 5 mg/L | |
| 155 | 突變毒性 | | 倉鼠 細胞 | 5 mg/L | |
| 156 | 突變毒性 | | 倉鼠卵巢 | 400 ug/L | |
| 157 | 突變毒性 | | 倉鼠肺 | 300 ug/L/2H | |
| 158 | 突變毒性 | | 倉鼠成纖維細胞 | 200 nmol/L | |
| 159 | 突變毒性 | | 倉鼠卵巢 | 1 umol/L | |
| 160 | 突變毒性 | | 倉鼠肺 | 300 ug/L/2H | |
| 161 | 突變毒性 | | 倉鼠肺 | 10 ug/L | |
| 162 | 突變毒性 | | 倉鼠卵巢 | 160 ug/L | |
| 163 | 突變毒性 | | 倉鼠成纖維細胞 | 20 nmol/L | |
| 164 | 突變毒性 | | 雞 細胞 | 5 umol/L | |
| 165 | 突變毒性 | 靜脈注射 | 兔 | 1 mg/kg | |
| 166 | 致癌性 | 靜脈注射 | 大鼠 | 5 mg/kg | 1.致癌性——致癌(根據RTECS標準) 2.皮膚和附屬檔案毒性——腫瘤 |
| 167 | 致癌性 | 靜脈注射 | 大鼠 | 8 mg/kg | 1.致癌性——腫瘤(根據RTECS標準) 2.皮膚和附屬檔案毒性——腫瘤 |
| 168 | 致癌性 | 靜脈注射 | 大鼠 | 10 mg/kg | 1.致癌性——致癌(根據RTECS標準) 2.肺部、胸部或者呼吸毒性——腫瘤 3.皮膚和附屬檔案毒性——腫瘤 |
| 169 | 致癌性 | 靜脈注射 | 大鼠 | 5 mg/kg | 1.致癌性——可能致癌(根據RTECS標準) 2.皮膚和附屬檔案毒性——腫瘤 |
| 170 | 致癌性 | 靜脈注射 | 大鼠 | 8 mg/kg | 1.致癌性——致癌(根據RTECS標準) 2.皮膚和附屬檔案毒性——腫瘤 |
| 171 | 致癌性 | 靜脈注射 | 大鼠 | 10 mg/kg | 1.致癌性——致癌(根據RTECS標準) 2.皮膚和附屬檔案毒性——腫瘤 |
| 172 | 致癌性 | 靜脈注射 | 大鼠 | 5 mg/kg | 1.致癌性——致癌(根據RTECS標準) 2.皮膚和附屬檔案毒性——腫瘤 |
| 173 | 致癌性 | 靜脈注射 | 大鼠 | 5 mg/kg | 1.致癌性——可能致癌(根據RTECS標準) 2.皮膚和附屬檔案毒性——腫瘤 |
| 174 | 致癌性 | 靜脈注射 | 大鼠 | 2 mg/kg | 1.致癌性——腫瘤(根據RTECS標準) 2.皮膚和附屬檔案毒性——腫瘤 |
| 175 | 生殖毒性 | 腹腔注射 | 大鼠 | 8 mg/kg,雌性受孕 6-9 天后 | 1.生殖毒性——肌肉骨骼系統發育異常 |
| 176 | 生殖毒性 | 腹腔注射 | 大鼠 | 3 mg/kg,雌性受孕 10-12 天后 | 1.生殖毒性——新生兒體重增加量減少 |
| 177 | 生殖毒性 | 腹腔注射 | 大鼠 | 4 mg/kg,雌性受孕 6-9 天后 | 1.生殖毒性——胎兒毒性(如胎兒發育不良,但不至死亡) 2.生殖毒性——心血管循環系統發育異常 3.生殖毒性——泌尿系統發育異常 |
| 178 | 生殖毒性 | 腹腔注射 | 大鼠 | 3 mg/kg,雄性配種 1 天前 | 1.生殖毒性——雄性生精功能異常 (包括遺傳物質,精子形態,精子活力和計數) 2.生殖毒性——睪丸,附睪,輸精管發生變化 3.生殖毒性——雄性生育能力下降 |
| 179 | 生殖毒性 | 腹腔注射 | 大鼠 | 4200 ug/kg,雌性受孕 7-13 天后 | 1.生殖毒性——肌肉骨骼系統發育異常 2.生殖毒性——新生兒身體變化 |
| 180 | 生殖毒性 | 腹腔注射 | 大鼠 | 2 mg/kg,雌性受孕 3 天后 | 1.生殖毒性——胚胎植入前死亡率上升 2.生殖毒性——植入後死亡率增加 3.生殖毒性——肌肉骨骼系統發育異常 |
| 181 | 生殖毒性 | 腹腔注射 | 大鼠 | 8 mg/kg,雌性受孕 9-12 天后 | 1.生殖毒性——胎兒毒性(如胎兒發育不良,但不至死亡) 2.生殖毒性——肌肉骨骼系統發育異常 |
| 182 | 生殖毒性 | 靜脈注射 | 大鼠 | 500 ug/kg,雄性配種 1 天前 | 1.生殖毒性——雄性生精功能異常 (包括遺傳物質,精子形態,精子活力和計數) |
| 183 | 生殖毒性 | 靜脈注射 | 大鼠 | 10 mg/kg,雄性配種 1 天前 | 1.生殖毒性——睪丸,附睪,輸精管發生變化 |
| 184 | 生殖毒性 | 靜脈注射 | 大鼠 | 3 mg/kg,雄性配種 1 天前 | 1.生殖毒性——雄性生精功能異常 (包括遺傳物質,精子形態,精子活力和計數) 2.生殖毒性——睪丸,附睪,輸精管發生變化 |
| 185 | 生殖毒性 | 靜脈注射 | 大鼠 | 8 mg/kg,雄性配種 1 天前 | 1.生殖毒性——雄性生精功能異常 (包括遺傳物質,精子形態,精子活力和計數) |
| 186 | 生殖毒性 | 靜脈注射 | 大鼠 | 8 mg/kg,雄性配種 1 天前 | 1.生殖毒性——雄性生精功能異常 (包括遺傳物質,精子形態,精子活力和計數) |
| 187 | 生殖毒性 | 腸外 | 大鼠 | 61336 ug/kg,雄性配種 56 天前 | 1.生殖毒性——雄性生精功能異常 (包括遺傳物質,精子形態,精子活力和計數) |
| 188 | 生殖毒性 | 未報告 | 大鼠 | 4500 ug/kg,雌性受孕 10-12 天后 | 1.生殖毒性——泌尿系統發育異常 2.生殖毒性——新生兒體重增加量減少 3.生殖毒性——影響新生兒的行為 |
| 189 | 生殖毒性 | 靜脈注射 | 小鼠 | 2 mg/kg,雄性配種 1 天前 | 1.生殖毒性——雄性生精功能異常 (包括遺傳物質,精子形態,精子活力和計數) |
| 190 | 生殖毒性 | 靜脈注射 | 小鼠 | 7 mg/kg,雌性受孕 7-13 天后 | 1.生殖毒性——胚胎或胎兒死亡 2.生殖毒性——肌肉骨骼系統發育異常 |
| 191 | 生殖毒性 | 靜脈注射 | 小鼠 | 700 ug/kg,雌性受孕 7-13 天后 | 1.生殖毒性——新生兒身體變化 |
| 192 | 生殖毒性 | 靜脈注射 | 小鼠 | 4200 ug/kg,雌性受孕 7-13 天后 | 1.生殖毒性——胎兒毒性(如胎兒發育不良,但不至死亡) |
| 193 | 生殖毒性 | 靜脈注射 | 兔 | 7800 ug/kg,雌性受孕 6-18 天后 | 1.生殖毒性——流產 |
物質毒性參考資料: