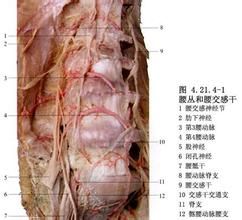
發病機制
病因:
許多病因可引起交感神經鏈綜合徵。如各種急性及慢性感染全身性或局部感染各種內源性外源性中毒,以及外傷、脊柱退行性疾病腫瘤、血管性疾病和慢性刺激性病灶等。
 交感神經鏈綜合徵
交感神經鏈綜合徵本病因不同交感神經節受損而導致相應臨床表現。病理改變因原發病不同而異。感染性炎症引起可見到細胞內空泡形成及脂肪變性,伴神經節間質及周圍組織充血、水腫和浸潤中毒和敗血症引起可見神經節細胞壞死。
在動物模型中結紮/切斷大鼠坐骨神經或脊神經是神經源性SMP經典動物模型。在Kim和Chung的模型上,進行過兩種實驗。
(1)先手術切斷雙側腰2至腰6交感神經,7天后再結紮單側腰5和腰6脊神經,大鼠不再產生神經源性疼痛。
(2)先結紮脊神經引起神經源性疼痛,再切斷雙側腰2至腰6交感神經,幾乎可完全消除結紮脊神經所致的神經源性疼痛。
Kinnman等切斷大鼠支配腰5脊神經的腰4交感神經,對切斷腰5脊神經所致的神經源性疼痛的產生和維持具有抑制作用。而切斷支配腰4脊神經的腰3交感神經,對上述神經源性疼痛不產生影響。說明外周神經損傷後,交感神經系統可能與疼痛感受系統形成耦聯,脊神經損傷節段的交感神經節後神經元對神經源性疼痛起著重要的作用。
正常大鼠背根神經節(Dorsalrootganglion,DRG)內有少量沿血管走行的交感神經節後纖維。結紮大鼠脊神經後,其DRG內交感神經節後纖維的數量與正常相比明顯增加,DRG神經元周圍間質腔隙包含囊泡的軸突擴大,沿著交感纖維的長軸有串珠狀的曲張體。一些DRG神經元尤其是大神經元被數層交感神經節後纖維所包繞,形成交感神經節後纖維包繞神經元的籃狀結構,可見耦聯形成於DRG處,其內有交感神經節後纖維的出芽生長,交感神經突觸部的曲張體很可能是DRG部位交感-感覺耦聯的結構基礎。Ramer等人認為交感軸突出芽生長與受損神經殘端的神經生長因子(Nervegrouthfactor,NGF)的水平上調引起Wallerian變性有關,後者可逆行傳輸到未損傷的感覺軸突,引起交感軸突發芽生長。所以Wallerian變性與交感神經出芽生長有密切聯繫,NGF起介質作用。另外,外周神經損傷後DRG區域交感神經的發芽生長程度與損傷神經纖維數量有關,而與神經源性疼痛的表現程度無關。而且DRG出芽生長的交感神經纖維密度隨著年齡增長而增長,這也許是SMP多見於老年人的緣故。以上表明,交感神經系統不僅僅具有調節自主神經功能,還在感覺通路的傳導上扮演了重要角色。
臨床表現
1、本病可發生於任何年齡,兩性均可發生,臨床上並非少見,因在晚期才出現典型症狀,使臨床診斷率較低多為亞急性或慢性起病亦可急性起病,通常有轉為慢性遷延、時起時伏的趨勢。局部交感神經鏈病變的基本特徵是:具有節段性不對稱性及強烈擴散性和周期性加重等特點因受損的交感神經節不同臨床表現不盡相同但都有共同的臨床症狀。
2、疼痛及感覺障礙疼痛呈發作性或持續性,伴發作性加劇,夜間較重,情緒波動體力勞動天氣變化及寒冷刺激等因素均可使疼痛加重。範圍較彌散有廣泛擴散趨勢。受損交感神經節的體表投射區可出現壓痛如發現壓痛點常有助於定位診斷可出現各種各樣的感覺異常如麻木、蟻走樣感等,客觀感覺障礙較主觀症狀輕,多為痛覺異常,溫度覺異常較少見觸覺及深感覺障礙更少見。
3、皮膚及附屬器改變皮膚可出現刺激性症狀如出汗增多及立毛反射亢進;亦可表現為功能缺失症狀如皮膚導電性能減低出汗減少及立毛反射減弱等此外皮膚還可出現營養障礙、乾燥萎縮、毛髮脫落及指(趾)甲變脆等。
4、血管功能障礙主要表現為小動脈和毛細血管痙攣亦可出現血管張力減退甚至發生麻痹,以及軀體神經功能障礙。
臨床證據
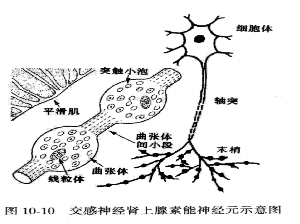 腎上腺素示意圖
腎上腺素示意圖以下證據表明交感神經末梢釋放的去甲腎上腺素(NE)作用於腎上腺素α受體是SMP產生和維持的關鍵性因素。對於局部交感神經阻滯後疼痛緩解的SMP病人,在其原疼痛區域皮下注射NE10mmol能使疼痛復現,而注射生理鹽水的對照組則無疼痛產生。同時用都卜勒雷射探測手掌皮膚血流,只有當NE達到10mmol時血管有明顯收縮。在試驗組非疼痛區域和對照組注射NE不會引起疼痛。10分鐘後向SMP病人引起疼痛區域注入腎上腺素受體拮抗劑酚妥拉明(1mg/kg)能使疼痛和疼痛過敏緩解。這說明皮下注射NE能引起SMP病人疼痛,且使用劑量必須達到引起血管收縮劑量。PatrickD.Wall等提出,外周使用α受體阻滯劑酚妥拉明或選擇性α2受體阻滯劑育亨賓可有效減輕神經源性疼痛的痛覺過敏,而α1受體阻滯劑哌唑嗪則無效。以上說明拮抗腎上腺素作用能對抗SMP,其中α1受體對SMP的形成影響,而α2受體對SMP的形成起促進作用。採用離子導入法將呱乙啶和生理鹽水預先導入前臂皮膚,再導入小劑量腎上腺素以引起血管收縮,胍乙啶組血管收縮反應明顯提高。提示呱乙啶延長了貯存腎上腺素的消耗,引起腎上腺素超敏感,產生腎上腺素介導的痛覺過敏。但Rubin等指出受損傳入神經元引起的腎上腺素敏感化不一定需要交感節後神經纖維參與。一部分學者也支持"非直接耦聯"學說:皮膚炎性介質NA反過來作用於交感末梢,釋放前列腺素類介質,使傳入末端敏感化,也就是腎上腺素作用通過其它非腎上腺素類化學介質及受體介導。
臨床上根據病因及引起疼痛的機理不同,將疼痛大體上分為三種類型:
①傷害源性疼痛,與各種傷害性刺激作用於傷害感受器有關;
②神經源性疼痛,與神經損傷或自發性功能障礙有關;
③交感神經性疼痛,主要表現為交感神經介導性,與交感神經的功能障礙、受損有關。在臨床實際工作中所遇到的慢性疼痛。
雖然絕大多數是上述三種類型的混合性疼痛,但是,根據其主要病因的不同,而又有不同的臨床表現。其中,與
交感神經介導性密切相關的疼痛,大體包含如下幾個方面。
1、複雜的局部痛綜合徵(ComplexRegionalPainSyndrome,CRPS)指繼發於意外損傷、醫源性損傷或全身性疾病之後,出現的以嚴重頑固性、多變性疼痛,營養不良和功能障礙為特徵的臨床綜合徵。它包含了兩類典型的交感神經性疼痛疾病,即反射性交感神經萎縮症(refrexsympatheticdystrophyRSD)和灼性神經痛(causalgia)。此類疼痛性疾病,儘管病因及機理不同,但臨床表現多有相似之處,故多命名為損傷後疼痛綜合徵、灼性神經痛、痛性營養不良、慢性損傷性水腫、損傷後血管運動障礙等等。
2、內臟痛
來源於胸、腹、盆腔等內臟器官的疼痛,可通過植物性神經向中樞傳導,多由腫瘤、缺血或炎性病變等原因引起。其特點是:部位不明確,疼痛範圍廣泛,常伴牽涉痛。而壁層胸、腹膜及腸系膜、膈肌引發的疼痛,則由體神經傳導,故一旦病變侵襲,即可出現較為固定而明確的疼痛。
3、周圍血管性疼痛性疾病
包括周圍血管收縮功能失調、栓塞、硬化等病變引起的疼痛。這些疾病大多存在著交感神
經功能失調,可通過交感神經阻滯進行診斷、判斷預後和治療。如雷諾氏病、紅瘢性肢痛症、手足發紺症、網狀青斑、動靜脈栓塞、脈管炎、視網膜病變等。
檢查方法
 頭顱肢體檢查
頭顱肢體檢查1、血尿便常規及生化檢查與原發病相關
2、腦脊液常規檢查多無特異性。
其它輔助檢查:
1、頭顱肢體影像學檢查有鑑別診斷意義。
2、藥物和毒物檢測也具有病因鑑別診斷意義.
全身或局部的植物性神經功能判斷,對疼痛性疾病的診斷、治療、療效判定、併發症的防治和預後判斷均有十分重要的意義。由於植物性神經系統的節後神經元的數量遠比節前纖維多(其比值約1∶2~30),故一個節前神經纖維元的衝動,可引起大量的節後細胞放電。單個神經即可引起廣泛的、定位不精確的症狀。即少量節前神經元可控制相當大範圍的外周效應器官。這種解剖學聯繫,對外周組織和終末器官的反應起著放大的作用。
上述特點決定了臨床上交感神經性疼痛的複雜性及對各種療法反應的多變性。在疼痛性疾病的診療過程中,把握治療前、後植物神經系統的功能狀態是十分必要的。神經阻滯前應重視植物性神經系統功能的檢查。對於典型的病變,其診斷和制訂治療方案並不困難。而有些病變是否屬於植物神經性,或在病變發生過程中植物性神經參與的程度如何,並不十分明顯,需要在充分把握全身或局部的植物性神經功能狀況下,方能對其做出正確的判斷。曾有報導行SGB後發生心跳驟停的病例,事後分析為迷走神經張力過高所致。神經阻滯後植物性神經功能的檢查更顯重要。在判定神經阻滯效果的基礎上,對鑑定疼痛類型、決定治療方案及判斷預後等起著重要的作用。對神經阻滯後客觀效果的判斷,有時需做極為精細的檢查。如微量精神發汗法、微小神經電極法等。
 交感神經鏈綜合徵
交感神經鏈綜合徵常用的植物性神經功能檢查方法
1、眼心反射:仰臥閉眼,用手指輕壓病人一眼球的兩側,3~4秒後(有輕度疼痛)開始數脈搏(數15秒),記錄每分鐘的脈搏數,並與檢查前的脈搏數相比較。正常人檢查後可減少4~7次/分。若患者減少12次/分以上者為陽性,說明迷走神經張力增高;減少18~24次/分以上者,迷走神經張力顯著增高。此種病人特別容易發生暈厥,在治療過程中有發生心跳驟停的可能。除心率減慢外,脈搏力量也常常減弱,臨床上可有眼前發黑、頭暈、噁心甚至嘔吐,通常稱為迷走神經緊張症。反之,若壓眼球後脈搏反而增加,稱為倒錯反應,說明病人有交感神經張力增高。
2、白色劃紋症:用竹籤或指甲輕而快地划過皮膚(下肢表現較為明顯),8~20秒內出現白色劃紋,持續3~5分鐘。這是由於神經性反射引起血管收縮所致,表明交感神經興奮性增高。
3.紅色劃紋症:用竹籤稍加壓力划過皮膚,正常3~5秒出現紅色劃紋,持續8~30分鐘。若紅紋較寬、持續時間較久,可能與副交感神經興奮性增高有關。嚴重時,划過皮膚1~2分鐘方可出現,且持續1~12小時。引起劃紋處皮膚隆起、水腫,系血管擴張並有血液滲出所致。皮膚劃紋症在正常人也可出現,只有在持續時間過長、或無論輕重劃法均出現一種反應時,才有臨床參考意義。
4、臥立試驗:讓患者平臥,計數1分鐘脈搏;然後坐起,再計1分鐘脈搏。由臥位到立位脈搏增加10~20次/分,為交感神經興奮性增強;由立位到臥位若減少10~20次/分,為副交感神經興奮性增強。
5、豎毛反射:將冰塊或其他寒冷刺激物置於患者頸後或腋窩皮膚上數秒,可見豎毛肌收縮,皮膚毛囊處隆起呈雞皮樣外觀。該反射受交感神經節段性支配,根據不同部位的反應,可對交感神經功能障礙進行定位診斷。如C8~T3支配頭面部、頸部,T4~7支配上肢,T8~9支配軀幹,T10~L2支配下肢。
6、微量發汗測定法:皮膚濕度與汗腺的功能是有關聯的。溫熱性出汗主要與環境溫度有關,可調節人體體溫。神經性發汗主要由植物神經功能控制。汗腺受膽鹼能交感神經的節後纖維支配,通過監測皮膚的神經性微量汗腺分泌,可以及時判定交感神經的緊張度。
7、微小神經電極法:採用矽碳微小神經電極,尖端直徑0.1μ,可以插入單個神經細胞內,在銅網禁止的環境下,通過電子儀器放大,直接引出交感神經的衝動發放。這是判斷交感神經功能最直接的方法之一。
8、診斷性交感神經阻滯:是臨床上最常用的方法。選擇性阻滯支配病變部位的交感神經,若阻滯後疼痛迅速緩解,患病部位由陰冷潮濕,轉為舒適的溫曖感,面部皮膚溫度升高,發汗減少;則說明該痛症的發生與交感神經密切相關。
9、其他:心電圖R2R間期法,血中激素濃度測定等。CRPS的概念一般認為,如反射性交感神經萎縮症(refrexsympatheticdystrophyRSD)、灼性神經質痛(causalgia)等病變,均為交感神經機能異常亢進所致,屬典型的交感神經相關性疼痛,故交感神經阻滯應有良好的療效。可是,臨床上常可遇到一些病例,即使對其行完善的交感神經阻滯,也不能完全阻止其病痛的發作;甚至還有一些患者,在交感神經阻滯後,疼痛反而加重。這種現象提示:儘管有些病例有著完全相同的臨床症狀,但因發病機理不盡相同,故對交感神經阻滯的反應各異。故有人提倡,在這類疾病中,把對交感神經阻滯反應良好的叫做交感神經維持性疼痛(sympatheticallymaintainedpainSMP);對交感神經阻滯無反應的叫做交感神經無關性疼痛(sympatheticallyindependentpainSIP),而對於那些交感神經阻滯後而疼痛加重的叫做ABC綜合徵(AngryBackfiringC2nociceptorsyndromeABC綜合徵)。即使在同一病人,在病程發展的不同階段;也可有SMP、SIP、ABC綜合徵等表現。為此,國際疼痛學會提出了複雜的局部痛綜合徵(ComplexRegionalPainSyndromeCRPS)的概念。即因局部損傷所引起的病理性疼痛,因持續時間過久,常常導致運動功能低下,並隨著時間的推移,可進行性地引起多種綜合徵。當然,在CRPS中,包括了傳統的RSD和灼性神經痛。通常把CRPS分為兩型。RSD屬於CRPSⅠ型,即有神經損傷的可能性,但不能確定究竟是什麼神經受損。而灼性神經痛屬於CRPSⅡ型,常有較明顯且明確的神經損傷。其中,絕大多數為交感神經維持性疼痛。
疼痛可發生於四肢、軀幹,也可發生於頭面部。疼痛性質表現為燒灼樣痛、針刺樣痛,伴有血管舒縮功能異常如出汗異常,喜暖怕涼,遇冷加重,溫暖時有一定緩解。查體可有痛覺過敏、痛覺超敏和自發痛。血管運動障礙表現為:早期皮膚濕潤潮紅腫脹,皮溫可高可低不定,後期缺血性改變如皮溫下降,皮膚蒼白。隨著疾病進行性發展,毛髮指甲生長速度減慢,出現營養不良表現如皮膚菲薄、指甲捲曲失去光澤、肌力下降、肌肉廢用性萎縮、關節僵直,X線顯示局部斑片狀骨密度降低、骨質疏鬆,這些是由於血運不良所致。
輔助檢查
常用的植物性神經功能檢查方法:
(1)眼心反射:若減少12次/分以上者為陽性,說明迷走神經張力增高。反之若壓眼球後脈搏反而增加,說明病人交感神經張力增高。
(2)白色劃紋症:這是由於神經性反射引起血管收縮所致,表明交感神經興奮性增高;若副交感神經興奮性增高則表現為紅色劃紋症。
(3)臥立試驗:由臥位到立位脈搏增;10~20次/,提示交感神經興奮性增強,由立位到臥位若減少10~20次/分,為副交感神經興奮性增強。
(4)其它還有:豎毛反射;微量發汗測定法;微小神經電極法;心電圖R2R間期法;血中激素濃度測定等。SMP可有上述一項或幾項檢查陽性,提示交感神經功能亢進或減退,但這並不能作為診斷SMP的標準,診斷SMP的臨床標準應為對交感神經阻滯有效。
治療措施
 交感神經鏈綜合徵
交感神經鏈綜合徵常用治療方法
1、交感神經阻滯 通過阻斷其介導的疼痛,擴張支配區域血管達到治療作用。
(1)星狀神經節阻滯(StellategangeionblockSGB):頸部交感神經乾每側有3個交感節,分別稱頸上、中、下節,頸下神經節常與胸1交感神經合併成星狀,故名星狀神經節。星狀神經節阻滯使分布區內的交感神經纖維支配的心血管運動、腺體分泌、肌肉緊張、痛覺傳導受到抑制,這些外周作用被用來治療頭、頸、肩、心臟和肺的一些疾病。SGB阻滯一般以出現Horner’s征為成功標誌。值得注意的是,SGB應以單一用藥為原則,只使用局麻藥為好,無需複雜的消炎鎮痛配方,否則有悖於治療原理。其療效可能比較緩慢,應進行反覆多次阻滯以求最佳效果。
(2)胸交感神經阻滯:胸部交感神經每側一般有10~12個,其分支主要分布於胸腹壁、肝脾腎等實質臟器和結腸左曲以上的消化管,多用於胸腹壁和部分臟器的SMP。國外報導常採用腹腔鏡胸行交感神經阻滯治療頭、頸、胸部多汗症並取得良好效果。
(3)腰交感神經阻滯:腰交感乾由3~5節交感神經節組成,腰1~4交感神經節主要分支支配下肢的交感神經。常使用局麻藥或神經毀損藥或射頻熱凝對腰交感神經阻滯,對於下肢血管性疾病以及腰椎管狹窄引起的下肢疼痛短期療效顯著,長期療效大於50%,並能有效降低潰瘍的發生。腰交感神經阻滯對於改善下肢溫度有顯著效果。Tran等報導,行腰交感阻滯後同側拇趾皮溫提高3℃以上,自發性疼痛也隨之緩解。但要注意雙側阻滯可能會影響男性勃起功能。
(4)腹腔神經叢阻滯:位於腹主動脈上段前方,圍繞腹腔動脈和腸系膜動脈根部,接納來源於內臟大神經的節前纖維,其分支有肝叢、胃叢、脾叢、胰叢、腎叢和腸系膜上叢,並沿同名血管到達各臟器。腹腔神經叢阻滯能有效緩解頑固性上腹疼痛,有效率達70~90%。
(5)內臟神經阻滯:Fujita2Y報導,對上腹癌痛病人使用15ml無水酒精進行內臟神經毀損能有效緩解疼痛,大幅度減少嗎啡用量。
(6)腸系膜下神經叢阻滯:主要用於腸系膜下動脈支配區域的下腹痛。
(7)上腹下神經叢阻滯:位於腰5椎體前方,髂總動脈分叉處下方。主要用於來自盆腔臟器如膀胱、直腸、子宮附屬檔案等病變所致的疼痛,對於盆腔良性和惡性疼痛皆有良好效果。
(8)奇神經節阻滯:主要用於肛周、會陰部疼痛。Munglani對16例晚期宮頸癌、直腸癌、膀胱癌的病人行奇神經局麻藥阻滯全部獲得疼痛緩解,再次注入4~6ml酚甘油後8例獲100%長期緩解,其餘獲50%以上長期緩解。
(9)硬膜外交感神經阻滯:對於範圍較廣泛的SMP,採用0.5%的利多卡因持續硬膜外輸注,打斷疼痛的惡性循環,多可取得較好療效。其中,胸段硬膜外交感神經阻滯常用於不穩定性心絞痛的治療。
2、受體拮抗劑治療
比較常用的是酚妥拉明靜脈給藥,它具有阻滯全身交感神經的作用,特別適用於全身多處患有SMP的病人,具有用法簡單、安全性高、無創等特點。套用酚妥拉明前先靜脈注射心得安2mg,用以預防酚妥拉明易引起的心動過速。將酚妥拉明1mg/kg於10分鐘內靜脈輸入。其間每5分鐘測定一次疼痛評分。酚妥拉明輸注完畢後繼續監測心電血壓並測定疼痛評分30分鐘。若輸注酚妥拉明後疼痛明顯緩解(VAS評分下降75%以上),可診斷為SMP。
 視頻控制下交感神經檢測圖
視頻控制下交感神經檢測圖3、交感神經切除術 多數人不主張使用,主要是術後數日至數周可能產生新的疼痛———交感神經切除術後痛,多發生於被切除交感神經支配的遠端肢體,出現交感去神經支配的症狀如過度出汗、深部肌肉壓痛、皮膚痛覺過敏,發生率高達30%~50%。可能是由於切斷了交感乾中的體壁神經和內臟傳入神經,導致軸突神經元細胞死亡,引起傳入神經阻滯性疼痛。
4、脊髓電刺激(Spinalcordstimulation,SCS) 主要用於定位明確的難治性SMP如頑固性心絞痛、周圍血管病、CRPS等。脊髓電刺激作為一項成熟的操作技術,在世界範圍內已得到越來越廣泛的套用。首先將單極或多極刺激電極過經皮穿刺技術放置入相應節段的硬膜外腔,用誘發電位刺激該脊髓節段觀察是否能涵蓋相應疼痛區域,然後進行為期一周左右的測試階段,若病人反應良好,則將刺激器永久埋入腹部或臀部皮下成為永久性刺激裝置。在全球已有10萬以上病例進行脊髓電刺激治療,總有效率約80%。SCS的鎮痛原理主要根據閘門理論,使用一種溫和的電刺激干擾疼痛的上傳通路。SCS對SMP的治療包括兩部分:一方面是由於SCS對交感神經的調節作用,削弱疼痛信號的傳導;另一方面是通過對交感持續血管收縮效應的抑制作用達到擴張血管、改善局部血流目的,使缺血病變癒合減少疼痛刺激傳入。SCS對神經源性疼痛刺激停止後,其鎮痛效果可持續數小時至數月,提示SCS在脊髓后角對神經遞質的變化和神經活動的變化有後續效應。SCS對於頑固性心絞痛有特殊治療效果,Mur2phy和Mannheiner報導20例心絞痛病例經SCS治療後臨床症狀改善,其心臟最大工作負荷時ECG上ST段下降幅度減少,心絞痛發作間期延長,發作時間縮短,但對最大心輸出量無影響。推測SCS治療作用可能與以下因素有關;減少心臟氧耗、降低周圍血管阻力、抑制疼痛信號傳入等。SCS治療下肢動脈梗阻性疾病,對於嚴重的硬皮病、糖尿病、血栓性脈管炎、雷諾氏綜合徵等所致的肢體缺血潰瘍,尤其是其它保守治療方法和交感神經切除無效,甚至重建外科方法不能奏效的病症,SCS治療仍能取得較好效果。SCS還可用於複雜性局部痛綜合徵、帶狀皰疹後神經痛、幻肢痛、殘肢痛等。SCS的併發症主要發生在電極植入時和植入後。在電極植入時首先可能遇到的問題是當電極在硬膜外腔向頭部移動時,會遇到組織阻擋而無法到達所需的位置,尤其是在頸段和胸段。在電極植入後所發生的併發症有無菌性和細菌性腦膜炎、部分橫斷性脊髓損傷、硬膜外膿腫、淺表部位的感染、電極移位和電極折斷,其中發生最多的併發症為電極移位。一旦被診斷為CRPS,應儘可能地及早尋求減輕疼痛的方法,同時積極開展康復治療。
預防性治療:受傷早期對創面的完善處理和充分的鎮痛是很重要的。即把疼痛完善地控制在急性期,阻止其向慢性化方向發展,同時結合精神方面的治療,一般認為可取得較好的療效。
神經阻滯治療:以交感神經阻滯為主。常用的神經阻滯有:SGB、胸交感神經阻滯、腰交感神經阻滯、靜脈內局部神經阻滯。也可酌情選用硬膜外阻滯、蛛網膜下腔阻滯及局部痛點阻滯。在局麻藥阻滯效果不明顯時,也有人試用柳胺苄心啶行交感神經阻滯。阻滯的原則是,反覆使用局麻藥,尤其是通過反覆阻滯,疼痛逐漸減輕者,更應持續進行阻滯。當局麻藥阻滯後,疼痛症狀未見改善或只是臨時改善時,要考慮使用神經破壞性藥物,進行神經毀損術或交感神經切除術。在進行交感神經乾、節阻滯時,應強調用藥單一、以局麻藥為主的原則。如臨床上廣泛套用的SGB,常有作者將很複雜的消炎鎮痛液配方,用於SGB。這樣做既無必要,又易增加併發症,也不符合SGB的治療機理。臨床上所行的交感神經阻滯,主要通過阻斷其介導的疼痛,擴張其支配區域的血管等,來發揮作用。在絕大多數的交感神經阻滯適應證中,所擬阻滯的交感神經乾、節等部位,本身並沒有炎性病變,在此處注射藥物的目的,僅在於臨時或永久性地阻止其神經傳導功能,以解除其所支配區域的血管痙攣、疼痛等。故從治療原理上講,與伴有炎性病變的脊神經根、乾及局部神經阻滯,有著根本的區別。不應以同一配方千篇一律地用於所有神經阻滯。
經皮電刺激(TENS):經皮電刺激是通過激活內源性阿片肽而鎮痛,也可刺激疼痛部位的粗纖維神經,通過閘門學說的機制而鎮痛,對改變感覺衝動傳入中樞神經系統,減輕慢性疼痛,終止其繼發性生理/病理反應,有著積極的作用。曾有單純依靠HANS治療的報導,可完全治癒三叉神經第一支帶狀皰症後神經痛及術後頑固性刀口痛的經驗。
抗憂鬱藥:常用的有阿密替林、丙密嗪、多慮平、麥普替林等三(四)環類抗憂鬱藥。過去多用於改善慢性疼痛的精神憂鬱狀態,後來發現該類藥物還具有獨特的鎮痛作用而被廣泛套用於慢性疼痛的治療中。主要通過抑制突觸部位的52羥色胺和去甲腎上腺素再吸收,影響中樞傳導遞質的量而產生抗憂鬱及鎮痛作用。而在慢性長期用藥時,其鎮痛作用的發揮尚與P物質、促甲素樣肽、γ2胺基丁酸的活性變化有關。一般成人從25mg/日起,老年人從10mg/日起,每晚睡前頓服。若效果不明顯,且無副作用,每數日可增加10~25mg,在達到150mg/日後,應維持使用1~2周。如無副作用,最大量不能超過300mg/日。當出現口乾時,表明藥量已足。用藥期間應密切注意其併發症(抗膽鹼、奎尼丁樣作用)的出現。
抗痙攣藥:代表性的藥物有卡馬西平、苯妥英鈉、丙戊酸鈉,對神經電擊樣的疼痛有效。國外套用較為廣泛的是加巴噴丁(gabapentin),可明顯緩解糖尿病或帶狀皰疹引起的神經痛。本類藥物作用原理不完全清楚,考慮與抑制受損神經元的異常放電或過度興奮有關。長期套用本類藥物會引起肝、腎、胃腸道及造血系統功能異常,故一般主張在密切監測下套用或交替使用。
抗心律失常藥:周圍神經受損後將導致其自發性興奮性增加,是引起中樞敏感性增加和發生慢性頑固性疼痛的的主要原因。被病毒侵襲的神經組織,由於Na通道過敏性亢進,容易導致神經纖維持續性興奮。故通過阻滯Na通道,
可抑制神經組織的興奮性而鎮痛。常用有慢心律,50~200mg,每日三次。心動過緩、房室傳導阻滯及嚴重心、肝、腎功能不全者禁用。
利多卡因:作用原理基本同慢心律,100~300mg/1~2小時,靜滴,有一定療效。
氯胺酮:NMDA受體的拮抗藥[7],可抑制感覺纖維的過度興奮。試用方法:0.3mg/kg,先靜注半量後,餘下的量在20分鐘內靜滴。效果不理想時,可加至0.6mg/kg,2~3周為一個療程。惡夢或噁心等副作用出現時,可用氟哌啶或咪唑安定對抗。
交感神經阻滯藥:有研究表明,交感神經性疼痛與受損部位的α2腎上腺能受體激活有關。耗竭交感神經末梢的去甲腎上腺素,可有效地對抗SMP。常用酚妥拉明,5mg/次,1~2次/日。
其他:非甾體類消炎鎮痛藥、神經妥樂平、前列腺素製劑、激素、嗎啡類藥物等。
心理學方面的治療:急性疼痛轉為慢性疼痛的過程中,隨著功能障礙的出現,患者的心理負擔在不斷加重,導致QOL低下。在治療疼痛的整個過程中,心理因素不能忽視,要適當地介入一些精神心理方面的治療,如認知療法、松靜療法、生物反饋療法、催眠等。