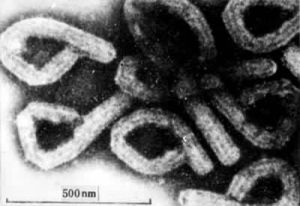
病毒簡介
馬爾堡病毒結構為典型的絲狀病毒,形似絲線,直徑通常一樣,但長度介於800至14,000納米(nm),通常感染力最強時長度約為790nm。病毒物質由七種已知蛋白質組成。馬爾堡病毒結構與依波拉幾乎一樣,但兩者的抗原反應不一。換言之,兩者在引致感染者體內產生的抗體不同。馬爾堡病毒是第一種被發現的線狀病毒。
兩種病毒形態相似,為多形性細長絲狀,可呈“U”形、“б”形或環狀,像空心的管道(見圖)。
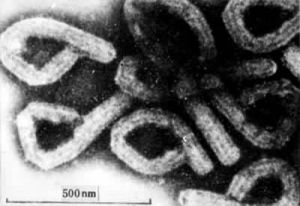 馬爾堡病病毒
馬爾堡病病毒歷史來源
 馬爾堡病毒
馬爾堡病毒馬爾堡出血熱最先有記載的爆發是在1967年的德國馬爾堡,31人獲病,病症亦因此而以該地命名,之後在法蘭克福及貝爾格勒亦有病例。31人中,25人是直接感染,當中七人死亡。直接染病的人多是因為接觸當地實驗室內染有馬爾堡病的猴子而致病。另外六人是二次感染,當中包括兩名醫生,一名護士,一名解剖助理,及一名獸醫的妻子。他們都是與直接感染的病人,有緊密接觸。兩名醫生是在抽血時不慎接觸病者血液染病。這次爆發的來源經調查後,發現是來自非洲烏干達一種品種為Cercopithecusaethiops的猴子。德國的一家公司入口該批染有病毒的猴子,原意是用來研製小兒麻痹症的疫苗。
1975年,一名從辛巴威回到南非的人,感染了另外三名南非人。但該次小規模爆發只引致了一人死亡。之後1980年及1987年在肯亞亦有發現馬爾堡出血病,但亦沒有大規模爆發。之後最大的爆發發生在1998年至2000年的剛果民主共和國。149宗個案中123人死亡。
馬爾堡病毒與伊波拉病毒屬於同“絲狀病毒科”家族,它的發現早於伊波拉病毒。在1967年秋,西德馬爾堡、法蘭克福和南斯拉夫貝爾格勒的幾所醫學實驗室的工作人員中同時暴發了一種嚴重出血熱,有31人發病,其中7人死亡,這些患者大都接觸過一批從烏干達運來的非洲綠猴。科學家們對患者的血液和組織細胞進行了培養,分離出一種以前沒有見到過的病毒。根據發病地點,將這種病毒命名為馬爾堡病毒。以後,在南非、肯亞、辛巴威也相繼出現過馬爾堡病毒感染的病例。
症狀
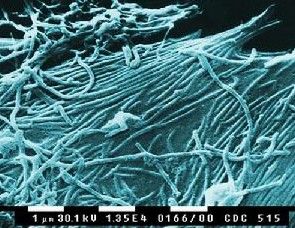 馬爾堡病病毒
馬爾堡病病毒馬爾堡病毒感染後,可引起臨床表現以發熱、出血症狀為主要表現的疾病,被稱為馬爾堡出血熱。由於馬爾堡病毒來自於非洲綠猴並主要在非洲流行,因此馬爾堡出血熱又被稱為青猴病和非洲出血熱。這種疾病最容易感染兒童,在非洲,有75%的病例發生在5歲以下兒童,成人感染者大多為與受感染兒童接觸密切的親屬和醫護人員。
馬爾堡出血熱的潛伏期一般為3~9天,病人突然發熱、畏寒、頭痛、全身疲乏、大量出汗、肌肉酸痛、咽痛、咳嗽、胸痛。最初的症狀很像流感,隨後病人會出現噁心、嘔吐、腹瀉、腹痛、全身皮疹,最後出現口鼻出血、尿血、陰道出血和消化道出血,嚴重者可發生休克,有大約1/4的患者死亡。
傳播途徑
 如圖
如圖主要經密切接觸傳播,即接觸病死動物和病人的屍體,以及感染動物和病人的血液、分泌物、排泄物、嘔吐物等,經黏膜和破損的皮膚傳播。在非洲疫區,因葬禮時接觸病人屍體,曾多次發生本病暴發。通過密切接觸也可以造成醫院感染和實驗室感染。此外,通過使用被污染的注射器等可造成醫源性傳播。有報導,病人在臨床康復3月內,仍可在精液中檢出馬爾堡病毒,因此,存在性傳播的可能性。通過含本病毒的氣溶膠感染實驗動物也有報導。
分子生物學
病毒基因組為單股負鏈RNA,長約19kb,編碼7種病毒蛋白,包括N蛋白(nucleoprotein,NP)、病毒蛋白35(VP35)、病毒蛋白30(VP30)、病毒蛋白24(VP24)、糖蛋白4(gp4)、RNA依賴的RNA聚合酶主要成分糖蛋白7(gp7)和次要成分病毒蛋白40(VP40)。
生物學特性
馬爾堡病毒病毒對熱有中度抵抗力,56℃30分鐘不能完全滅活,但60℃1小時感染性喪失。在室溫及4℃存放35天其感染性基本不變,-70℃可以長期保存。一定劑量的紫外線、γ射線、脂溶劑、β-丙內酯、次氯酸、酚類等均可滅活。本病毒可在多種細胞中培養,其中包括Vero細胞、VeroE6細胞和Hela細胞等。只發現一種血清型。
傳染源
感染病毒的非人靈長類動物和病人是主要傳染源。通常先由被感染的非人靈長類動物(如綠猴)將病毒傳染給人,然後再由病人傳染給其他健康人。馬爾堡病毒的傳染性極強,症狀越重的患者傳染性越強,潛伏期患者的傳染性弱。人不是病毒自然循環中的一部分,只是偶然被感染。本病毒在自然界中的儲存宿主目前尚不清楚。
傳播途徑
 爾堡病毒
爾堡病毒主要經密切接觸傳播,即接觸病死動物和病人的屍體,以及感染動物和病人的血液、分泌物、排泄物、嘔吐物等,經黏膜和破損的皮膚傳播。在非洲疫區,因葬禮時接觸病人屍體,曾多次發生本病暴發。通過密切接觸也可以造成醫院感染和實驗室感染。此外,通過使用被污染的注射器等可造成醫源性傳播。有報導,病人在臨床康復3月內,仍可在精液中檢出馬爾堡病毒,因此,存在性傳播的可能性。通過含本病毒的氣溶膠感染實驗動物也有報導。
臨床表現
 馬爾堡病毒疫苗
馬爾堡病毒疫苗堡出血熱初期的病徵與其他傳染病如瘧疾、傷寒相似,因此有時斷症因難,特別是零星出現時。
馬爾堡的潛服期為3至9天。發病特徵是突然出現的發燒,頭痛,肌肉痛。一星期內,皮膚出現紅疹,然後有嘔吐、胸及腹痛,及腹瀉。之後病者可能出現黃膽,神志不清,肝衰竭,嚴重出血。患者復原過程十分漫長,並且經常出現陰囊收縮、復發肝炎、脊隨炎、眼睛、耳下腺感染等等後遺症。不同地區的醫療設備及支援對生還率影響很大,部分已開發國家出現時死亡率只有25%,但在開發中國家死亡率卻可以高達100%。
一般相信病毒是透過與染病的人畜緊密接觸,通過體液傳播。日常接觸相信不會傳染。病患者危急時,體內的病毒傳染力最強。部分非洲地區的殮葬風俗應該是導致疾病傳播的原因之一。
不少研究機構正嘗試研製對抗馬爾堡藥物及疫苗。2004年美國的研究人員已發現豚鼠注入不活躍的病毒後不會被感染。
發病機制
馬爾堡病毒進入人體後,首先侵犯樹突狀細胞和巨噬細胞,爾後被帶至區域淋巴結,在淋巴系統內播散,並通過血行感染肝、脾和其他組織。本病的發病機制主要包含以下兩方面:
1.病毒感染宿主細胞導致細胞的直接損傷:其機制是:病毒和細胞表面的凝集素結合,通過病毒蛋白的毒性作用導致細胞壞死。
2.病毒和機體免疫系統相互作用導致細胞的間接損傷:
其機制是:
1病毒由入侵部位擴散至各系統,從而抑制機體固有免疫應答,包括樹突狀細胞和巨噬細胞對1型干擾素的應答;
2由於病毒感染,樹突狀細胞對T細胞的活化受到部分抑制,從而影響體液免疫反應;
3在整個感染過程中產生大量淋巴細胞凋亡,導致免疫抑制;
4受感染的巨噬細胞產生各種介質,並通過各種途徑導致嚴重病變,如細胞表面表達組織因子引發播散性血管內凝血;細胞因子和趨化因子的釋放導致血管功能失調、低血壓和多臟器功能衰竭等。
病理改變
除橫紋肌、肺和骨骼之外,幾乎所有器官都可受損。其中肝、腎、淋巴組織的損害最為嚴重,腦、心、脾次之。肝、脾腫大,呈黑色。肝易破碎,切開時有多量血液流出,呈淺黃色。脾明顯充血,濾泡消失,髓質軟,呈粥糊樣,在紅色脾髓中可見大量巨噬細胞。紅髓壞死並伴淋巴組織破壞,脾小體內淋巴細胞明顯減少。肝細胞變性和壞死,常見透明變性。庫普弗細胞(枯否細胞)腫脹凸出,充滿細胞殘渣和紅細胞,竇狀隙充滿細胞碎屑。門靜脈間隙內單核細胞蓄積,但在肝壞死達到高峰時,可見肝細胞再生現象。淋巴組織的單核細胞變形。除了局限的出血和小動脈內膜炎外,肺內損害較少。神經系統的病變主要散布在腦神經膠質的各種成分,包括星狀細胞、小神經膠質細胞和少突膠質神經細胞等。神經膠質的損害有兩種,一是增生性,表現為膠質結節和玫瑰花狀形成。二是變性,表現為核固縮和核破裂。腦實質中可見多處出血。此外,還普遍存在腦水腫。
流行概況
馬爾堡病已發生過五次:1967年,德國和南斯拉夫, 31人(7人死亡),因接觸了來自烏干達的非洲綠猴而感染;1975年, 在南非診斷的3例中的死亡指示病例源於辛巴威;1980年,肯亞確 診了兩例,l例死亡;1982年,辛巴威發生1例;1987年,肯亞發生1例死亡。
埃波拉病最早於1976年在蘇丹的西部赤道省發現,距薩伊有500 英里;在鄉村醫院和村莊裡發現了600多病例;這些幾乎是同時爆發的 病死率約為70%。蘇丹的同一地區於1979年又發生第二次爆發。1994年,在象牙海岸,從一人和猩猩身上獲得另一不同的毒株。1995年,薩伊 發生一次大的爆發,病例集中在環Kitwit地區。在撒哈拉沙漠以南的非 洲其他幾個地區的居民中存在FA抗體,但是,它們同高毒力的埃波拉病毒的關係尚不清楚。
已經從1989和1990年從菲律賓進口到美國,1992年進口到義大利的 獼猴中分離到埃波拉相關的絲狀病毒;這些猴子很多死亡了。1989年裡 每天都和這些猴子接觸的五個管理員中,有四人產生了特異性抗體,他們先前未曾發熱或患過其它疾病。
形態特徵
在自然狀態下,馬爾堡病毒是多形態的,或呈長絲狀並且有時有分枝,或呈“U”形或“6”形或環形。以磷鎢酸負染後電鏡觀察,可見直徑約為80~90nm,長度130~2600nm不等的病毒粒子。外周有囊膜,表面有長約10nm的突起。
理化學特性
馬爾堡病毒含有一個單鏈負股RNA。對熱有中等程度的抵抗力,56℃不能完全將其滅活,60℃1小時感染性喪失。在室溫及4℃時存放35天其感染滴度基本不變,-70℃可以長期保存。紫外線,γ射線、脂溶劑、乙醚、β丙內脂、次氯酸和酚類等均可破壞病毒的感染性。
培養
馬爾堡病毒可在多種組織細胞內增殖,包括綠猴腎原代細胞、恆河猴腎細胞、人羊膜細胞、雞胚成纖維細胞、豚鼠成纖維細胞以及傳代細胞系Vero、BHK21、HeLa、ELF等,其中以VeroE6和Vero98最為敏感。感染細胞可出現細胞病變,如巨細胞的出現、嗜鹼性細胞漿內包涵體的形成等。
病原性
在實驗室條件下,猴、小鼠、豚鼠和倉鼠均可感染或發病。
豚鼠對馬爾堡病毒較為敏感。經腹腔、靜脈、皮內、皮下或鼻內等途徑人工接種病毒或高熱期患者血液,均可引起嚴重的發熱反應。但在最初幾代傳代時,動物無明顯的發病體徵和死亡,感染豚鼠在14~21天內產生特異性抗體。隨著在豚鼠體內傳代次數的增加,病毒對豚鼠的毒力增高,感染豚鼠大多死亡。病變可見肝、脾、肺和淋巴結內出現壞死性變化,並常見間質性肺炎和瀰漫性血管內凝血,肝細胞內有小型的嗜鹼性包涵體。
倉鼠的敏感性較低,病毒常常需要先在豚鼠體內多次傳代後,才能適應於倉鼠體內增殖並傳代。小鼠雖可感染但不發病。
猴在實驗室條件下經不同途徑和劑量接種均可感染髮病,包括非洲綠猴、獼猴和松鼠猴等。潛伏期2~6天,小劑量皮下接種可推遲至10天。發病早期,病猴體溫升高達413℃,但精神尚好,臨死前48小時表現厭食,聚堆,對外界剌激反應遲鈍,體重減輕等。在皮膚,尤其是臀部和股部皮膚上可見瘀點狀丘疹。發病後期,病猴呼吸困難,觸診可見肝腫大,瀕死期發生腹瀉,直腸和陰道黏膜出血,多在發病後6~13天死亡。
人類潛伏期為3~9天。發病急劇,初發症狀為全身疲乏,頭痛,發熱,畏寒,大量出汗,全身肌肉痛等,類似流感。隨後病人表現噁心,大量嘔吐,水樣腹瀉和瀰漫性腹痛,約持續7天。發病1~2天內,嘔吐物和糞便中含有大量血液。體溫在3~4天時達高峰,可達40℃以上,14天后開始下降,但經12~14天可再次升高。患病5~7天時出現皮疹,並從面部向軀幹及四肢擴展,起初為丘疹,24小時後發展為斑疹,並逐漸融合為暗紅色的斑疹,皮膚無癢感,一般持續3~4天后消退,隨後發生脫屑。上述皮膚損害為本病的特徵性症狀。皮疹出現的同時,病人呈現出血性傾向,如鼻衄、齒齦出血、尿血和陰道出血等,嚴重者可因發生休克而死亡,並伴有瀰漫性血管內凝血。
生態學
在首次發生本病的西德和南斯拉夫,患者共25名,他們都是製造小兒麻痹症弱毒疫苗的研究人員和工作人員,是在解剖非洲綠猴,直接接觸其內臟器官、血液以及處理使用過的器皿而被感染的。以後又發生6名患者,他們都是給予這些患者治療和護理的醫務人員,因接觸患者的血液或分泌物而發生感染。但經常接觸猴的飼養員卻極少發生感染,說明本病的傳播方式可能以直接接觸為主。
美國曾對非洲綠猴和黑猩猩的血清進行檢查,發現約有50%的血清含有1∶8~1∶25的補體結合抗體。
馬爾堡病毒可在蚊體內增殖,因此推測它們可能是自然界中猴類馬爾堡病的保有者和傳播媒介。
診斷
馬爾堡病毒屬於生物安全4級病原體,病毒分離培養和研究工作都必須在P4級實驗室內進行。 在急性病例,可取病人(猴)的急性期血液和尿,或死亡人(猴)的肝臟等病料,電鏡觀察病毒粒子,即可做出診斷。病毒的分離可取上述病料接種Vero細胞,3天后採用免疫螢光技術即可檢出細胞內的病毒抗原。也可將上述病料接種豚鼠、乳鼠或猴,動物發病後,可採用電鏡或免疫螢光技術檢查血液或組織器官中的病毒抗原。
血清診斷方法包括間接免疫螢光試驗、酶聯免疫吸附試驗和放射免疫測定技術等。間接免疫螢光試驗不僅檢出抗體時間早、水平高,而且可測定IgG和IgM兩類抗體。IgM抗體在發病後7天即可出現,並很快達到高峰,可用於疾病的早期診斷;而IgG抗體在感染後30天達到高峰,並持續較長時間。
防制
由於本病主要呈人人或猴人之間傳播,因此必須嚴格隔離患者,嚴密消毒,防止因接觸污染血液和分泌物或經醫療器械而發生感染。飼養和解剖可疑猴時,也要同樣採取嚴密的預防措施。
治療
一般支持治療
應臥床休息,就地隔離治療。給高熱量、適量維生素流食或半流食。
液體療法
補充足夠的液體和電解質,補液應以等滲液和鹽液為主,常用的有平衡鹽液和葡萄糖鹽水等。以保持水、電解質和酸鹼平衡。
恢復期病人血清治療
如給早期病人注射恢復期患者的血清,可能有效。
對症和併發症治療
有明顯出血者應輸新鮮血,以提供大量正常功能的血小板和凝血因子;血小板數明顯減少者,應輸血小板;對合併有彌散性血管內凝血者,可用肝素等抗凝藥物治療。心功能不全者套用強心藥物;腎性少尿者,可按急性腎功能衰竭處理:限制入液量,套用利尿劑,保持電解質和酸鹼平衡,必要時採取透析療法;肝功能受損者可給予保肝治療。重症病人可酌情套用抗生素預防感染。