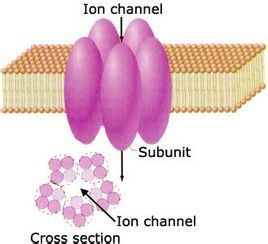
概述
活體細胞不停地進行新陳代謝活動,就必須不斷地與周圍環境進行物質交換,而細胞膜上的離子通道就是這種物質交換的重要途徑.人們已經知道,大多數對生命具有重要意義的物質都是水溶性的,如各種離子,糖類等,它們需要進入細胞,而生命活動中產生的水溶性廢物也要離開細胞,它們出入的通道就是細胞膜上的離子通道. 離子通道由細胞產生的特殊蛋白質構成,它們聚集起來並鑲嵌在細胞膜上,中間形成水分子占據的孔隙,這些孔隙就是水溶性物質快速進出細胞的通道.離子通道的活性,就是細胞通過離子通道的開放和關閉調節相應物質進出細胞速度的能力,對實現細胞各種功能具有重要意義.兩名德國科學家埃爾溫·內爾和貝爾特·扎克曼即因發現細胞內離子通道並開創膜片鉗技術而獲得1991年的諾貝爾生理學獎.
離子通道的主要類型
離子通道的開放和關閉,稱為門控(gating).根據門控機制的不同,將離子通道分為三大類:(1)電壓門控性(voltage gated),又稱電壓依賴性(voltage dependent)或電壓敏感性(voltage sensitive)離子通道:因膜電位變化而開啟和關閉,以最容易通過的離子命名,如K+、Na+、Ca2+、Cl-通道4種主要類型,各型又分若干亞型.(2)配體門控性(ligand gated),又稱化學門控性(chemical gated)離子通道:由遞質與通道蛋白質受體分子上的結合位點結合而開啟,以遞質受體命名,如乙醯膽鹼受體通道、谷氨酸受體通道、門冬氨酸受體通道等.非選擇性陽離子通道(non-selective cation channels)系由配體作用於相應受體而開放,同時允許Na+、Ca2+ 或K+ 通過,屬於該類.(3)機械門控性(mechanogated),又稱機械敏感性(mechanosensitive)離子通道:是一類感受細胞膜表面應力變化,實現胞外機械信號向胞內轉導的通道,根據通透性分為離子選擇性和非離子選擇性通道,根據功能作用分為張力激活型和張力失活型離子通道.此外,還有細胞器離子通道,如廣泛分布於哺乳動物細胞線粒體外膜上的電壓依賴性陰離子通道(voltage dependent anion channel,VDAC),位於細胞器肌質網(sarcoplasmic reticulum,SR)或內質網(endoplasmic reticulum,ER)膜上的ryanodine受體通道、IP3受體通道.
細胞膜表面受體的共同特點是由多亞基組成受體/離子通道複合體,除本身有信號接受部位外,又是離子通道,其跨膜信號轉導無需中間步驟,反應快,一般只需幾毫秒。分為二類,一類是配體(非電壓)依賴性複合體,另一類是電壓依賴性複合體。
配體依賴性離子通道
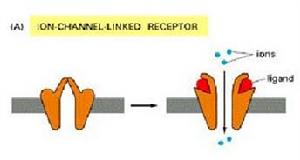 配體依賴性離子通道
配體依賴性離子通道配體依賴性離子通道常見於神經細胞和神經肌接頭處,屬於此類受體的有菸鹼型乙醯膽鹼受體(nAchR)、γ-氨基丁酸受體(GABAR)、甘氨酸受體等。它們都是由幾個亞基組成的寡聚體蛋白,除含有配體結合部位外,本身就是離子通道,籍此將信號傳入胞內。依賴於神經遞質的離子通道型受體屬於這類受體,它位於突觸後膜上,接受神經遞質刺激後,通道開放,導致離子跨膜流動,引起突觸後膜去極化或超極化,繼而產生生物效應。
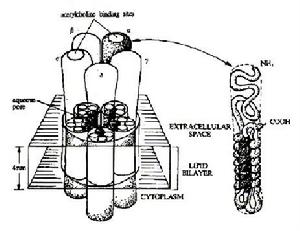 乙醯膽鹼受體
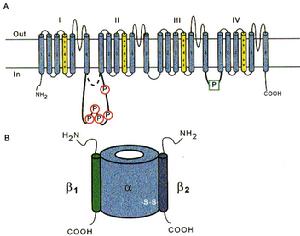
乙醯膽鹼受體nAchR是此類受體研究的比較清楚的一種。nAchR是由由5個同源性很高的亞基構組成的5聚體蛋白質,包括2個α亞基,1個β亞基,1個γ亞基的和1個δ亞基,中間位離子通道。每一個亞基都是一個四次跨膜蛋白,約由500個胺基酸殘基構成。推測跨膜部分為四條α螺鏇結構,其中一條α螺鏇含較多的極性胺基酸,就是由於這個親水區的存在,使五個亞基共同在膜中形成一個親水性的通道。乙醯膽鹼的結合部位是在兩個α亞基上,此亞基位於膜外側且具有糖基化部位。
乙醯膽鹼受體可以以三種構象存在。兩分子乙醯膽鹼的結合可以使之處於通道開放構象,但即使有乙醯膽鹼的結合,該受體處於通道開放構象狀態的時限仍十分短暫,在幾十毫微秒內又回到關閉狀態。然後乙醯膽鹼與之解離,受體則恢復到初始狀態,做好重新接受配體的準備。
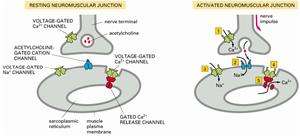 電壓依賴型離子通道
電壓依賴型離子通道電壓依賴型離子通道
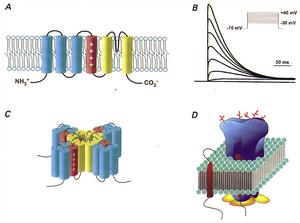
電壓依賴型受體/離子通道複合體的特點為它是單個大分子多肽,每個分子含有4個同源性重複序列,跨膜形成離子通道。每個重複序列單位含6個跨膜片段,其中第四個片段構成獨特性區域,規則排列的極性胺基酸序列被非極性胺基酸中斷,推測此部位代表電位感受器。二氫砒啶受體是這類複合體的代表,調節L型Ca2+慢通道。
離子通道的主要功能及研究方法
離子通道的主要功能有:(1)提高細胞內鈣濃度,從而觸發肌肉收縮、細胞興奮、腺體分泌、Ca2+依賴性離子通道開放和關閉、蛋白激酶的激活和基因表達的調節等一系列生理效應;(2)在神經、肌肉等興奮性細胞,Na+ 和Ca2+通道主要調控去極化,K+主要調控復極化和維持靜息電位,從而決定細胞的興奮性、不應性和傳導性;(3)調節血管平滑肌舒縮活動,其中有K+、Ca2+、Cl-通道和某些非選擇性陽離子通道參與;(4)參與突觸傳遞,其中有K+、Na+、Ca2+、Cl-通道和某些非選擇性陽離子通道參與;(5)維持細胞正常體積,在高滲環境中,離子通道和轉運系統激活使Na+、Cl-、有機溶液和水分進入細胞內而調節細胞體積增大;在低滲環境中,Na+、Cl-、有機溶液和水分流出細胞而調節細胞體積減少.
研究離子通道功能的最直接方法是用膜片鉗技術直接測定通過離子通道的電流或測量細胞膜電位的變化.膜片鉗技術是利用一個玻璃微吸管電極完成膜片或全細胞電位的監測、鉗制和膜電流的記錄,通過觀測膜電流的變化來分析通道個體或群體的分子活動、探討離子通道特性.分子生物學技術為離子通道的分子結構分析、基因克隆、功能表達研究提供了有力工具,對於編碼離子通道亞單位的基因結構可採用基因定位克隆確定其在染色體上的定位,用逆轉錄-聚合酶鏈反應、Northern雜交等明確其在器官組織中的分布,用Western雜交檢測基因表達產物等.螢光探針鈣圖像分析技術為檢測細胞內游離鈣離子濃度提供了有效手段,常用的螢光探針有Fura-2/AM、Indo-1/AM、Fluo-3/AM、Calcium Green等,常用的檢測儀器有雙波長顯微螢光光度計、雷射掃描共聚焦顯微鏡等,目前國外Olympus、Zeiss、Spex等公司已生產了測定細胞內游離鈣離子的顯微螢光裝置,國內自行研製的活細胞鈣離子濃度螢光顯微檢測系統也已問世。將離子濃度圖像記錄和膜片鉗記錄結合,同時進行光電聯合檢測,從離子產生的離子濃度、圖像變化和電信號變化多個方面研究離子通道,將獲得更多的離子通道功能信息.
類型和功能特徵
離子通道依據其活化的方式不同,可分兩類:一類是電壓活化的通道,即通道的開放受膜電位的控制,如Na+、Ca+、Cl-和一些類型的K+通道;另一類是化學物活化的通道,即靠化學物與膜上受體相互作用而活化的通道,如 Ach受體通道、胺基酸受體通道、Ca+活化的K+通道等。
鈉通道
 鈉通道
鈉通道各種生物材料中,與電興奮相關的Na+通道有相似的基本特徵。通道活化時間常數小於1毫秒,失活時間常數為數毫秒,Na+電流的反轉電位約+55毫伏。單通道電流記錄顯示,Na+單通道電導為4~20pS,平均開放壽命數毫秒。
根據一些藥物和毒素對Na+通道功能的不同影響,可分為4種類型:①通道阻斷劑,如河豚毒素(TTX)、石房蛤毒素(STX)。②通道活化增強劑,如β-蠍毒、箭毒蛙毒素(BTX)、藜蘆鹼毒素(VER)等。③通道活化抑制劑,如一些局部麻醉劑及其衍生物。④通道失活抑制劑,如鏈霉蛋白酶、N-溴乙醯胺(NBA)等。
鈣通道
Ca2+通道廣泛存在於各種生物組織的細胞膜中。巨觀的Ca2+電流動力學特徵與Na2+電流相似,但峰值小且失活過程慢,可達數十到數百毫秒。Ca2+通道對Ca2+、Ba2+、Sr2+都有高通透性,但Ni2+、Cd2+、Co2+、Mn2+等離子能有效地阻斷Ca2+通道。藥物對Ca2+通道的作用可分為:①通道阻斷或抑制劑,可分為苯烷基胺類(如異博定、甲基異博定D600)、苯硫氮類、雙氫吡啶類等類型。②通道激活劑,一些雙氫吡啶化合物如BayK8644等藥物可活化Ca2+通道。近年,對小雞背根神經節細胞的研究發現有3種類型的Ca2+通道:①L型,該種通道在膜電位大於-20毫伏時活化,電流失活緩慢。單通道電導約25pS。②T型,膜電位約-60毫伏時通道即活化,-10毫伏以上通道電流幅值反而下降,單通道電導約8pS。③N型,該種通道在膜電位不小於-10毫伏才能活化,但又必須超極化到-80毫伏以下才能克服通道的失活。電流動力學比 L型快但比T型慢,單通道電導約13pS。以上3類Ca2+通道在不同細胞膜上選擇性分布及密度的差別,將影響各種細胞的生理功能。Ca2+通道除了對細胞電興奮性有貢獻外,它通過調節細胞內Ca2+濃度,可進一步調節許多細胞功能。
 鉀通道
鉀通道鉀通道
根據功能特性的不同,K+通道可分為以下類型:①慢(延遲)K+通道(K通道),也就是H-H模型中的K+通道。單通道電流記錄顯示,單個K通道電導在2~20pS,通道平均開放壽命為數十毫秒。該種通道可被四乙胺(TEA)等特異性阻斷,通道對K+有高度選擇性,這種通道在神經軸突和骨骼肌細胞膜中有較高密度。②快(早期)K+通道(A通道),該種通道外向的K+流在膜去極化的早期就出現,表明通道的活化時間常數比慢K+通道小得多,但在-40毫伏以上該通道即關閉。電壓鉗位實驗表明,其巨觀電流動力學與Na+電流相似。較低濃度的4-氨基吡啶即能阻斷該通道,它也可被四乙胺阻斷。③Ca2+活化的K+通道,該種通道的開放,不但與膜電位有關,而且依賴於細胞內Ca2+的濃度,每個通道需結合兩個Ca2+才能活化。單通道電導可高達300pS,並有較長的開放壽命,這種通道與Ca2+通道協同作用,對調節細胞膜電興奮性的節律有重要意義。它可被四乙胺、N'-四乙酸(EGTA)、奎尼丁和Ba2+阻斷。④內向整流的K+通道,其特徵是:在膜超極化時通道開放與膜電位和胞外K+濃度密切相關,通道開放時產生內向K+電流,單通道電導在5~10pS範圍。
離子通道病
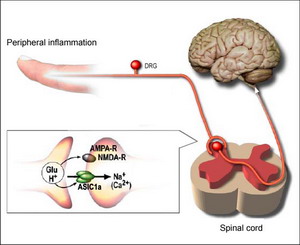
離子通道病是指離子通道的結構或功能異常所引起的疾病,具體表現在編碼離子通道亞單位的基因發生突變或表達異常,或體內出現針對通道的病理性內源性物質時,離子通道的功能發生不同程度的減弱或增強,導致機體整體生理功能紊亂,形成某些先天性或後天獲得性疾病,主要累及神經、肌肉、心臟、腎臟等系統和器官.迄今為止,研究比較清楚的離子通道病主要涉及鉀、鈉、鈣、氯通道領域,現簡介如下:
 離子通道病
離子通道病鉀通道病 鉀離子通道在所有可興奮性和非興奮性細胞的重要信號傳導過程中具有重要作用,其家族成員在調節神經遞質釋放、心率、胰島素分泌、神經細胞分泌、上皮細胞電傳導、骨骼肌收縮、細胞容積等方面發揮重要作用.已經發現的鉀通道病有常染色體顯性良性家族性新生兒驚厥(benign familial neonatal convulsions,BFNC)、1-型發作性共濟失調(episodic ataxia type 1)、陣發性舞蹈手足徐動症伴發作性共濟失調(paroxysmal choreoathetosis with episodic ataxia)、癲癇、1-,2-,5-,6-型長QT綜合徵、Jervell和Lange-nielsen綜合徵、Andersen綜合徵等.
鈉通道病 鈉離子通道在大多數興奮細胞動作電位的起始階段起重要作用,已經發現的鈉通道病有高鉀型周期性麻痹、正常血鉀型周期性麻痹、部分低鉀型周期性麻痹、先天性副肌強直、各型鉀加重的肌強直、先天性肌無力、3-型長QT綜合徵、1-型假性醛固酮減少症、Liddle綜合徵、全面性癲癇熱性發作疊加症(generalized epilepsy with febrile seizures plus)等
鈣通道病:鈣離子通道廣泛存在於機體的不同類型組織細胞中,參與神經、肌肉、分泌、生殖等系統的生理過程.已經發現的鈣通道病有家族性偏癱型偏頭痛、低鉀型周期性癱瘓、2-型發作性共濟失調、6-型脊髓小腦共濟失調、中央脊髓性肌病(central core disease of muscle)、惡性高熱、Lambert-Eaton肌無力綜合徵癲癇等.
氯通道病:氯離子通道廣泛分布於機體的興奮性細胞和非興奮性細胞膜及溶酶體、線粒體、內質網等細胞器的質膜,在細胞興奮性調節、跨上皮物質轉運、細胞容積調節和細胞器酸化等方面具有重要作用.已經發現的氯通道病有先天性肌強直(Thomsen型)、隱性遺傳全身性肌強直(Becker型)、囊性纖維化病、遺傳性腎結石病、3-型Bartter綜合徵等.
需要說明的是,相當數量的離子通道病並不是新出現的疾病,而是早已出現甚至早被熟知的疾病,只是此前一直未發現其在離子通道水平存在病變,如癲癇、偏頭痛等;有些離子通道病為單一離子通道結構或功能異常而至,如1-型發作性共濟失調是由於KCNA1基因突變引起,該基因位於染色體12p13上,編碼電壓依賴性鉀離子通道;也有些離子通道病涉及多種離子通道結構或功能異常,如癲癇與L型電壓依賴性鈣通道(a1 D亞單位基因表達減弱)、電壓依賴性鉀通道(KCNQ2和KCNQ3基因突變)、乙醯膽鹼受體通道(a4和b2亞單位基因突變)等有關.