概述
2干擾及其消除
影響測定結果,故在回流前向水樣中加入 硫酸汞,使成為絡合物以消除干擾。 氯離子含量高於2000mg/L的樣品應先作定量稀釋、使含量降低至2000mg/L,再行測定。
3方法的適用範圍
用0.25mol/L濃度的重鉻酸鉀溶液可測定大於50mg/L的COD值。用0.025mol/L濃度的重鉻酸鉀溶液可測定5—50mg/L的COD值,但準確度較差。未經稀釋的水樣的測定上限是700mg/L。
4測定過程
取水樣20mL(原樣或經稀釋)於錐形瓶中
加入HgSO₄ 0.4g(消除CL離子干擾)混勻
加入0.25mol/L 重鉻酸鉀 10mL 和沸石若干 混勻接上回流 裝置
從冷凝管上口加入 AgSO₄-H₂SO₄溶液30mL ( 催化劑)混勻
回流加熱2小時
冷卻30分鐘
從冷凝管上口加入80mL水於反應液中
取下錐形瓶
加入鐵靈試劑3滴
此時溶液應呈黃色(既過量重鉻酸鉀中 六價鉻顏色)
用0.1mol/L 硫酸亞鐵銨 標準溶液 滴定 此時溶液顏色逐漸變成藍綠色(既 六價鉻被亞鐵試劑還原成 三價鉻的顏色)
繼續滴定至溶液呈現紅棕色停止 (此時水樣中重鉻酸鉀全部被還原 亞鐵離子和亞鐵試劑產生紅棕色)記錄 硫酸亞鐵銨溶液的用量V₁mL。
以 蒸餾水為空白水樣,同上法測定 硫酸亞鐵銨溶液的用量Vο mL。
按下面公式計算CODcr值:
CODcr(O₂,mL/L)=(Vο-V₁)*c*8*1000/V
V表示水樣體積mL,c表示 硫酸亞鐵銨溶液濃度mol/L,8表示氧的摩爾質量g/mol,*號表示乘以
儀器
(1)回流裝置:帶250ml錐形瓶的全玻璃回流裝置(如取樣量在30ml以上,採用500ml錐形瓶的全玻璃回流裝置)。
(2)加熱裝置:電熱板或變組電爐。
(3)50ml酸式滴定劑。
試劑
(1) 重鉻酸鉀標準溶液(1/6 =0.2500mol/L:)稱取
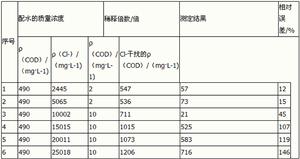 重鉻酸鉀法測定高濃度Cl-廢水COD誤差
重鉻酸鉀法測定高濃度Cl-廢水COD誤差預先在120℃烘乾2h的基準或優級純重鉻酸鉀12.258g溶於水中,移入1000ml容量瓶,稀釋至標線,搖勻。
(2) 試亞鐵靈指示液:稱取1.485g鄰菲囉啉,0.695g硫酸亞鐵溶於水中,稀釋至100ml,貯於棕色瓶內。
(3) 硫酸亞鐵銨標準溶液:稱取39.5g硫酸亞鐵銨溶於水,邊攪拌邊緩慢加入20ml濃硫酸,冷卻後移入1000ml容量瓶中,加水稀釋至標線,搖勻。臨用前用重鉻酸鉀標準溶液標定。
(4)硫酸-硫酸銀溶液:與2500ml濃硫酸中加入25g硫酸銀。放置1-2d,不時搖動使其溶解(如無2500ml容器,可在500ml濃硫酸中加入5g硫酸銀)。
(5)硫酸汞:結晶或粉末。
注意事項
(1)使用0.4g 硫酸汞絡合 氯離子的最高量可達40mL,如取用20.00mL水樣,即最高可絡合2000mg/L氯離子濃度的水樣。若 氯離子濃度較低,亦可少加 硫酸汞,保持硫酸汞:氯離子=10:1(W/W)。如出現少量 氯化汞沉澱,並不影響測定。
(2)水樣去用體積可在10.00-50.00mL範圍之間,但試劑用量及濃度按相應調整,可得到滿意結果。
(3)對於 化學需氧量小於50ml/L的水樣,應該為0.0250mol/L重鉻酸鉀 標準溶液。回滴時用0.01mol/L硫酸亞鐵銨標準溶液。
(4)水樣加熱回流後,溶液中重鉻酸鉀剩餘量應為加入量的1/5-4/5為宜。
(5)用 鄰苯二甲酸氫鉀標準溶液檢測 試劑的質量和操作技術時,由於每克鄰苯二甲酸氫鉀的理論CODCr為1.176g,所以溶解0.4251L鄰苯二甲酸氫鉀與重 蒸餾水中,轉入1000mL容量瓶,用重蒸餾水稀釋至標線,使之成為500mg/L的CODcr標準溶液。用時新配。
(6)CODcr的測定結果應保留三位 有效數字。
(7)每次實驗時,應對 硫酸亞鐵銨標準 滴定溶液進行標定,室溫較高時尤其注意其濃度的變化。

