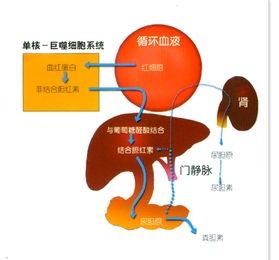
概述
藥物在體內的排泄主要是通過腎臟、膽汁和乳腺等渠道進行的。藥物經肝轉化,可以代謝物或以原形分泌進入膽汁,經膽總管排入十二指腸,其中一部分被小腸重吸收,由門靜脈回流入肝,然後再經膽汁排入腸腔。如此往復,就形成肝腸循環。
肝腸循環的意義決定於藥物在膽汁的排出率。膽汁排出量多時,肝腸循環能延長藥物的作用時間,如果能阻斷該藥物的肝腸循環,則能加速該藥物的排泄。
過程
化學循環
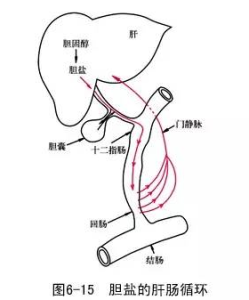 肝腸循環
肝腸循環生物循環
藥物及其代謝產物經膽汁排泄往往是主動過程,有酸性、鹼性及中性三個主動過程排泄通道。某些藥物,尤其是膽汁排泄後的藥物經膽汁排入十二指腸後部分藥物可再經小腸上皮細胞被重新吸收,在藥動學上表現為藥時曲線出現雙峰現象,而在藥效學上表現為藥物的作用明顯延長。也有些結合性代謝物經膽汁排入腸道後,水解釋放出原型藥物,會再次吸收形成肝腸循環。洋地黃毒苷26%經膽汁排入腸內形成肝腸循環,只是該藥作用持久的原因之一。經乳汁排出的藥物如嗎啡、阿托品、麥角生物鹼等可能引起乳兒中毒。
發生機制
通過肝腸循環(enterohepaticcirculation,EHC)排泄的物質主要包括藥物、內源性物質和毒物等,其中具有EHC現象的藥物有阿托伐他汀類、秋水仙鹼等,內源性物質有膽汁酸和膽色素等,毒性物質有T-2毒素等化合物。對於藥物而言,在排泄時可重新被吸收,從而使藥物的藥時曲線出現雙峰或多峰的現象,不僅提高了藥物的生物利用度,還可使藥物之間發生相互作用。但對於內源性物質和毒性物質來說,EHC過程的存在對人體是非常有害的。
1.膽汁酸的EHC機制研究
膽汁酸的EHC對於機體脂質的消化至關重要。人體每天從外界攝取的脂質需要15~32g的膽汁酸來消化,但是肝臟每天只能合成0.4~0.6g的膽汁酸,所以機體需要通過EHC使排泄的膽汁酸再度被吸收利用,這就是膽汁酸的EHC。它的生理學過程主要是膽汁酸通過肝細胞的主動分泌,隨膽汁進入膽囊,再由膽囊進入腸道發揮它的消化功能,然後在迴腸末端通過主動吸收或被動運輸的方式經門靜脈回到肝臟,在肝細胞內進行加工轉化,然後同新合成的膽汁酸一起又被分泌入小腸。膽汁酸的這種EHC過程每天會循環4~12次,大約有95%的膽汁酸被回吸利用。如果膽汁酸的EHC遭到破壞,不僅會影響體內脂類的消化吸收,也會使機體形成膽固醇結石。有學者發現,膽汁酸EHC的分子機制主要是轉運體運輸、結合蛋白的結合,例如頂端鈉依賴性膽酸轉運體在腸道的運輸。膽汁酸在腸道的重吸收包括游離膽汁酸在小腸近端的被動擴散和結合膽汁酸在小腸遠端的主動吸收,其中後一種方式是小腸膽汁酸重吸收的主要方式。迴腸膽汁酸結合蛋白是迴腸上皮細胞胞內膽酸結合蛋白,負責與膽汁酸分解後的膽鹽結合,然後是鈉依賴性膽酸轉運體的運輸作用。而在肝臟首先是鈉鹽牛磺膽酸共轉運蛋白的吸收,再者是膽鹽轉運蛋白膽鹽輸出泵的分泌;如果轉運體被抑制,那么膽汁酸的EHC過程就會終止,這些發現對高脂血症和動脈粥樣硬化形成機制的研究均具有重要意義。近年來,有學者提出,膽汁酸的EHC對小腸消化間期移行性複合肌電活動(MMC)也有影響,尤其是對十二指腸起源的MMC影響更大。MMC是指在禁食的情況下小腸發生運動與靜止有節律的一種肌電活動。研究認為,MMC出現主要受腸神經系統和胃腸激素的調控,在機體健康時,胃腸的這種MMC運動呈現出明顯的規律性,而當膽汁酸的EHC被破壞後(如膽管梗阻時),尤其是在早期十二指腸起源的MMC則完全消失。但也有研究認為,EHC對MMC並無特殊作用。
2.膽紅素的EHC機制研究
機體內80%以上膽紅素的來源是衰老紅細胞血紅蛋白的釋放。健康成年人每天約6g的血紅蛋白轉化成膽紅素通過肝臟排泄,在排泄過程中,膽紅素與其他物質結合生成膽紅素酯(如膽紅素甘氨酸酯、膽紅素牛磺酸酯等),酯型膽紅素又稱為非結合膽紅素,不溶於水,所以不能通過腎小球濾出隨尿液排出體外。這種非結合膽紅素在肝臟轉化生成的葡萄糖醛酸膽紅素稱為結合膽紅素,隨膽汁排泄至腸道內,在腸道內細菌的作用下,在迴腸末端被水解而分離又形成非結合膽紅素,一部分又被腸道吸收,形成膽紅素的EHC。另外一部分腸道內的非結合膽紅素經細菌分解為膽素原。人體每天有40~280mg的膽素原從糞便排出,稱為糞膽素原,在空氣中氧化為糞膽素(糞便的主要顏色),但還有一部分膽素原被腸黏膜重吸收回血液,經腎臟隨尿液排出,稱為尿膽素原,經空氣氧化為尿膽素(尿液的主要顏色),經門靜脈入肝,進入肝臟的膽素原大部分又以原形排入膽管,構成膽素原的EHC。
3.藥物的EHC研究
藥物在體內的吸收和排泄同樣具有EHC現象。經肝細胞排泄的藥物分泌到膽汁中,並與葡萄糖醛酸結合形成的代謝產物進入腸道後被腸道內的菌群水解為原型藥物,在迴腸末端又被重吸收到門靜脈進入全身循環,形成藥物的血藥濃度-時間曲線呈現出雙峰或多峰現象。所以藥物的EHC可減少藥物的排泄,並增加利用程度,這種現象對於醫師臨床用藥量的控制非常重要。在EHC過程中,藥物從血液至肝臟,再從肝臟到腸道以及從腸道重吸收的過程均是由轉運體介導來完成的,不同的過程有不同的轉運體來完成,並發揮著各自的作用。在肝細胞對物質的攝取及排泄過程中,有機陰離子轉運多肽B1、有機陰離子轉運多肽B3和多藥耐藥相關蛋白2發揮著重要作用。有機陰離子轉運多肽B1和有機陰離子轉運多肽B3負責肝臟對物質的攝取作用,包括內源性物質膽汁酸鹽、膽紅素、三碘甲狀腺素原氨酸、甲狀腺素以及各種藥物(如他汀類、降糖藥、抗腫瘤藥和免疫抑制藥等)。多藥耐藥相關蛋白2主要介導肝細胞對物質(如與葡萄糖醛酸結合的膽紅素及藥物活性物質)的排泄。藥物在腸道的吸收與排泄同樣是由轉運體介導完成的,例如,P-糖蛋白、乳腺癌耐藥蛋白和多藥耐藥相關蛋白等作為排出型轉運體,主要把吸收入血中的物質重新排泄到腸道中,從而減少藥物的吸收。H/寡肽共轉運體、有機陰離子轉運體、有機陽離子轉運體和有機陽離子/肉毒鹼轉運體等作為攝取型轉運體,主要起到腸道的重吸收作用。隨著對基因多態性研究的深入,有學者發現,轉運體主要受基因多態性的影響,個體基因型不同,所具有的轉運體對物質的轉運程度就不同,而每種藥物在體內吸收及排泄量也是不同的。這對EHC的過程及個體化治療方案的制訂均具有重要意義。
4.毒物的EHC研究
作為對機體有害的毒性物質同樣具有EHC過程,如重金屬鉛離子、有機鹵族化合物等。由於毒性物質的EHC對機體是有害的,因此可阻斷其EHC過程,降低其重吸收,以減少對機體的損害。肖平等通過研究活性炭製劑驅鉛的過程,發現吸附劑能顯著降低動物體內鉛水平,藉此可開發套用於鉛中毒的臨床治療。有機鹵族化合物進入機體後主要儲存於脂肪組織,通過膽汁和非膽汁途徑分泌到腸道,其中大部分因EHC而被重吸收入體內,由於有機鹵族化合物對人體有致畸形、致癌變和致突變的作用,因此亦可通過阻斷其EHC過程以減少其對機體的損害。
所致疾病的防治
1.高膽固醇血症和膽固醇結石的防治
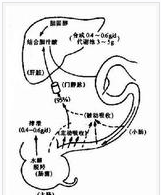 肝腸循環
肝腸循環2.黃疸的防治
膽紅素的代謝與EHC有著密切的關係,尤其表現為新生兒黃疸。由於新生兒膽紅素的EHC發育不成熟以及新生兒葡萄糖醛酸轉移酶活性低下,容易導致高膽紅素血症。因此,對於新生兒病理性黃疸,一方面要利用膽紅素的EHC加強排泄,減少重吸收,另一方面要加強肝細胞的轉運。文獻報導,採用雙歧桿菌製劑增加膽紅素的排泄治療新生兒高膽紅素血症取得了滿意的療效。
3.肝臟疾病的防治
研究者發現,正常情況下肝臟能滅活來自腸道的各種毒素、細菌、真菌等。當肝臟發生疾病時,腸道微生態會顯著變化,大量的毒素、細菌等進入血液無法被清除,導致腸道屏障功能受損,從而激活機體免疫系統,引起異常免疫反應,加快肝細胞凋亡、壞死。在腸黏膜屏障功能受損、腸道通透性增加以及腸菌群過度生長的情況下,這些細菌及產物會大量通過門靜脈系統進入肝臟,激活肝臟的非特異性免疫系統,產生大量的炎性細胞因子和趨化因子,引起或加重肝臟的炎症反應,甚至導致肝硬化、肝癌的發生。鑒於腸道菌群的EHC在肝臟疾病中的特殊作用,益生菌正成為治療肝臟疾病的新途徑。
研究
由於肝腸循環(EHC)屬於微觀的範疇,是西方醫學近代以來才發現的一種生理及病理現象,所以祖國醫學沒有這方面的文獻記載。但對於EHC的生物學功能,中醫學家很早提出了自己的觀點,即肝脾相關理論。目前大多數醫家都認可中醫的“脾”就是現代醫學中的“腸”。而中醫肝脾相關理論最早源自於《黃帝內經》,如《素問·寶命全形論篇》曰:“土得木而達”。生理上,肝和脾有著密切的聯繫:在飲食物的消化吸收方面表現在肝主疏泄和脾主運化的配合。《素問·靈蘭秘典論篇》言:“脾胃者,倉廩之官,五味出焉”;“小腸者,受盛之官,化物出焉”,認為胃和小腸完成食物的攝入和吸收。《素問·經脈別論》雲:“飲入於胃,游溢精氣,……五經並行”,認為脾完成飲食物的具體運輸和利用。《格致餘論》曰:“主閉藏者腎也,司疏泄者肝也”,提出肝可助脾胃運化;在氣血運行方面,表現在肝藏血與脾統血之間的密切配合。而在病理上,首先表現在木旺乘土,《素問·玉機真髒論》說:“五臟受氣於其所生,傳之於其所勝……”,另外還有土壅木郁;《素問·氣厥論》雲:“脾移熱於肝,則為驚衄”等都是五行相剋理論的具體體現。肝脾在生理與病理上的密切聯繫體現了現代醫學中EHC中肝與腸之間的關係,在生理上,脾主運化水谷即食物的消化吸收,肝主疏泄,肝之餘氣泄於膽助食物消化;在病理上,表現為肝病傳脾、脾病傳肝,對應於臨床上肝病時內毒素血症產生。現代中醫也對肝、脾的實質作了一定的研究,肝主疏泄不僅與現代醫學消化有關,還與內分泌功能有密切關係,脾主運化也與內分泌、免疫、神經系統有密切的關係。根據肝脾相關理論,有人認為,便秘、泄瀉大多是由肝膽疏泄功能異常引起的。
依據中醫肝脾相關理論,對於肝臟疾病的治療可從脾論治。有學者認為,肝硬化早期為脾虛,實脾為主要治則;肝硬化晚期出現腹水則是虛實夾雜之證,應靈活運用攻逐水飲、補氣健脾、滋養肝陰等方法治療。另外,“下法”也是治療肝病的有效策略,通過影響腸-肝軸,阻斷重吸收對機體有毒的物質。下法可清除彌散在胃腸道的毒性物質,影響腸-肝軸,從而有效阻斷EHC。對於黃疸的中醫治療,《金匱要略·黃疸篇》認為:“然黃家所得,從濕得之,……當下之。”
展望
雖然現代醫學對肝腸循環(EHC)的發生機制進行了相當多的研究,並取得了一定的成就,但對由於EHC作用所致疾病的防治還有諸多不足。而中醫學對EHC的臨床及試驗研究還處於比較淺顯的階段,臨床上“下法”及“通因通用”的運用及肝脾相關理論在肝臟疾病EHC過程中重要作用的探討還遠未達到臨床的套用要求。如果將肝脾相關理論較好地套用到EHC的研究中去,將有可能使人們對肝臟疾病的認識提高到一個新的層面。
意義
使有限的膽汁酸重複利用,促進脂類的消化與吸收。