簡介
中文名稱:羥汞化反應
英文名稱:hydroxy-mercury reaction
碳的不飽和鍵(包括雙鍵和三鍵)與汞鹽加成生成有機汞化合物的反應。
例如:醋酸汞溶液和烯烴經環汞化、反式開環兩步反應,生成有機金屬化合物,反應方程式如下所示:
CH=CH2+(CHCOO)Hg+HO→HO-CH-CH-HgOCOCH
炔烴和水的加成常常用汞鹽做催化劑。例如,乙炔和水的加成是在10%硫酸和5%硫酸汞水溶液中發生的。
水先與三鍵加成,生成一個很不穩定的加成物——乙烯醇(羥基直接和雙鍵碳原子相連的化合物稱為烯醇),乙烯醇很快發生異構化,形成穩定的羰基化合物。實驗證據顯示:炔烴和水加成的中間產物都有汞,因此有一種可能的機理如下式所示:
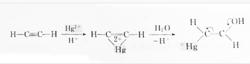 炔烴發生羥汞化反應機理1
炔烴發生羥汞化反應機理1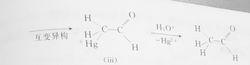 炔烴發生羥汞化反應機理2
炔烴發生羥汞化反應機理2在反應中,催化劑汞離子先和三鍵形成環狀π絡合物(i),然後水分子進攻碳原子,並失去一個質子,生成烯醇式金屬化合物(ii),進一步反應形成α碳原子上帶有汞的酮式化合物(iii),經過酸水解得到最終產物。
加在雙鍵碳原子上的基團除了 汞以外還有溶劑分子,溶劑為水則引入羥基,為甲醇則引入甲氧基,為乙酸則引入CH3COO基。
若與硼氫化鈉反應,金屬化合物中的碳汞鍵(C-Hg)被還原為碳氫鍵(C-H),得到醇、醚和酯該反應條件溫和,產率高。
在不對稱烯烴的羥汞化反應中,主要生成符合馬氏原則的產物,汞加在雙鍵上烷基較少的碳原子上(由碳正離子中間體的穩定性決定,但不發生重排),主要得到反應加成產物,屬於親電加成反應。
反應歷程為形成三元環狀過渡態,脫氫的產物。
特點
1.反應較快(羥汞化反應一般只需要幾分鐘)。
2.產率較高(>90%)。
3.易操作,條件溫和,Hg易處理(通過還原反應脫去)。
4.區域選擇性好(馬氏取向)。
5.無重排產物。
6.非立體專一(加成順式與反式兼具)。
套用
是實驗室製備醇的一種方法。由於汞及其可溶性鹽溶液均有毒,因此羥汞化反應的套用受到限制。
羥汞化反應不只局限於烯烴和水的反應,如果用炔烴代替烯烴也能經反應產生酮,再由互變異構體之間的轉換成烯醇,最後行羥汞化反應產生醇類。如果用醇代替水,反應後就會產生醚類。這兩者一樣遵守馬爾科夫尼科夫規則。
在醇存在下,使用乙烯基醚能使烷氧基(RO-)從醇轉換成醚。羥汞化反應下,烯丙基醇與乙烯基醚可以得到R–CH=CH–CH–O–CH=CH,這是適於克萊森重排反應。
機制
第一步,烯烴的雙鍵對乙酸汞進行親核進攻,使一個乙酸負離子離去,隨後汞原子上的孤對電子對攻擊雙鍵上的一個碳,形成汞鎓正離子中間體。在形成該中間體的過程中,烯烴HOMO軌道上的電子對填入汞原子的空dz軌道而汞原子dxy軌道上的電子對填入烯烴LUMO軌道。
第二步,作為親核試劑的水分子攻擊多取代的碳,使碳-汞鍵異裂,鍵對電子轉移給汞原子,使後者恢復中性。此時氧原子帶正電荷。
第三步,在第一步中生成的乙酸負離子拿走氧原子上的氫,形成副產物乙酸,並且產生最終產物-醇類。
立體選擇性與立體化學
羥汞化反應具有相當強的立體選擇性且遵從馬爾科夫尼科夫規則;排除極端例子,水當親核試劑時會攻擊有較多取代基的碳,並接上羥基,這解釋了機制第一步產物之一的汞一價陽離子形成的三個共振結構。通過觀察這些結構可以看出,帶正電汞原子有時會駐留在取代多的碳上(約4%),這形成了暫時性的三級碳陽離子,為反應性很高的親電子試劑,而親核試劑也在此時攻擊汞陽離子。
在立體化學上,羥汞化反應是屬於反式加成反應,如圖所示第二步中,親核試劑不能攻擊和汞離子相同的面上的碳因為有立體障礙,分子的片上根本沒有足夠的空間同時容納汞離子和親核試劑,因此,當其無法自由轉動,羥基和醋酸汞基將總是彼此成反式
以為環己烯的羥汞化反應為例,有一個龐大的基團像三級丁基鎖定環的椅式構象,並防止環翻轉。 4-叔丁基-環己烯羥汞化反應產生兩種產物:在雙鍵的加成反應上總是呈反式,但羥基和丁基就順反比例差不多了,醋酸汞基有和三級丁基稍微偏好呈反式,因此最後羥基和三級丁基呈順式的較多一點。而 1-甲基4-叔丁基-環己烯羥汞化反應只有一種產物,除了在雙鍵加成上總是反式,水也只攻擊取代基較多的碳。反式加成的原因,是因為水的孤對電子軌域重疊的最大化與在反面的醋酸汞的汞陽離子空電子軌域。在立體選擇性來看,水比較偏好攻擊有較多取代基的碳,但水無法在雙鍵上行順式加成,這代表在過渡狀態有利於水從醋酸汞組的相對側上的攻擊。
羥汞化還原反應
在實踐上,由羥汞化反應產生的汞加成產物幾乎總是用硼氫化鈉(NaBH)在鹼水溶液中行 脫汞反應。在脫汞反應中,醋酸汞基會被氫給取代掉,屬於還原脫去反應。羥汞化反應結束後就接著脫汞反應,此兩者合稱羥汞化還原反應。
羥汞化還原反應整體淨反應就是在雙鍵上進行水的加成。所有建立在羥汞化反應的立體化學結構問題上,都會受到脫汞反應的干擾,因此氫和氫氧根彼此可能為順式或反式。羥汞化還原反應是一種流行的實驗室技術來在馬氏選擇性下進行烯烴的水合反應,同時可避免碳陽離子中間體,因為這可能導致重排產生複雜的產物。
拓展
烯烴羥汞化反應機理的探討:從軟硬酸鹼理論、電負性等基本概念出發,結合量子化學計算結果,對烯烴的羥汞化機理進行了深入分析,指出烯烴的羥汞化屬於親核加成,而不是多數教材中認為的親電加成。通過對碳汞鍵的極性分析,對烯烴和炔烴羥汞化脫汞難易給予了合理解釋。
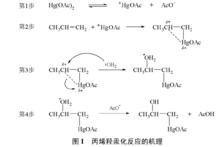 丙烯羥汞化機理
丙烯羥汞化機理