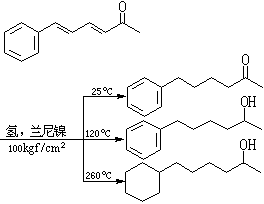
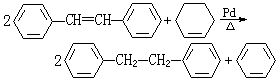催化氫化反應
定義
在催化劑的作用下,氫分子加成到有機化合物的不飽和基團上的反應,例如: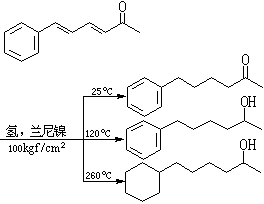
幾乎所有的不飽和基團都可以直接加氫成為飽和基團,
其從易到難的順序大致為:醯氯、硝基、炔、醛、烯、酮、腈、多核芳香環、酯和取代醯胺、苯環。各種不飽和基團對於催化氫化的活性次序與催化劑的品種和反應條件有關。
催化劑
催化氫化的關鍵是催化劑。
它們大致分為兩類:①低壓氫化催化劑,主要是高活性的蘭尼鎳、鉑、鈀和銠,低壓氫化可在 1~4 個大氣壓和較低的溫度下進行;②高壓氫化催化劑,主要是一般活性的蘭尼鎳和亞鉻酸銅等。高壓氫化通常在100~300個大氣壓和較高的溫度下進行。鎳催化劑套用最廣泛,有蘭尼鎳、硼化鎳等各種類型。貴金屬鉑和鈀催化劑的特點是催化活性高,其用量可比鎳催化劑少得多。用鉑作催化劑時,大多數烯鍵可在低於100℃和常壓的條件下還原:
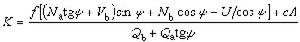
近年來新發展的均相催化劑主要是銠、釕和銥的帶有各種配位基的絡合物,這些絡合物能溶於有機相,故稱為均相催化劑。較好的均相催化劑有:氯化三 (三苯基膦)合銠【(Ph3P)3·RhCl】、氯氫化三(三苯基膦)合釕【(Ph3P)3·RuClH】、氫化三(三苯基膦)合銥【(Ph3P)3·IrH】等,上述分子式中Ph為苯基。均相催化劑的優點是催化活性較高,不會由於雜質(例如有機硫化合物等)的存在而喪失或降低其活性,可在常溫常壓下進行催化反應而不引起雙鍵的異構化。
若用一個有機化合物作為氫的給予體,在催化劑作用下進行氫化,則稱為催化轉移氫化反應,例如: