簡介
中文名稱:氰化亞銅;
中文同義詞:氰化銅(Ⅰ);氰化銅;氰化亞銅;氰化亞銅 046-04 ;氰化亞銅(I);
英文名稱:COPPER(I) CYANIDE;
英文同義詞:CUPROUS CYANIDE;CUPRICIN;COPPER CYANIDE;COPPER(I) CYANIDE;COPPER(+1)CYANIDE;ai3-28745;Copper cyanide (Cu(CN));coppercyanide(cu(cn));
Mol檔案:544-92-3.mol。
物理性質
相對密度(水=1):2.9(氮氣中)
溶解性:不溶於水、稀酸,易溶於濃鹽酸。
易溶於氨水、銨鹽溶液。溶於氰化鈉、氰化銨、氰化鉀時生成氰銅絡合物。
分子結構數據:
1、摩爾折射率:無可用的;
2、摩爾體積(m/mol):無可用的;
3、等張比容(90.2K):無可用的;
4、表面張力(dyne/cm):無可用的;
5、介電常數:無可用的;
6、極化率(10-24cm):無可用的;
7、單一同位素質量:88.932675 Da;
8、標稱質量:89 Da;
9、平均質量:89.5634 Da。
化學性質
溶於氰化鈉、氰化銨、氰化鉀時生成氰銅絡合物。可與多種金屬離子形成絡合物。不溶於水和冷的稀酸。在沸騰的稀鹽酸中分解成氯化亞銅和氰化氫。劇毒。
毒性
本品劇毒,毒性與氫氰酸類似。慢性中毒出現頭痛、消瘦、性機能及性慾障礙、貧血、白細胞減少及氰化血紅蛋白升高。吞入粉塵引起中毒時,用3%雙氧水或0.2%高錳酸鉀洗胃,每過15分鐘給一湯匙硫酸亞鐵和煅鎂氧乳液。
毒理學數據
急性毒性:大鼠經口LD50:1265mg/kg,除致死劑量外無詳細說明;慢性中毒會出現頭痛、消瘦,最高容許濃度為0.5mg·m-3。
生態學數據
其他有害作用:該物質對環境有危害,應特別注意對水體的污染。
計算化學數據
1、疏水參數計算參考值(XlogP):無;
2、氫鍵供體數量:0;
3、氫鍵受體數量:2;
4、可鏇轉化學鍵數量:0;
5、互變異構體數量:無;
6、拓撲分子極性表面積(TPSA):23.8;
7、重原子數量:3;
8、表面電荷:0;
9、複雜度:10;
10、同位素原子數量:0;
11、確定原子立構中心數量:0;
12、不確定原子立構中心數量:0;
13、確定化學鍵立構中心數量:0;
14、不確定化學鍵立構中心數量:0;
15、共價鍵單元數量:2。
作用與用途
1.本品在氰化物鍍銅的電鍍液中作絡合劑,鍍液的分散性和復蓋性較好,鍍層結晶細緻,而且鍍渡呈鹼性,有一定的去污性。對於鋼鐵製品和鋅製品等基體金屬上直接電鍍銅層可獲得結合力良好的鍍層。其缺點是該鍍液有劇毒,用此液鍍銅必須進行三廢處理,以保護環境,減少公害。
2.氰化亞銅是提供鍍銅或鍍銅合金鍍液中銅離子的主鹽,鍍液中銅離子濃度與陰極過程有較大的影響,銅離子含量低時,陰極極化值增大,電流效率顯著下降,允許的工作電流密度低,也用作化學浸鍍錫及化學鍍銅的穩定劑等。
3.氰化亞銅是有機Cu(I)試劑和有機Cu(II)試劑的有效前體。
氰化亞銅與烷基錫形成的Me3SnCu(CN)Li試劑能與炔基羧酸酯反應得到3-三甲基錫-2-烯基羧酸酯,並且控制不同的溫度能選擇性得到順式或反式產物 。
 氰化亞銅
氰化亞銅類似的,氰化亞銅與烷基鋰形成的烯基銅試劑能作用於α,β-不飽和酮得到加成產物,並進一步發生分子內成環反應 。
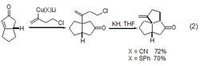 氰化亞銅
氰化亞銅從有機錫化合物製備而來的α-烷氧基銅試劑也能與α,β-不飽和酮發生加成反應 。
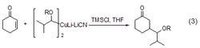 氰化亞銅
氰化亞銅2-噻吩基銅試劑能在丁基鋰作用下與碘代烯烴發生金屬-鹵素交換反應得到烯基銅,進而也能與α,β-不飽和酮發生加成反應。這種合成方法對於前列腺素的合成顯得非常重要。
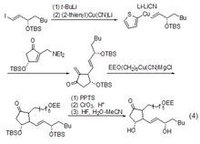 氰化亞銅
氰化亞銅4.用於電鍍銅及其他合金,合成抗結核藥及防污塗料。
5.主要用於無氰電鍍,是供給鍍液中銅離子的主鹽。適用於裝飾性保護層的銅底層和要求滲碳零件的局部防滲碳塗層。用於焦磷酸鹽鍍銅、鍍青銅、鍍鎳、鍍銅錫合金以及鍍鎢合金等,還用於分析試劑.
使用注意事項
危險性概述
健康危害:吸入後引起紫紺、頭痛、頭暈、噁心、嘔吐、虛弱、驚厥、昏迷、咳嗽、呼吸困難。對呼吸道有強烈刺激性,可引起肺水腫而致死。對皮膚、眼有強烈刺激性,可致灼傷。口服出現紫紺、頭痛、頭暈、噁心、嘔吐、虛弱、昏迷、呼吸困難、血壓下降等;刺激口腔和消化道或造成灼傷。
燃爆危險:該品不燃,劇毒,具強刺激性。
安全術語
S29Do not empty into drains.
切勿倒入下水道。
S45In case of accident or if you feel unwell, seek medical advice immediately (show the label whenever possible.)
若發生事故或感不適,立即就醫(可能的話,出示其標籤)。
S60This material and its container must be disposed of as hazardous waste.
該物質及其容器須作為危險性廢料處置。
S61Avoid release to the environment. Refer to special instructions / safety data sheets.
避免釋放至環境中。參考特別說明/安全數據說明書。
S7Keep container tightly closed.
保持容器密封。
風險術語
R26/27/28Very toxic by inhalation, in contact with skin and if swallowed.
吸入、皮膚接觸及吞食有極高毒性。
R32Contact with acid liberates very toxic gas.
與酸接觸釋放極高毒性氣體。
急救措施
皮膚接觸:立即脫去污染的衣著,用大量流動清水沖洗至少15分鐘。就醫。
眼睛接觸:立即提起眼瞼,用大量流動清水或生理鹽水徹底沖洗至少15分鐘。就醫。
吸入:迅速脫離現場至空氣新鮮處。保持呼吸道通暢。如呼吸困難,給輸氧。呼吸心跳停止時,立即進行人工呼吸(勿用口對口)和胸外心臟按壓術。給吸入亞硝酸異戊酯,就醫。
食入:飲足量溫水,催吐。用1:5000高錳酸鉀或5%硫代硫酸鈉溶液洗胃。就醫。
消防措施
危險特性:不燃。受高熱或與酸接觸會產生劇毒的氰化物氣體。與硝酸鹽、亞硝酸鹽、氯酸鹽反應劇烈, 有發生爆炸的危險。遇酸或露置空氣中能吸收水分和二氧化碳分解出劇毒的氰化氫氣體。
有害燃燒產物:氰化氫、氧化氮。
滅火方法:該品不燃。發生火災時應儘量搶救商品,防止包裝破損,引起環境污染。消防人員須佩戴防毒面具、穿全身消防服,在上風向滅火。
滅火劑:乾粉、砂土。禁止用二氧化碳和酸鹼滅火劑滅火。
泄漏應急處理
應急處理:隔離泄漏污染區,限制出入。建議應急處理人員戴防塵面具(全面罩),穿防毒服。不要直接接觸泄漏物。
小量泄漏:避免揚塵,用潔淨的鏟子收集於乾燥、潔淨、有蓋的容器中。
大量泄漏:用塑膠布、帆布復蓋。然後收集回收或運至廢物處理場所處置。
操作處置與儲存
操作注意事項:嚴加密閉,提供充分的局部排風和全面通風。操作儘可能機械化、自動化。操作人員必須經過專門培訓,嚴格遵守操作規程。建議操作人員佩戴頭罩型電動送風過濾式防塵呼吸器,穿連衣式膠布防毒衣,戴橡膠手套。避免產生粉塵。避免與氧化劑、酸類接觸。搬運時要輕裝輕卸,防止包裝及容器損壞。配備泄漏應急處理設備。倒空的容器可能殘留有害物。
儲存注意事項:儲存於陰涼、通風的庫房。遠離火種、熱源。庫內相對濕度不超過80%。包裝密封。應與氧化劑、酸類、食用化學品分開存放,切忌混儲。儲區應備有合適的材料收容泄漏物。應嚴格執行極毒物品“五雙”管理制度。
製備
. 氰化亞銅的生產方法有亞硫酸鈉法、亞硫酸鈉循環法、氯化亞銅法。常彩亞硫酸鈉循環法,該法具有操作穩定,控制方便,可節省亞硫酸鈉原料等優點。其工藝流程如下。本方法對原料中含鐵量要求較高,除確保工業原料純度外,硫酸銅含鐵量<0.05%,碳酸鈉含鐵量≤0.005,氰化鈉含鐵量≤0.005,碳酸和硫酸中的含鐵量≤0.001%。因此在合成氰化亞銅前應對原料進行含鐵量處理。
氰化鈉溶液的製備與處理 在溶解槽內用水將氰化鈉和碳酸鈉溶解配成含氰化鈉130 g/L,碳酸鈉60 g/L,加入少量的氫氧化鈉吸收氰化納水解時產生的微量氰化氫。此時Fe形成Fe(OH)3沉澱,轉入沉降槽沉降16 h,上清液經檢驗合格後打入高位槽備用。
硫酸銅溶液的製備與處理 將硫酸銅用水溶解後,用10%的碳酸鈉溶液將pH值調至5~5.3,然後用次氯酸鈉(10%)溶液把Fe氧化成Fe,用水稀釋至硫酸銅280 g/L轉移到沉降槽靜置48 h,澄清液化驗合格備用。
亞硫酸鈉溶液的配製及處理 在溶解槽內將亞硫酸鈉,碳酸鈉用水溶解,配成含亞硫酸鈉150 g/L,碳酸鈉40 g/L的溶液,再加入少許燒鹼,使鐵離子沉澱,在沉降槽中沉降16 h,上清液化驗合格後抽入高位槽備用。
氰化亞銅的合成 將上述製備的硫酸銅和亞硫酸鈉溶液自高位槽中計量放入反應釜中,在不斷攪拌下生成亞硫酸銅和亞硫酸亞銅復鹽糊狀沉澱。再自高位槽計量放出氰化鈉溶液,有碳酸鈉中和副產物硫酸,充分攪拌反應完成後,用稀硫酸調pH值至1~2。用水浮洗除去FeSO4,Na2SO4等雜質。結晶放入真空乾燥器內,真空乾燥即得成品。
1kg CuSO4溶於3.2L水中(40~50℃)。280g NaHSO3溶於800mL水中(50~80℃)。280g NaCN溶於800mL水中(50~80℃)。每種溶液均在60℃過濾。將NaHSO溶液在1~2min內倒入CuSO溶液,接著立即倒入NaCN溶液。有少量SO2放出。10min後將熱溶液過濾。產品用沸水洗滌,再用乙醇洗,在100℃乾燥,得到細軟粉末。
2.硫酸法:在溶解槽內將氰化鈉和碳酸鈉用水在30~40℃溶解成含氰化鈉130g/L、碳酸鈉60g/L的溶液,加入少量氫氧化鈉,以吸收氰化鈉水解時產生的微量氰化氫氣體,並使Fe 、Fe、Ca 、Mg 生成氫氧化物沉澱,沉降16h後分離得合格清液,供反套用。將硫酸銅用水在30~40℃溶解,加入15%~20%碳酸鈉溶液,調ph至5~5.3,加入10%次氯酸鈉使二價鐵氧化成三價鐵,配成含硫酸銅280g/L的溶液,沉降48H,分離清液含Fe<20×10-6,供反套用。將亞硫酸鈉、碳酸鈉用水在30~35℃溶解成含亞硫酸鈉150g/L、碳酸鈉40g/L的溶液,再加入少量氫氧化鈉,使Fe、Ca 、Mg 生成氫氧化物沉澱,沉降16H,分離清液含Fe<20×10-4後,供反套用。將上述配製好的硫酸銅、亞硫酸鈉與碳酸鈉溶液,在攪拌下反應生成亞硫酸銅與亞硫酸亞銅的復鹽糊狀沉澱,再將氰化鈉與碳酸鈉溶液進行反應生成白色氰化亞銅。反應生成的硫酸被碳酸鈉中和,並加稀硫酸調PH至1~2,使沉澱狀態的鐵變成可溶性Fe在漂洗時洗掉,並使CO3 變成CO2氣體放出。反應後的物料用水漂洗除去硫酸鈉,再經離心分離,真空乾燥,即得氰化亞銅成品。其反應式如下:
6CuSO4+6Na2SO3+2H2O→2CuSO3·Cu2SO3↓+6Na2SO4+2H2SO4
2CuSO3·Cu2SO3+6NaCN+H2O→6CuCN↓+3Na2SO3+H2SO4
H2S04+Na2CO3→Na2SO4+CO2↑+H2O

