歷史背景
毒物興奮效應( hormesis)起源於16 世紀Paracelsus 的名言“劑量決定毒物”,即所有物質都是有毒的,只有劑量才能區別毒物,可以說這是毒物興奮效應的雛形。19 世紀微生物學家Schulz 觀察到重金屬和有機溶劑對酵母生長的促進作用後,認為這種現象可能普遍存在於各種化學物和生命體,進而提出了Arndt- Schulz 定律, 即:弱刺激加速生命力,中等強度刺激促進生命力,強刺激抑制生命活力,但很強刺激卻能致死。1943 年,Southam 和Ehrlich 在研究紅雪松提取物對真菌的作用時,將觀察到的雙相劑量- 效應關係曲線正式命名為“hormesis”, 首次使用“hormesis”一詞描述低濃度的有利效應,發表在《Phytopathology》雜誌上,這是hormesis 這個詞第一次出現在學術刊物上。到了20 世紀80 年代,美國EPA 在評價化學物的致癌性時,將Hormesis 列入考慮範圍,以此來回答對於致癌物質“How clean is clean?”,Hormesis 的熱潮開始復甦,尤其是其對危險度評價的影響得到了廣泛的探討。。Calabrese 和Baldwin對Hormesis 進行了大量的研究, 2003 年在《Nature》雜誌上發表題為“Toxicology rethinks its central belief”的文章,至此,有關Hormesis 的研究進一步成為毒理學中的熱點。
Hormesis 一詞源於希臘語“hormaein”,本意是“to excite(激活)”,過去也曾用“hormoligosis”一詞,oligo 表明在低劑量水平下。其劑量-效應關係以“low-dose stimulation and highdoseinhibition”為特徵的雙相曲線。目前在中國近年出版的毒理學參考書和專業雜誌中多將“hormesis”譯成“毒物興奮效應”,也有的譯為“化學興奮效應”、“低劑量促進效應”等。
定義及特徵
簡單地說,一般將Hormesis 定義為化學物對生物體在高劑量時表現負面影響(如生長、發育受抑) ,但在低劑量時卻表現為有益作用(如刺激生長發育) 的現象。精確地說,Hormesis被認為是一種以雙相劑量- 反應曲線為特徵的適應性反應,這種劑量反應曲線關於刺激反應的幅度、刺激域的範圍具有相似的定量特徵,它是生物過程直接誘發或是對生物過程的代償,最終能引起內環境穩態的紊亂。另外Hormesis 也包括高劑量下具刺激作用而低劑量下卻具抑制效應的現象。
最初hormesis在植物生物學、昆蟲反應、免疫刺激等諸多領域的研究中都有發現,但其後由於受到多方面質疑,漸漸被冷落。直至20 世紀90 年代,才又受到重視。現在美國環境保護局( EPA) 在評價物質致癌性時,已開始考慮低劑量物質的興奮效應。到目前為止,在各類生物(包括動物、植物、微生物) 、各類毒物(包括致癌物、非致癌物,致癌物又包括遺傳毒性致癌物與非遺傳毒性致癌物) 及各類生命現象(包括腫瘤形成、生殖、生長、壽命及代謝等) 中都發現了Hormesis 現象。其範圍幾乎涵蓋了包括重金屬化合物、氰化物、多環芳烴、多氯聯苯、有機砷化物以及農藥和一些抗生素在內的所有有毒物質。
總的來說,Hormesis以雙相劑量反應關係為主要特徵,即低劑量表現為刺激效應,而高劑量則表現為抑制效應。事實上,一種物質能引起一個模型一個部位的興奮效應並不一定在該模型的其他部位也能引起同樣的效應。例如一些殺草劑在低劑量下能促進植物根的生長,但它在任何劑量下都不會促進植物芽的生。毒物興奮效應在對毒物有不同敏感性的個體和種族之間卻有著相似的定量特徵。Calabrese and Baldwin將其概括為很小的刺激反應幅度,很窄的刺激反應劑量範圍。最大的刺激反應幅度一般不會超過對照的2倍,通常情況下,這種反應只比對照高30% - 60% ,Hormesis 效應劑量通常比未觀察到作用濃度(NOEC) 低10 倍左右。
作用機制
針對Hormesis的機理,已經有幾種理論,但是這些理論尚缺乏足夠的實驗證據支持。對絕大部分有毒物質低劑量的刺激作用的機理至今並不清楚。一系列的證據表明,沒有哪一個機制能完全解釋毒物興奮效應現象的發生, 因為根據的組織、細胞和終點的選擇的不同,它通過不同的激動劑和受體來起作用的。
其中一個比較公認的理論就是受體機制。受體機制認為機體應具有兩種不同激動劑親和力的受體亞型,通過這兩種受體亞型要么引起興奮效應,要么引起抑制效應。低濃度時具有高親和力的受體亞型起作用,對於激動劑,低親和力的受體有很高的容量,也就是有很多的受體。高濃度時低親和力的受體發揮作用,並且它的高容量這時將變得相當重要。正是有兩種不同親和力受體亞型的出現,才解釋了毒物興奮效應的發生。
另一個代表性理論是Stebbing的矯正過度(overcorrection)控制理論,指出由於所有的有毒試劑在高濃度時都抑制生物的生長,那么Hormesis可能是生物體對於低劑量抑制的一種反應,也就是說由抑制生長所造成的生長刺激作用,是生物體對抑制的中和或反抗(neutralises oropposes),或者說是生物體的一種自我矯正。任何通過這樣的控制機制對抑制的矯正過度都會導致Hormesis現象,而且,該理論還指出在哺乳動物或單細胞生物體中出現的Hormesis,其機理應是亞細胞水平的。調節控制機制最有可能的方式是對生物合成速率進行調整,不僅表現在生物化學水平改變上,而且還表現在生物體發生Hormesis現象的整個過程中,Hormesis是調節生物體控制的副產品。
Calabrese認為Hormesis顯示了一種過度補償效應,此效應是對體內平衡達到瓦解地步的回響。按照這一觀點,生物體受到刺激,最初的抑制反應之後會出現一個補償過程,這個補償行為會逐漸超過控制行為,從而導致一個淨刺激效應,也就是通常所提及的Hormesis效應。大量的例子表明類似毒物興奮效應的劑量- 反應在動態平衡的破壞中能表現出一種過度補償作用。過度補償作用可以表現為生理上試圖逃避化學刺激,或者對這種刺激表現出一種補償作用。在植物中,Weidman 和Appleby觀察到,它可產生更多的樹子,使一代有更多的機會成活。有毒物興奮效應表現為,在低劑量下,它刺激植物激素的產生,而高劑量下則抑制。當動物暴露一低劑量的化學物時,它們會產生更多的後代來抵抗不利環境條件下的低成活率。
研究進展
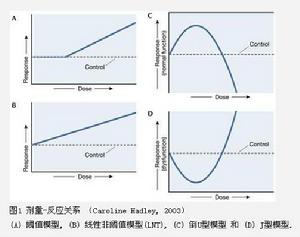 圖一
圖一劑量/效應曲線是毒理學的基本問題。通常,化學品與生物機體(離體和活體)相互作用的關係可以用二類劑量效應關係描述:線性回響和非線性回響[8]。在非線性回響中,已經觀察到的效應隨劑量變化類型包括:
1)效應隨劑量單調非線性遞增或遞減;
2)拋物線結構,並且存在一個無作用劑量;
3)“S”型曲線,或通常觀察到急性毒性的劑量/效應關係:
4)“口”型曲線,存在一個最大效應,高於或低於該效應濃度時效應減弱;
5)“U”型曲線,存在一個最小效應,高於或低於該效應濃度時均表現出效應增強。
在當前毒理學研究中,存在2種劑量-效應關係模型,即線性非閾值模型(linear non-threshold model,LNTModel) 、閾值模型(threshold model)。它們是傳統毒物風險評估中套用最多的兩種模型,前者主要套用於非致癌物及非遺傳毒性致癌物健康風險評估中,後者主要套用於遺傳毒性致癌物健康風險評估與毒物生態風險評估中。Calabrese 認為劑量-反應關係既非閾值模型,又非線性模型,其基本形式應該是U型(圖1) 。U 型曲線通常被稱做毒物興奮性劑量-反應關係曲線,即在低劑量條件下表現為適當的刺激(興奮) 反應,而在高劑量條件下表現為抑制作用。1982年Stebbing提出了公認的β-曲線,在1990 年Svendsgaard 強調β-曲線和U-型劑量反應關係。毒物興奮效應從復興到目前,主要是由於線性域值模型在估計腫瘤發生危險度和由此導致的昂貴的補救措施讓人不容樂觀。
生物學意義
Hormesis 是生物長期進化過程中為順應自然選擇,提高在各種低水平脅迫下的成活率而形成的一個生理機制,其意義在於當生物體自穩狀態(homostatic)受到破壞後能夠迅速恢復。Hormesis 的功能主要有:(1) 儘快修復脅迫引起的損傷; (2) 保護生物體在其後的脅迫中免受或少受傷害,即使是其後不再遭遇相同脅迫,也有利於生物體抵禦環境中其他不利因素的影響。在低濃度的外源性因素作用造成輕微的損傷時,如(化學) 興奮效應機制被激活發揮作用,則機體很快恢復;但如果興奮效應機制被抑制,則損傷進一步擴大、惡化,形成更大範圍的損傷。
在環保方面,它對評價致癌危險度的低劑量線性關係模型的可信度及套用是一個挑戰,強調了致癌劑存在閾值。如果遵循毒物興奮效應規律,化學物在低劑量存在時實際上不是一件壞事,似乎沒有必要如此浪費財力,因此這一觀點為政府部門有的放矢地控制污染,節約資金提供了依據。同時,毒物興奮效應的觀點徹底改變了向公眾進行危險度交流的策略。
在醫學上帶來的影響:許多抗生素、抗病毒劑和抗腫瘤製劑以及大量的其它藥物都表現出毒物興奮性的雙相劑量-反應:一個劑量可能是臨床有效的,但另一劑量則可能是有害的。如一些抗腫瘤藥物(如蘇拉明) 在高劑量下抑制細胞增殖,此時具有臨床療效,而在低劑量條件下又成為一種局部激動劑,可以促進細胞增殖。因此,毒物興奮效應的雙相劑量-反應關係不僅為完善臨床治療方案提供了新的機會,同時也提出了必須要解決的危險性問題。
總之,毒物興奮效應劑量-反應關係是一種更為普遍的、更適用的劑量2反應關係模型。對毒物興奮效應的全面認可將會提高對生物的適應性反應、危險度評價和臨床醫學的認識,並在更廣的生物學範疇加深對細胞和機體水平調控機制的理解。
存在的爭論
(1)關於Hormesis的普遍性
Calabrese 認為化學興奮效應廣泛存在於不同種屬、不同結構的化學物以及各種生命終點。早在19 世紀就已在動物實驗中發現了毒物興奮效應,在此之後的100 多年時間裡已發現了5000 多例毒物興奮效應的例子,如低水平的環境因素如鎘、糖精、二惡英、大量的多環芳烴、X 射線和γ射線源可降低一些種屬動物的腫瘤發生率;低劑量的X射線可增加小鼠和豚鼠的壽命;低劑量的乙醇和乙醛能延長果蠅的壽命;多種環境刺激因素可以延長線蟲的壽命;許多毒物(如鎘、鉛) 可促進不同植物的生長等。Roberts則認為Hormesis 現象的產生依賴於3 個條件,第一,所選擇的健康終點必須存在可以升高或降低的基線,如癌症發生率、經常性頭痛發生率等;第二,具有U 型劑量反應關係的毒物對這些健康終點會產生影響,並且低劑量時的影響與高劑量相反;第三,這種現象的產生應是源於內環境穩定受到破壞後所導致的超補償效應(overcompensation),H ormesis 現象的發生也正是在超補償效應充分表達之後。
(2)關於其毒物風險評價中套用價值
擁護者認為Hormesis 在毒物健康風險評估(包括致癌風險評估、非致癌風險評估) 、生態風險評估中都具有極高的套用價值。最大好處表現在既能更有效地控制風險,又能降低風險控制成本。另一些人則認為雖然在生態風險評估中,毒物風險的表現形式可能不應該只有單調函式一種形式,但Hormesis也並非就是非線性函式的最佳形式。因為Hormesis 需要一個參照,當沒有參照而無法判斷影響結果的好壞時,多數生態風險評估學者都認為任何一種偏離生態系統正常範圍的變化(包括某一物種數量的減少或增加),特別是與人類活動有關的變化,都應該視為不利;其次,當前生態風險評估中一個最大的難題是尚難判斷低層次影響與整個生態系統影響之間的相關性,採用單調模型評價存在這個問題,引入Hormesis 後仍同樣存在這個問題;第三,個體對於毒物等不利因素存在適應性反應,而種群、群落和生態系統不存在,因此Hormesis只適用於個體水平,而不適合於生態系統。總之,考慮Hormesis效應並不足以解決當前生態風險評估中存在的問題。
中醫理論
古語有云 “是藥三分毒”, 中藥中含有多種有毒成分。中醫藥理論認為藥物毒性即是藥物的偏性, 是中藥發揮臨床療效的基礎, 但同時也是藥物損傷機體導致毒副反應的根源。由於對藥物進行法定炮製,採用合理的配伍,適宜的劑型,以及嚴格的藥物劑量,有效的降低了藥物的毒性,使中藥的毒性被控制在低劑量的範圍內。所以筆者認為,中藥在一定程度上起到了毒物興奮效應。據研究發現,清解藥能增強單核2吞噬細胞系統(MDS) 功能,能增加T細胞功能,能使體液免疫系統抗體增強,從而增強機體中和病毒、中和外毒素的能力,並促進吞噬功能。還發現補腎陽的淫羊藿、鹿茸、等能增強腎虛患者T 淋巴細胞的比值,促進健康人淋巴細胞轉化。補腎陰藥枸杞子、五味子、山茱萸也同樣具有促進健康人淋巴細胞轉化的作用。這些藥物對機體免疫的激發,便是一種毒物興奮效應。中醫經過歷代醫家醫療實踐,總結出了精妙的藥物配伍法則和炮製工藝,在經驗上得到了比較合理的藥物毒性的劑量標準。所以在長期的治療中很好的運用的毒物興奮效應的原理。
除了中藥之外,拔火罐、刮痧、針灸、熱水浴等中醫傳統療法,同樣起到了毒物興奮效應(Hormesis)。通過對對機體的局部損傷,而引發“全身應激反應”,如免疫,抗氧化系統的激活.據研究發現,刮疹療法作為一種誘導因素升高白細胞和IL-6,刺激免疫細胞增殖和活化,提高機體免疫能力,另外還誘導直接膽紅素和SOD的升高,增強機體抗氧化防禦系統。針灸療法可使白細胞總數增加、網狀內皮細胞吞噬機能增強、免疫活性細胞活躍。同時促使體液免疫中各類免疫球蛋白(IgA、IgM、IgM)、殺菌素、補體、溶菌素等含量升高,以及自然殺傷細胞(NK細胞)的增加。對培養細胞進行溫和的熱刺激(42℃,30 min,相當於熱水浴),細胞顯示出顯著的(約20倍)谷胱甘肽轉移酶hGST5.8的上調和轉運羰基垃圾的RLIP76蛋白的誘導表達。
