病因
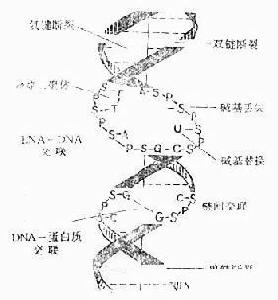 電力輻射對DNA的損傷
電力輻射對DNA的損傷明顯增加而較大劑量照射甲狀腺功能改變和甲狀腺炎更常見。
2.甲狀腺功能改變與射線的劑量、種類、暴露、時間個體差異、年齡、性別、遺傳有關。
3.放射性碘治療,即頭頸部疾病外照射治療後可引起急性和慢性甲狀腺炎。
發病機制:
理論上放射線可以抑制濾泡上皮功能,減少功能性濾泡數量,改變血液供應或血管通透性,誘導免疫反應產生各種甲狀腺功能異常的表現。然而,任何形式的放射損傷的確切機制還不清楚。在致死劑量核爆炸的3到6周內急性改變包括濾泡變小伴扁平立方上皮較高的放射劑量如治療劑量的131Ⅰ產生濾泡壞
 放射性甲狀腺炎
放射性甲狀腺炎死、急性血管炎血栓形成和出血,隨後淋巴細胞浸潤、血管硬化低劑量引起的慢性改變包括局部無規則的濾泡增生,血管玻璃樣變和纖維化淋巴細胞浸潤。
一項前瞻性研究表明在放射治療期(甲狀腺毒症期)血清TSH明顯下降,因為放射線促進甲狀腺激素的釋放,抑制TSH分泌放射治療後(甲狀腺功能減低期)TSH增加。甲狀腺接受治療劑量的外照射可發生甲狀腺毒症。放射治療開始後4~12個月血清TSH增加,而前3個月的潛伏期是穩定的。甲狀腺激素中游離T4是放射誘導的甲狀腺功能異常最敏感指標。甲狀腺毒症是輕微的,在給予小劑量放射線如4周40Gy後未發現甲狀腺組織學上破壞性的改變,因此,認為過度的激素釋放可能是因為細胞膜通透性增加引起放射治療結束後2周降低的TSH水平開始上升,此時,仍明顯低於治療前,此後TSH繼續上升。類似的改變也見於亞急性甲狀腺炎的病程中,認為放射治療期間甲狀腺發生炎症性改變即急性放射性甲狀腺炎。在放射性甲狀腺炎6個月時TSH水平高於治療前,隨訪期未恢復到基線水平,提示濾泡不可逆損傷可能發生一些研究證明放射治療後幾年甲狀腺功能減低的發生率增加其原因可能是放射治療後的甲狀腺幹細胞被殺傷導致有絲分裂減少逐漸產生甲狀腺功能減低,血管損傷也起一定的作用。
典型的病理改變:濾泡破壞和萎縮、嗜酸細胞變、核異形性、結節形成、淋巴細胞浸潤、濾泡外大量膠質、纖維化。
急性期變化:早期甲狀腺充血、水腫、濾泡細胞脫落膠質吞噬;此後,濾泡細胞片段,少量炎症細胞(如中性粒細胞)浸潤,膠質丟失,繼之濾泡崩解,濾泡上皮呈無一定結構的上皮巢,類膠質溢出濾泡外,廣泛壞死,核固縮。濾泡上皮發生嗜酸性細胞變,胞漿豐富並出現嗜酸性顆粒,細胞大小排列染色均不一致,核大小不一,常有核肥大、深染和畸形,應與癌細胞鑑別。放射線可能損害結締組織,一些濾泡變小,呈不含類膠質的小濾泡,少數病例可有甲狀腺結節或腺瘤形成,可能是從放射性碘損害後仍具增生能力的甲狀腺組織增生而成的。小血管擴張血管壁增厚,可有纖維素樣變亦可有血栓形成。間質或有輕度炎症細胞浸潤。部分病例有淋巴瘤樣甲狀腺腫樣的結構。間質常有纖維組織增生,尤以濾泡間和小葉間區為明顯。纖維組織增生隨時間增長而增多,最後使整個甲狀腺體積變小,留下小而不規則缺乏類膠質的濾泡殘存於大片纖維組織中,稱為放射後纖維化(postradiation fibrosis)。Kennedy和Thomson認為濾泡上皮的嗜酸細胞變而不存在明顯的甲狀腺炎是放射後較特殊的改變。
進展期變化:增生逐漸停止,修復過程開始,血管損傷繼續,濾泡內和血管旁水腫逐漸消失細胞片段的積聚減少,急性壞死被慢性變形代替濾泡細胞空泡形成,核深染減少肥大和局部增生出現。
晚期變化:甲狀腺萎縮、增生、腫瘤形成或正常。
臨床表現
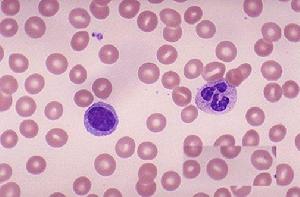 淋巴細胞病理圖
淋巴細胞病理圖2.頸部不適、壓迫感、甲狀腺局部疼痛、吞咽困難、發熱、乏力,心慌、手抖等一過性甲狀腺功能亢進表現少數有甲狀腺危象。甲狀腺觸痛明顯,皮膚表面紅斑皮膚瘙癢和水腫。放射性甲狀腺炎的臨床嚴重程度不一定和放射劑量相關。
併發症:
1.放射性甲狀腺功能減退症(radiation hypothyroidism) 放射性甲狀腺功能減退症是指甲狀腺局部一次或短時間(數周)內多次大劑量受照或長期超當量劑量限值的全身照射所引起的甲狀腺功能低下。處理原則: (1)密切觀察病情,每年複查1次(禁用核素顯像檢查)。
(2)TSH及血脂持續升高者給予甲狀腺製劑替代治療。
(3)暫時脫離射線工作,恢復後可繼續從事放射性工作。 臨床型甲狀腺功能減退症:
(1)脫離射線工作。
(2)甲狀腺製劑替代及輔助治療,每年定期複查。
(3)恢復後可繼續從事放射線工作,持續不恢復者終身替代治療。
2.放射性甲狀腺良性結節radiation benign thyroid nodule) 放射性甲狀腺良性結節是指甲狀腺組織受到大劑量或長期超當量劑量限值的照射後誘發的結節性病變處理原則:
(1)脫離射線工作。
(2)甲狀腺製劑治療,每年複查1次(禁用核素顯像檢查)。
(3)癌變者手術切除按放射性甲狀腺癌處理。
診斷
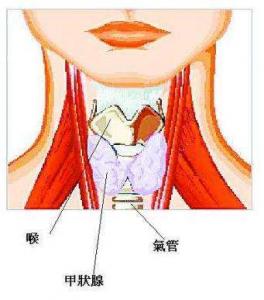 甲狀腺結構圖
甲狀腺結構圖2.一般照射線後2周內發病。
3.有甲狀腺局部壓痛、腫脹。
4.有甲狀腺功能亢進症狀與體徵重症可出現甲狀腺危象。
5.三碘甲腺原氨酸(T3)、血清甲狀腺素(T4)及甲狀腺球蛋白(Tg)升高
6.參考指標血常規白細胞數減少。紅細胞沉降率加快淋巴細胞染色體畸變率及微核率升高。
慢性放射性甲狀腺炎是指甲狀腺一次或短時間(數周)內多次或長期受射線照射後,導致的自身免疫性甲狀腺損傷。診斷標準:①有射線接觸史,甲狀腺劑量為0.3Gy以上②潛伏期1年以上。③甲狀腺腫大,多數無壓痛。④甲狀腺微粒體抗體(Tm-Ab)和(或)甲狀腺球蛋白抗體(Tg-Ab)陽性,促甲狀腺激素(TSH)增高。⑤可伴有甲狀腺功能減退症。
甲狀腺細針穿刺細胞學檢查:131Ⅰ影響的甲狀腺除了典型的結節性甲狀腺腫和(或)慢性淋巴細胞性甲狀腺炎的表現外,塗片有濾泡細胞、大量膠質、纖維血管基質和淋巴細胞組成。濾泡細胞主要呈鬆散的單層叢狀,偶爾形成微小濾泡,有明顯的核大小不等和多形性,大量的體積大而不典型濾泡細胞,主要是單個或叢狀和纖維基質與血管混雜這些細胞的核染色質粗大,偶爾可見明顯的核仁,沒有核溝和核內包涵體核/漿比例稍微增加,細胞質豐富,許多核巨大表現裸核,因此,塗片可被誤診為未分化癌。手術標放射性甲狀腺炎理證實所有的腺體結構被結節形成、淋巴細胞浸潤、纖維化、濾泡萎縮破壞,濾泡細胞明顯的多態性。
鑑別診斷:
亞臨床甲狀腺功能降低病人應幾個月隨訪1次,測定TSH以決定是否L-T4治療,有人建議在亞臨床甲狀腺功能減低階段套用L-T4治療。其他實驗室檢查也有助於診斷甲狀腺功能亢進及甲狀腺炎,攝碘率、TGAb、TPOAbTRAb,細針穿刺細胞學檢查套用於甲狀腺結節甲狀腺掃描和超音波檢查也用於鑑別鑑定。
治療
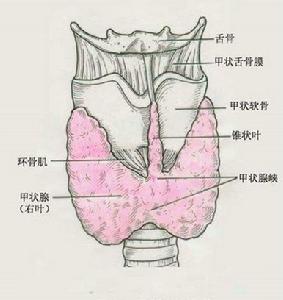 甲狀腺結構圖
甲狀腺結構圖2.病人在服用放射性碘後2~3周出現輕度無菌性甲狀腺炎,多於1周左右自行消退,不需處理或用簡單的鎮痛藥。大劑量放射性碘治療引起甲狀腺激素過度釋放呈一過性甲狀腺功能亢進症甚至甲狀腺危象,常由於治療前準備不充分所致,應對症治療,症狀重者給予鎮靜、止痛和腎上腺皮質類固醇激素治療,甲狀腺危象者按相應情況進行治療β受體阻止藥如普萘洛爾可用主張用抗甲狀腺藥物,此病常常是自限性胺碘苯丙酸鹽聯合β-受體阻止藥治療嚴重破壞性引起的甲狀腺毒症,通過抑制5-脫碘酶減少血中T3減弱甲狀腺激素的外周作用。
3.出現嚴重的喉水腫時,需作氣管切開。
4.脫離射線,每年複查1次(禁用核素顯像檢查);癌變者手術切除,按放射性甲狀腺癌處理。
預後
立即脫離放射源,停止核素治療一般數天后症狀可自行緩解。
預防:
已經接受放射線照射的個體需定期、系統的臨床評價甲狀腺或垂體功能,至少1年1次。包括甲狀腺功能異常症狀,如體重變化、耐熱性月經功能、皮膚或頭髮改變和體力變化甲狀腺功能減低或甲狀腺功能亢進的體徵,仔細觸診甲狀腺以評價大小、發現結節,胸頸部照射後出現心包或胸膜滲出、心律失常或高膽固醇血症的病人應該評價甲狀腺功能測定血清TSH和FT4濃度無症狀的個體也該1年1次檢查以診斷亞臨床甲狀腺功能減低。
