簡介
 扎那米韋
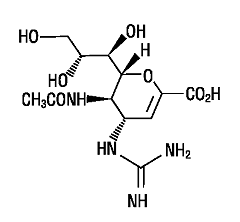
扎那米韋扎那米韋(zanamivir),代號GG167(前代號GR-121167X)。其CAS:139110-80-8,是一個有效的流感病毒唾液酸抑制劑,用於流感的預防和治療。其化學名為N-乙醯基-2,3-二去氧-4-胍基唾液酸(簡稱4-胍基-神經氨-5-乙醯-2-烯)。為無色晶體,溶點>240℃(分解)。[α]20D+41.0(C0.9,H2O),由GL-axo Wellcome公司研製,已獲美國FDA批准,且於1999年5月首先在澳大利亞獲準後,通過相互承認程式,得到歐盟所有成員國的批准。
藥物信息
藥物名稱:扎那米韋 zanamivir
藥物別名:Relenza
分子式成分:化學名為:5-乙醯氨基-4-[(氨基亞氨基甲基)-氨基]-2,6-氫-3,4,5-三去氧-D-丙三醇基-D-半乳糖-2-烯醇酸。分子式C12H20N4O7,相對分子質量332.3。本品為白色或灰白色粉末,20℃時水中的溶解度約為18 mg.ml-1。分子結構如右圖。
製劑規格:片劑:5mg
藥物研究實驗
 扎那米韋
扎那米韋流感是一種極為常見的病毒感染性疾病,僅在美國,每年就有2500~5000萬人患流感,30萬人住院治療,約有2~4萬人死亡。據Glaxo Wellcome公司統計,每年用於治療流感的費用約為1.2億美元。
抑制病毒複製過程中的若干關鍵步驟應是控制和消滅受感染組織中病毒的有效方法。有人認為,流感病毒的唾液酸酶(糖元水解酶)是流感病毒感染和病情發展的重要因素。該酶對病毒從被感染的宿主細胞中釋放新的病毒粒子起著某種作用。因此,抑制唾液酸酶應可阻止或干擾流感病毒的複製。套用分子模型和計算機的化學方法學,Glaxo Wellcom公司根據唾液酸與流感唾液酸酶組相結合的X-衍射晶體結構,合理地設計出了4-胍基-神經氨-5-乙醯-2-烯和-4-氨基神經氨-5-乙醯-2-烯。這兩個化合物對流感A型病毒的唾液酸酶都有特異活性,而且,前者的特異性更好,這一化合物就是扎那米韋。
藥理、藥效學研究
體外結合試驗表明,扎那米韋對A/Tokyo/3/67(N2)流感病毒的抑制是以慢結合的方式進行的,其與流感病毒唾濃酸酶的結合常數(Ki值)比與人唾液酸酶的Ki值高得多。由此說明,扎那米韋有高度特異性。研究人員指出,慢結合是該藥物分子中胍基部分的作用,且對流感A型病毒的特異性,對B型病毒作用較弱。胍基能將A型病毒唾液酸酶活性部位的、呈結合狀態的水分子逐出而產生緊密結合,達到抑制效果。扎那米韋對流感A型和B型多種病毒株(包括實驗室和最近臨床分離的病毒株以及對金剛烷胺、金剛乙胺耐藥的病毒株)的體外活性研究結果發現,該藥對所有分離的病毒均有極強活性,對實驗室傳代病毒株中的流感A型病毒的IC50為0.004~0.014μmol/L,對B型病毒IC50為0.005μmol/L。而金剛烷胺和金剛乙脘的IC50分別為為1.1~7.3μmol/L和0.45~0.62μmol/L。扎那米韋對流感A型和B型病毒的臨床分離病毒株的IC50為0.002~16μmol/L,在用藥濃度為10mmol/L時尚未見其有細胞毒性。對人呼吸道上皮表流感毒B/Hong Kong/5/72毒株也有較強活性,24小時和48小時的IC50值分別為0.54μmol/L和0.25μmol/L,在濃度高達100μmol/L時未見對人的呼吸道上皮細胞有毒性,而利巴韋林的濃度在10和100μmol/L時,對人呼吸道上皮細胞生長有明顯的抑制作用,根據體外研究的數據表明,扎那米韋是迄今所發現的作用最強、酶特異性的廣譜抗流感藥物。但對單純性皰疹A型和B型病毒、帶狀皰疹病毒、人巨細胞病毒、人鼻2型和14型病毒以及副流感2型和3型病毒均無作用。
在體內實驗中,用動物模型研究了扎那米韋的抗病毒活性。該藥對流感A型病毒中的A/Singapore/1/57(H1N1)和A/Mississippi/1/85(H3N2)兩個病毒株的抑制活性比金剛烷胺強100倍;比神經氨-5-乙醯-2-烯強300倍;比利巴韋林強1200倍。並能明顯降低小鼠肺中病毒的滴度和受感染小鼠的死亡率,且未見病毒復燃。
藥動學研究
採用經口給藥、鼻內給藥、皮內或靜脈注射給藥等多種途徑研究了扎那米韋在小鼠體內的藥動學。實驗結果表明,除口服給藥外,其它途徑給藥均有較好的生物利用度。靜注的消除半衰期為10min。經口、皮內和鼻內給藥的尿液排泄率分別為3%、68%和43%。
在人體藥動學研究中,分別過行了不同劑量下單劑量靜脈注射給藥和多劑量給藥的藥動學實驗。靜注扎那米韋後,體內消除迅速,消除半衰期為1.6h,多以原藥形式經尿液排泄,尿中原藥量為給藥量的87%;體內分布僅限於細胞外液,Vdss為16L。經鼻給藥後,尿中原藥排泄量比靜注給藥少得多,為4%~10%,血漿半衰期為3.4h,生物利用度為10%~25%;吸入給藥的半衰期為2.9h。在劑量為16mg時,每日4次,連續7日多劑給藥,藥動學線性未見改變。
臨床研究
在Ⅰ期和Ⅱ期臨床實驗中,採用雙盲、隨機、安慰劑對照的試驗設計,分別多次驗證了扎那米韋對流感A型病毒感染的預防和治療作用。結果表明,該藥有較好的臨床療效,能預防並減少病毒的傳播。鼻內噴霧給藥3.6mg和7.2mg時,相對於安慰劑組,扎那米韋使流感的感染率降低了1/2,且能阻止大多數受感染者體內病毒的散布。在感染流感A型病毒後32h,給予扎那米韋鼻內滴劑16mg2次/d,與安慰劑對照,出現發燒症狀者的比例降低(27:8),症狀級別也明顯下降,且病毒排出量減少(AUC 6.9:0.8)。
臨床前藥理、藥效,藥動學和早期臨床研究概況清楚地說明,作為一個新的抗病毒藥物扎那米韋,對防治流感A型病毒感染具有潛能,根據其藥動學特性,扎那米韋適於每天給藥,並具有良好的藥效和安全性。
藥理毒理
 扎那米韋
扎那米韋美國FDA於1999年8月批准用於治療A型和B型流感。它是自1993年金剛乙胺獲準上市後第一個獲得許可的流感治療藥物,將由葛蘭素威康公司推向市場。
本品通過抑制流感病毒的神經氨酸酶,從而改變了流感病毒在感染細胞內的聚集和釋放。體外試驗時發現,當藥物濃度不斷增加時,仍有流感病毒對扎那米韋的敏感性下降。經分析,這與病毒突變引起神經氨酸酶及血細胞凝集素二者或其一的胺基酸發生改變有關。
功用作用
成年患者和12歲以上的青少年患者,治療由A型和B型流感病毒引起的流感。
藥動學
口腔吸入本品10 mg後,1~2 h內4%~17%的藥物被全身吸收,藥物峰濃度範圍17~142 ng.ml-1,藥時曲線下面積為111~1364 ng.h.ml-1。本品的血漿蛋白結合率低於10%。藥物以原形在24 h內由腎排出,尚未檢測到其代謝物。血清半衰期為2.5~5.1 h不等。總清除率為2.5~10.9 L.h-1。
輕(中)度或重度腎功能不良的患者分別靜脈輸注扎那米韋4 mg或2 mg後,腎清除率明顯下降:正常人總清除率平均為5.3 L.h-1,輕(中)度腎功能不良者為2.7 L.h-1,重度腎功能不良者為0.8 L.h-1。半衰期明顯增加:正常人平均為3.1 h,輕(中)度腎功能不良者為4.7 h,重度腎功能不良者為18.5 h。
適應症:成年患者和12歲以上的青少年患者,治療由A型和B型流感病毒引起的流感。
不良反應
本品對哮喘或慢性阻滯性肺疾病患者治療無效,甚至可能引起危險。文獻報告使用本品後,輕度或中度哮喘患者可引起支氣管痙攣,引起支氣管痙攣的患者應停藥並通知其主治醫生。患有呼吸道疾病的患者服用扎那米韋時,身邊應備有吸入型速效支氣管擴張藥。
服用此藥的其它不良反應包括:頭痛、腹泄、噁心、嘔吐、眩暈等。發生率低於2%,多為輕度反應。
動物試驗表明:扎那米韋不會致癌、致畸、致突變,未見生殖毒性。扎那米韋在動物試驗中能通過胎盤屏障,胎兒血藥濃度明顯低於母體。目前缺乏充分有效的研究結果證實懷孕婦女體內藥物動力學,使用時應權衡對胎兒的影響。哺乳大鼠的乳汁中測得扎那米韋存在。但是,人乳汁中藥物是否存在尚不肯定,哺乳婦女使用此藥應慎重。該藥物對老人及12歲以下兒童的不良反應尚不確定。
體外研究未見本品有明顯的藥物相互作用,本品不影響肝臟微粒體酶,也不是P450酶的底物。
用法用量
本品經口吸入給藥。使用前患者應在其主治醫生的指導下學習吸入劑正確使用,可能的話應由醫師示範使用方法。患者也要仔細閱讀並遵守藥品包裝內的使用說明。
本品可用於成年患者和12歲以上的青少年患者,每日兩次,間隔約12 h。每次10 mg,分兩次吸入,一次5 mg。連用5 d。隨後數日兩次的服藥時間應儘可能保持一致,劑量間隔12 h(如早晨或傍晚)。
患者即使感到症狀好轉也應完成5 d療程,並應被告知服用扎那米韋不能減少流感傳染的危險性。
服用本品時,使用1種呼吸驅動的塑膠吸入裝置Dishkhaler。此裝置可裝入1片Relenza Rotodisk,每片Rotodisk含有4個泡囊,每個泡囊含Relenza(5 mg)和乳糖(20 mg)的混合粉末。使用時,將Relenza Rotodisk放入該吸入裝置,當患者通過嘴吸入時,泡囊被刺穿,藥物隨氣流釋放出來。
本品是否可預防流感尚不清楚。
注意事項
對該藥物處方中的任何成分過敏者禁用。
貯藏方法
密封。
