概述
海洋生物中蘊藏著大量結構新穎、生理活性和功能獨特的生物活性物質及其基因,這使海洋生物成為具有獨特功能和藥用價值的生物活性物質的重要源泉。而海洋生物毒素是海洋活性物質中研究發展最迅速的領域之一,也是海洋新型藥物研究的熱點。
海洋生物毒素種類多,分布廣,結構奇特,活性廣泛且活性強。其中,由基因直接編碼的多肽蛋白毒素是天然海洋生物毒素中毒性最強的。比較具有代表性的海洋多肽類毒素包括芋螺毒素、海蛇毒素、海葵毒素、水母毒素和海膽毒素等。這些多肽毒素具有毒性作用強烈、藥效高和作用劑量小等特點。
芋螺毒素
芋螺毒素(conotoxin,CTX)是由熱帶海洋中肉食性軟體動物芋螺(Conus)分泌的毒液中的一大類活性多肽,用於麻醉獵物和防禦敵害。在所有的動物毒素中,來自海洋軟體動物芋螺毒液中的多肽類毒素-芋螺毒素可能是迄今為止最具有多樣性的代表。全世界大約有500~700個芋螺物種,每一種類的芋螺所含有的不同序列結構的肽類毒素多達100~200種,而且任何兩種芋螺所含有的毒素很少重疊,因此,據估計現有的芋螺毒素種類可高達50000種以上。
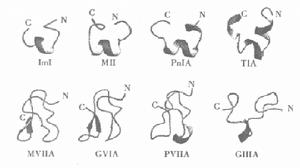 芋螺毒素分子三維結構
芋螺毒素分子三維結構海蛇毒素
海蛇屬於海蛇科(Hydrophiidae),大約有50種,廣泛分布於印度洋和太平洋的熱帶及亞熱帶海域。海蛇毒液中含有20種以上的活性物質,包括酸性磷酸酶、磷脂酶A、長鏈和短鏈神經毒素等,且大多數屬於低分子量蛋白質。它們均能高度專一性地與運動終板菸鹼乙醯膽鹼受體結合,阻斷神經傳導成為突觸後神經毒素,成為研究菸鹼乙醯膽鹼受體的重要工具。由於海蛇毒素(sea snake toxins)具有多種多樣的毒理和藥理活性,且在治療腫瘤、心血管及神經系統疾病方面有極高的藥用價值。除了海蛇科外,海蛇毒素還廣泛存在於眼鏡蛇科毒液中。相同乾重的海蛇致死毒性遠高於眼鏡蛇,但是,海蛇的排毒量比陸地蛇低8~10 倍。這給進行海蛇蛇毒的研究帶來很大困難。國內關於海蛇毒素的研究非常少,大多數是關於海蛇蛇毒的毒理學和抗海蛇毒血清的研究。 迄今為止,已經發現了100 多種蛇突觸後神經毒素,根據它們的胺基酸序列特徵和與不同乙醯膽鹼受體亞型結合的能力,可將其分為短鏈α-神經毒素、長鏈α-神經毒素、κ-神經毒素、γ-神經毒素和弱毒神經毒素五類。短鏈α-神經毒素一般由60~62 個胺基酸組成,含有4 對鏈內二硫鍵,長鏈α-神經毒素一般由66~74 個胺基酸組成,含有5 對鏈內二硫鍵,兩者之間胺基酸同源性較高。兩者的空間結構都有一個三指結構。長鏈和短鏈的海蛇神經毒素都是有效的阻斷神經肌肉接頭的菸鹼乙醯膽鹼受體。
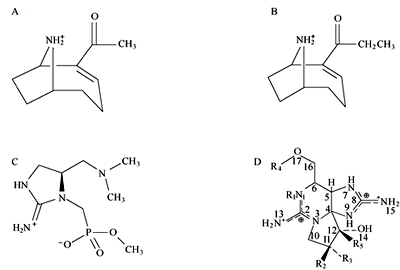 海蛇毒素分子結構
海蛇毒素分子結構海葵毒素
海葵(anthopleura)屬於腔腸動物門(soelenterata),在熱帶和溫帶海域廣泛分布。它的口周圍有許多觸手,觸手上分布著腔腸動物所特有的刺絲囊,能分泌大量的肽類毒素。海葵毒素多肽是一類相對分子質量範圍在3000~6000、由2~3個二硫鍵交聯著的單鏈鹼性分子。根據作用方式的不同,可將這些肽類毒素分為海葵神經毒素(sea anemone neurotoxin,SAN)、海葵溶細胞素(sea anemone cytolysin,SAC)和鉀離子通道抑制劑(Sea anemone potassium Channel inhibitor )。這些海葵毒素(anthoplerin toxin)能特異作用於神經和肌肉可興奮細胞膜上的關鍵靶位即神經受體或離子通道,從而影響一系列細胞調控活動,具有廣泛的神經系統活性、心血管系統活性和細胞活性。因此,海葵毒素作為分子探針用以研究鈉通道有巨大潛力,並且發現更多有套用前景的海葵毒素並進行基因重組、表達,極具重要意義。對於海葵神經毒素的研究始於1976年美國夏威夷大學Shibata等的工作,他們從黃海葵(Anthopleura xanthogrammica)中分離純化了海葵神經毒素A(anthopleurin A,Ap-A)和海葵神經毒素B(anthopleurin B,Ap-B)兩種毒素。
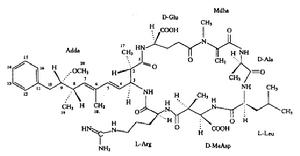 砂海葵毒素分子結構
砂海葵毒素分子結構水母毒素
水母(jellyfish) 也屬於腔腸動物門(Soelenterata),亦稱海蜇,它們種類多、數量大且廣泛分布於溫帶、亞熱帶及熱帶海域。水母的觸手中也分布有能分泌大量毒液的刺絲囊,肽類毒素是其中主要的毒液成分,它們結構新穎獨特,具有溶血性、酶活性、神經毒性、皮膚壞死、肌肉毒性、肝臟毒性、心臟毒性以及細胞毒性等多種生物活性。這些毒素通過作用於離子通道,對心臟、血管產生影響,進而引起血壓和心電圖改變及造成細胞毒性。因此,水母毒素(jellyfish venom) 有望開發為作用於心血管系統、中樞神經系統和肌肉的藥物。
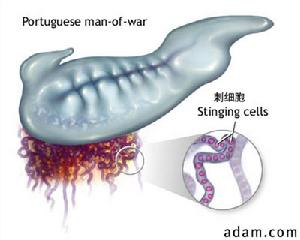 水母觸手
水母觸手海膽毒素
海膽屬於棘皮動物門(Echinodermata),是海洋中一類常見的無脊椎動物,在世界各大海域的海底中均有分布。海膽中的毒素主要由叉棘(pedicellariea)和棘(spine)產生。海膽毒素可引起動物呼吸困難、肌肉麻痹、溶血、引起心臟激活以及使肌肉對非直接刺激不起反應。因此,海膽毒素具有潛在的藥用價值。近幾年來,科學工作者主要集中研究刺胞毒素的分離提取、功能基因的克隆、毒素的單克隆抗體檢測等。
合成毒素的PCR方法
生物肽類毒素分子量相對較小,可以通過人工合成和基因工程技術進行重組表達、大批量生產。聚合酶鏈式反應(polymerase chain reaction,PCR),即PCR 反應技術,是由美國Cetus 公司人類遺傳研究室的科學家Mullis於1983 年發明的一種能在生物體細胞外通過酶促合成反應快速擴增兩段已知序列之間的DNA序列的方法,又稱無細胞分子克隆技術。目前,PCR 技術已被廣泛套用於分子生物學、工業、農業、食品科學醫藥學和法醫學等各領域,而其技術本身也獲得長足進步,可靠性不斷提高,因而具有更廣闊的發展前景。PCR反應的主要過程是,先在臨近沸點的高溫下雙鏈模板DNA變性形成兩條單鏈DNA,然後在低溫下引物與單鏈DNA互補序列結合,最後在適溫下DNA聚合酶以互補合成的DNA鏈為起點,以單鏈DNA為模板並利用4種脫氧核苷三磷酸合成新的DNA互補鏈。在整個反應過程中,高溫變性、低溫退火、適溫延伸等3個步驟反覆循環,每一循環中所合成的新鏈,都可以作為下一循環中的模板。經過數次循環後,特定DNA 序列的產量隨著循環次數呈指數增加。對於每一個特定的套用而言,需要對PCR 條件進行最佳化,以探索選擇最佳的PCR 條件,獲得高產率、高純度的特異產物。

