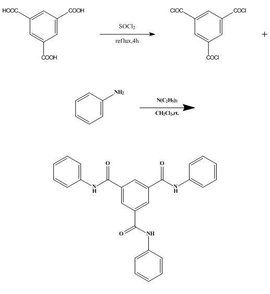
醯氯製備
醯氯最常用的製備方法是用亞硫醯氯、三氯化磷、五氯化磷與羧酸反應製得。
R-COOH + SOCl₂ → R-COCl + SO₂ + HCl
3R-COOH + PCl₃ → 3R-COCl + H₃PO₃
R-COOH + PCl5 → R-COCl + POCl₃ + HCl
其中一般用亞硫醯氯,因為產物二氧化硫和氯化氫都是氣體,容易分離,純度好,產率高。亞硫醯氯的沸點只有79°C,稍過量的亞硫醯氯可以通過蒸餾被分離出來。用亞硫醯氯製備醯氯的反應可以被 二甲基甲醯胺所催化。
也可以用草醯氯作氯化試劑,與羧酸反應製備醯氯:
R-COOH + ClCOCOCl → R-COCl + CO + CO₂ + HCl
這個反應同樣受到二甲基甲醯胺的 催化。機理中,第一步是二甲基甲醯胺與草醯氯作用生成一個活性的亞胺鹽中間體。
然後羧酸與此 中間體反應,生成醯氯,並重新得到二甲基甲醯胺:
此外醯氯也可由羧酸、 四氯化碳和三苯基膦發生Appel反應得到:
R-COOH + Ph₃P + CCl₄ → R-COCl + Ph₃PO + CHCl₃
羧酸與 三聚氰氯反應也可以生成醯氯。
工業上有很多新工藝,如用氯氣、氯某酸和二氯化硫反應法,還有直接用硫磺、氯氣和氯某酸直接反應的,但後者反應劇烈,溫度較難控制,必須通過降低通氯和冷凍水換熱保證理想的反應溫度。
化學反應
親核反應
醯氯中的氯原子有吸 電子效應,增強了碳的親電性,使醯氯更容易受到親核試劑的進攻,而且 Cl− 也是一個很好的 離去基團,因此醯氯發生親核醯基 取代反應的活性在所有羧酸衍生物中最強。最簡單的例子,便是低級醯氯遇水發生的 水解反應:
RCOCl + H-OH → RCOOH + HCl
除此之外,醯氯還可以與氨/胺反應生成醯胺(氨解),與醇反應生成酯( 醇解),與羧酸根離子反應生成 酸酐等。反應中一般加入鹼(如 氫氧化鈉、 吡啶或 胺)來 催化反應,並 吸收反應的副產物氯化氫。由於醯氯比相應的羧酸活性更強,用醯氯作原料的反應也往往產率更高,因此製取 醯胺、 酯、酸酐時也往往以醯氯為原料,而不是羧酸。
有機金屬
與 格氏試劑反應時,一分子的格氏試劑與醯氯反應生成酮,然後第二分子格氏試劑可以再將酮轉化為三級 醇。與活性較低的二 烷基銅鋰和有機 鎘試劑反應時,反應只生成酮。芳香醯氯一般不如脂肪醯氯活潑。
還原反應
還原反應:用 催化氫化、 氫化鋁鋰、 二異丁基氫化鋁還原時,醯氯轉化為一級醇。用1mol的三(叔丁氧基)氫化鋁鋰還原則生成醛。用中毒的鈀催化劑使醯氯發生催化還原時,也會生成醛,這個方法稱為Rosenmund還原反應。
取代反應
氯化鐵或 氯化鋁等 路易斯酸催化時,醯氯可以與芳香化合物發生親電芳香取代反應(傅-克反應),生成芳香酮。反應的機理為:
一個類似的反應是Nenitzescu反應(或稱Nenitshesku反應),是用醯氯與 烯烴在 路易斯酸作用下反應生成酮。機理是醯基正離子先與 烯烴發生 親電加成生成碳正離子,由於羰基α-氫很活潑,因此消除 質子便得到不飽和酮。