成份
 賽可平
賽可平本品主要成分為嗎替麥考酚酯。
化學名稱:2-嗎啉代乙酯(E)-6-(1,3-二氫-4-羥基-6-甲氧基-7-甲基-3-氧代-5-異苯並呋喃基)-4-甲基-4-己烯鹽。
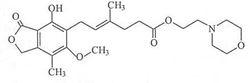
化學結構式:
分子式:CHNO
分子量:433.48
性狀
本品為白色或類白色片。
適應症
本品可用於預防同種腎移植病人的排斥反應,及治療難治性排異反應。本品可與環孢素和腎上腺皮質激素同時套用。也可與他克莫司同時套用。
規格
0.25克
用法用量
預防排異劑量
應於移植72小時內開始口服。腎移植病人服用推薦劑量為1克,一天兩次(一天2克)。口服本品2克/天比口服3克/天安全性更好。
治療難治性排斥的劑量
在臨床試驗中,治療難治性排斥的首次和維持劑量推薦為1.5克,一天兩次(3克/天)。
特殊劑量
如果發生中性粒細胞減少(中性粒細胞計數絕對值[1.3×10[sup]3[/sup]/微升),應停止或減量。嚴重腎功能損害:對有嚴重慢性腎功能損害的病人(腎小球濾過率[25毫升/分/1.73平方米),應避免超過每次1克,一天兩次的劑量(移植後即刻使用除外)。對這些病人應仔細觀察。對腎移植後腎功能延期恢復的病人不需要做劑量調整或遵醫囑。
不良反應
 賽可平
賽可平臨床經驗
免疫抑制劑的副作用的發生常不易明確,因為一方面是基礎病的存在,另一方面是其它多種藥物聯合套用。服用嗎本品或聯合服用本品、環孢菌素和皮質類固醇的主要不良反應包括腹瀉、白細胞減少、膿毒症和嘔吐,還有頻繁的某些類型的感染(見警告)。
使用本品治療難治性腎移植排異的安全性與在三組對照的、每日3克、預防排異的試驗中觀察到的安全性相同。同接受環孢菌素靜注治療的病人相比,腹瀉和白細胞減少,伴隨貧血、腹痛、膿毒症、噁心,嘔吐和消化不良反應是主要的報導較多的副反應。
接受免疫抑制方案的病人,包括合併藥物的病人,接受嗎替麥考酚酯片作為部分免疫抑制的病人,發生淋巴瘤和惡性腫瘤的危險性增加,尤其是皮膚(見警告)。術後3年內,在免疫方案中接受嗎替麥考酚酯片治療的病人發生淋巴增生性疾病或淋巴瘤,在一個預防腎移植排斥的對照實驗中,每天3克的病人的發生率為1.6%,每天2克的病人的發生率為0.6%,安慰組為0%,硫唑嘌呤組的發生率為0.6%。在治療難治性腎移植的對照實驗中,平均隨訪為期42個月的淋巴瘤發生率為3.9%。
所有病人機會感染的危險性增高,危險性隨免疫抑制負荷增加(見警告)。對腎移植病人,用嗎替麥考酚酯片治療和用咪唑硫嘌呤治療,病人機會感染的總發生率相似。
同年輕人相比,老年人,尤其那些接受嗎替麥考酚酯作為聯合免疫抑制方案一部分的病人,一些感染(包括巨細胞病毒屬組織侵入病)、可能的胃腸出血和肺水腫的危險增加。
本品治療腎移植排斥的Ⅲ期對照試驗,所報告的大於10%和3-<10%不良反應列於下表:
上市後的經驗
消化系統:結腸炎(有時由巨細胞病毒屬引起),胰腺炎。
免疫抑制紊亂:嚴重的威脅生命的感染,例如:腦膜炎和感染性心內膜炎偶有報導,有證據表明一定類型的感染如結核和非典型微生物感染有較高的發生頻率。
呼吸系統:肺間質異常,包括致命的肺纖維化少有報導,但在移植後服用本品的患者中如出現呼吸困難、呼吸衰竭等肺部症狀時,應考慮從此方面加以診斷。
本品上市後的其它副反應同在對照的腎移植研究中的副反應相似。
禁忌
本藥的過敏反應已被觀察到。因此,嗎替麥考酚酯片禁用於對於嗎替麥考酚酯和麥考酚酸有超敏反應的患者。
警告
接受免疫抑制劑治療的患者,包括聯合用藥,接受嗎替麥考酚酯片作為部分免疫抑制治療,發生淋巴瘤及其它惡性腫瘤的危險性增加,特別是皮膚。(見【不良反應】)。危險性與免疫抑制的強度和療效有關,而與特定的免疫抑制無關。
由於所有病人發生皮膚癌的危險性增加,應通過穿防護衣或高防護因子的防曬霜來限制暴露於陽光和紫外線下。
免疫系統的過度抑制可增加對感染的易感性,包括機會致病性感染,致死感染和膿毒病。
注意事項
接受免疫抑制療法的病人常採用聯合用藥方式,服用本品作為聯合套用免疫抑制藥物時,有增加淋巴瘤和其它惡性腫瘤(特別是皮膚癌)發生的危險。這一危險與免疫抑制的強度和持續時間有關,而不是與某一特定藥物有關。免疫系統的過度抑制也可能對感染的易感性增加。臨床試驗中本品已與以下藥物聯合套用:抗淋巴細胞球抗體、環孢素和皮質激素類藥物,以預防排斥反應和治療難治性排斥。
實驗室監測:服用本品的病人,第一個月每周一次進行全血細胞計數;第二和第三個月每月兩次;餘下的一年中每月一次。如果發生中性粒細胞減少(中性粒細胞絕對計數小於1.3×10[sup]3[/sup]/微升),本品應停止或減量使用,並對這些病人密切觀察。
嚴重慢性腎功能損害(腎小球濾過率[25毫升/分/1.73平方米),病人服用單劑量本品後,血漿MPA和MPAG的曲線下面積,比輕度腎功能損害病人及健康人高,應避免使用超過1克一天兩次的劑量,並且應對這些病人密切觀察(見藥代動力學和特殊劑量部分)。
移植後腎功能延遲恢復的病人,平均0-12小時MPA曲線下面積與正常恢復病人相仿,但MPAG 0-12小時曲線下面積前者比後者高2-3倍。對這些腎功能延遲恢復的病人無需做劑量調整,但應密切觀察(見藥代動力學和注意事項部分)。
本品不能與硫唑嘌呤同時使用。對這兩種藥物的聯合使用尚未進行試驗。
已注意到消膽胺能顯著減少MPA曲線下面積。不應與嗎替麥考酚酯片同時服用能幹擾腸肝再循環的藥物,因這些藥物可能會降低本品的藥效。
孕婦及哺乳期婦女用藥
大鼠和兔子孕期器官形成過程中使用本品有胎兒畸形可能。儘管還未對孕婦作充分和良好的對照研究,只有在本藥的潛在優點超過對胎兒的潛在危險時方予套用。
應在妊娠試驗陰性後,才開始服用本品。服用本品期間,應採取有效避孕措施,當病人一旦懷孕後,應及時向醫生諮詢。
對大鼠的研究發現MMF可通過乳汁分泌。人乳中是否分泌嗎替麥考酚酯片尚不清楚。並且MMF可能對哺乳期嬰兒有可能潛在的嚴重副作用,應根據MMF對於母親的重要性作出決定:停止哺乳,或者停藥。
兒童用藥
兒童使用該藥的安全性和有效性尚未確證。兒童藥代動力學資料有限,若使用時必需多觀察。
老年用藥
藥代動力學:嗎替麥考酚酯在老年人中的藥代動力學數據未被正式研究過。
用法與用量:老人(大於等於65歲):對腎移植病人,所推薦的口服每次1g,每天2次的劑量對老人是合適的。
注意事項:同青年人相比,老年人發生副反應的危險性增高。
藥物相互作用
阿昔洛韋:MMF和阿昔洛韋同時服用時,MPAG和阿昔洛韋的血漿濃度較兩種藥物單獨服用時為高。當腎功能損害時,MPAG和阿昔洛韋的血漿濃度都升高。這兩種藥物競爭性的通過腎小管排出,可能會進一步增高兩種藥物血濃度。
制酸藥物和氫氧化鎂以及氫氧化鋁:同時服用制酸劑時,MMF的吸收減少。
消膽胺:健康人先服用消膽胺4克一天三次,四天后,給予單劑量MMF1.5克,MPA的曲線下面積減少40%。
環孢素A:Cs A的藥代動力學不受MMF影響。
更昔洛韋: 未觀察到MMF和靜脈注射更昔洛韋之間有有藥代動力學的交叉作用。
口服避孕藥:目前未發現MMF和口服避孕藥1毫克炔諾酮/35微克炔雌醇之間有相互影響,但這僅是單次劑量研究所得出的結論,並不能排除長期服用嗎替麥考酚酯片後改變口服避孕藥的藥代動力學的可能性,這可能導致口服避孕藥的藥效降低。
磺胺甲基異噁唑:對MPA的生物利用度無影響。
他克莫司:腎移植病人:在接受環孢素和MMF(每次1克。一天三次)的穩定的腎移植病人中,當環孢素被他克莫司替換時,血漿MPA升高30%。血漿MPAG降低20%MPA的Cmax未受影響。而MPAG的Cmax降低大約20%。這種結果的機制不明。MPAG膽汁分泌增高伴隨MPA的肝腸循環的升高可能部分導致該結果,因為伴隨他克莫司給藥,MPA濃度的升高在濃度時間曲線的後部分發現較多(給藥後4-12小時)。對於用他克莫司的病人,MMF的劑量不應超過每次1克,一天兩次。病人應被小心監護並正確處理。在另一個腎移植的研究中表明MMF並不改變他克莫司的濃度。
其他相互作用:給猴子同時服用丙磺舒和MMF,可使血漿MPAG曲線下面積增加3倍,為此,其他經腎小管排出的藥物,可以與MPAG競爭,從而使血漿MPAG或這些藥物的濃度升高。
對於有免疫反應障礙的病人不應接種活疫苗。對其他接種的抗體反應可能被消除。
藥物過量
在人類尚無MMF藥物過量的報導。
血透不能清除MPA,當MPAG濃度極高時(]100微克/毫升),能清除小部分MPAG。MPA可通過藥物排出增加(如:給予消膽胺)而得到清除。
藥理毒理
藥理作用:嗎替麥考酚酯(簡稱MMF)是麥考酚酸(MPA)的2-乙基酯類衍生物,MPA是高效、選擇性、非競爭性、可逆性的次黃嘌呤單核苷酸脫氫酶(IMPDH)抑制劑、可抑制鳥嘌呤核苷酸的經典合成途徑。MPA對淋巴細胞具有高度選擇作用。嗎替麥考酚酯片對腎移植後排斥反應的預防和難治性排斥的治療極其有效。
藥代動力學
據文獻資料:
吸收
口服後迅速大量吸收,並代謝為活性成分MPA。口服平均生物利用度為靜脈注射的94%(根據MPA曲線下面積)。口服後在循環中測不出MMF。腎移植病人口服MMF,其吸收不受食物影響,但進食後血MPA最大濃度(Cmax)將降低40%。
分布
由於肝腸循環作用,服藥後6—12小時將出現第二個血漿MPA濃度高峰,與消膽胺(4克,一天三次)同時服用將使MPA曲線下面積減少約40%。表明MPA通過肝腸循環的量很多。在臨床有效濃度下, 97%的MPA與血漿白蛋白結合。
代謝
MPA主要通過葡萄糖醛酸轉移酶,代謝成MPA的酚化葡萄糖苷糖(MPAG), MPAG無藥理活性。
排泄
MMF代謝以後有極少量MPA([1%)從尿液排出,多數(87%)以MPAG的形式從尿液排出。移植後近期內([40天),MPA平均曲線下面積(AUC)和血濃度峰值(Cmax)比正常志願者和移植腎功能穩定的病人分別約低30%及40%。
特殊臨床情況下的藥代動力學
單劑研究(每組6例)顯示,嚴重的慢性功能損害(腎小球濾過率[25毫升/分/1.73平方米),MPA曲線下面積比正常志願者和輕度腎功能損害病人高28-75%。同樣情況下,MPAG曲線下面積高3-6倍,與MPAG主要由腎臟排出一致。尚未進行嚴重慢性腎功能損害病人的MMF多次劑量藥代動力學研究。移植手術後,腎功能延遲恢復的MPA0-12小時曲線下面積(AUC)與無腎功能延遲恢復受者無顯著差異,但無活性成分的MPAG,其0-12小時曲線下面積比腎功能正常恢復病人高2-3倍。
在酒精性肝硬化的志願者中,肝臟實質疾病對MPA的糖苷酸化過程相對無影響,嚴重的膽道損害,如原發性膽汁性肝硬化,可能對這一過程產生影響。
貯藏
15-30℃見貯存,避免潮濕。
包裝
鋁鋁泡罩包裝
10片/板,4板/盒;10片/板,2板/盒;8片/板,5板/盒。
有效期
暫定24個月
執行標準
YBH30692005
批准文號
國藥準字H20052083
生產企業
杭州中美華東製藥有限公司
核准日期
2007年03月12日
修訂日期
2007年09月13日
