病因
腎母細胞瘤可能是後腎胚基未向腎小管和腎小球分化導致異常增殖的結果Bove和McAdams(1976)提示腎母細胞增生複合體(nephroblastomosis complex)可能轉化為腎母細胞瘤。Knudson和Strong(1972)認為根據生殖細胞是否發生突變,可將Wilms瘤分為遺傳型和非遺傳型兩類。若屬於遺傳形式,則腫瘤發生得更早,更易為雙側性及多中心形式發生所有雙側性腎母細胞瘤及15%~20%的單側病變與遺傳有關
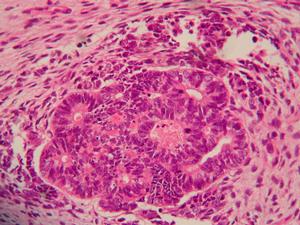 腎母細胞癌
腎母細胞癌臨床表現:
1.腹部腫塊 進行性增大的腹部腫塊是最常見的症狀,常在為患兒穿衣或洗澡時偶然發現腫塊較小時無明顯症狀,不影響患兒營養及健康易被忽視腫瘤巨大時可產生壓迫症狀可有氣促、食欲不振、消瘦、煩躁不安等表現。腫塊位於上腹季肋部一側,表面光滑,中等硬度,無壓痛早期可稍有活動性,迅速增大後,少數病例可越過中線。
2.腹痛 約有1/3患兒出現程度從局部不適、輕微疼痛到絞痛、劇烈疼痛不等如果伴有發熱、腹部腫物、貧血、高血壓常提示腎母細胞瘤包膜下出血。很少有繼發於瘤體腹腔內破裂導致的急腹症者。
3.血尿 約25%患兒有鏡下血尿,肉眼血尿見於10%~15%患兒血尿出現與腫瘤侵入腎盂有關,不作為腫瘤的晚期表現。
4.高血壓 約30%~63%病例出現,可能由於腎血管栓塞或腎動脈受壓缺血,產生腎素所致。有的作者認為腫瘤細胞可以產生腎素,與近球細胞瘤相似一般在腫瘤切除後恢復正常。
5.轉移症狀 下腔靜脈梗阻在肝靜脈以上可有肝大及腹水,如侵入右心房可致充血性心力衰竭或心臟雜音血行轉移可播散至全身各部位,而以肺轉移為最常見,可出現咳嗽胸腔積液、胸痛、低熱、貧血、惡病質。
6.腎外腎母細胞瘤 罕見可位於腹膜後或腹股溝區,可成為複合畸胎瘤的一部分,其他部位包括後縱隔盆腔及骶尾區。
7.全身症狀 無力、疲乏、煩躁、體重下降、食欲不振等,發熱亦較常見。
診斷依據
1.小兒上腹進行性增大的腫塊,首先考慮可能為腎母細胞瘤。
2.尿路造影示腎內占位性病變或腎不顯影。
3.超聲檢查示腎臟實質腫塊,下腔靜脈是否通暢。
4.CT掃描可確定原發瘤的侵犯範圍,腫瘤與周圍組織及器官關係,有無肝轉移等。
鑑別診斷
1.腎積水 出現腹部腫塊,但腫塊有囊性感,隨呼吸上下活動。無明顯消瘦。IVU示腎盂腎盞擴張。
2.多囊腎表現為腹部腫塊,但一般發病年齡較晚,腎功能損害較重。IVU示腎盂腎盞受壓伸長或變形而無擴張。超聲檢查和放射性核素腎掃描示兩側腎體積增大,腎區有多發圓形囊腫影像。CT檢查示雙腎增大,腎實質內可見多數邊緣光滑、大小不等的囊性腫塊。
3.腹膜後神經母細胞癌 多發生於嬰幼兒,表現為腹部腫塊。但腫瘤惡性程度更大,病程發展迅速。IVU示腎及輸尿管移位,腎盂腎盞形態正常。
4.腹膜後畸胎瘤 腹部腫塊與本病相似。但腫瘤生長緩慢,全身狀況較好。KUB平片常見不規則鈣化陰影,IVU示腎及輸尿管移位,腎盂腎盞形態正常。
治療
1.手術治療 對各期腎母細胞瘤,均應手術切除。一般採用經腹部切口,充分暴露術中減少對腫瘤的牽拉和搬動從而避免因手術導致腫瘤擴散。手術時將腫瘤連同鄰近組織和局部淋巴結作整塊切除。若腎靜脈或下腔靜脈有瘤栓,取出瘤栓。若手術切除有困難,可行姑息性手術,腫瘤殘留區域放置金屬夾作術後放療標記。對雙側腎母細胞瘤,一側腎臟作根治性切除另一側作腎部分切除術。
2.放射治療 腎母細胞瘤大多對放療敏感,術後放療可提高療效。也可術前放療,使腫塊縮小隨後手術切除。過去術前放療用於巨大腎母細胞瘤,6~8天內給8~12Gy(800~1200rad),2周內可見腫瘤縮小,減少術中腫瘤破裂可能但未經手術確診前行放療有盲目性,故隨著化療的進步,術前照射已較少套用。手術後48h放療與術後10天開始放療相比療效無明顯差異。早期給放療並不影響傷口癒合。但不宜晚於10天,否則增加局部復發機會凡Ⅰ期組織分化良好者可不作術後照射,組織學不好的術後1~3天即開始照射,Ⅱ、Ⅲ期腫瘤手術後照射20Gy(2000rad)。Ⅲ期有腹內擴散者行全腹照射,對側腎應保護,否則影響腎臟功能。如有殘留腫瘤,則局部追加5~10Gy (500~1000rad)。1歲以內照射10Gy(1000rad),以免影響發育。
3.化學治療 腎母細胞瘤對化療敏感,各期腫瘤術後均可行化療,以提高療效。常用放線菌素D(ACTD)長春新鹼(VCR)及多柔比星(ADR)前兩者可用於腎母細胞瘤各型各期,後者與前兩者聯合用於晚期腫瘤。具體用法是:①放線菌素D,每療程總量80μg/kg體重,分5~7天即15μg/kg體重,共5天或12μg/kg,共7天,靜脈注射。第1、第2療程之間間隔1.5個月,以後每3個月1個療程。②長春新鹼,1~2mg/m2每1mg溶於20ml生理鹽水靜脈注射每周1次連用10周后改為每2周1次,作為維持量。③ADR,每療程總量為40~60mg/m2,分2~3天靜脈注射,每療程間隔1個月以上。累計總量15歲以下≤300mg/m2,15歲以上≤400mg/m2,2歲以下小兒慎用。
術前化療可使腫瘤縮小,包膜增厚,減少手術危險,避免腫瘤破潰擴散,提高完整切除率降低腫瘤臨床分期避免術後放療。但術前化療也有一些缺點,良性腫瘤可能被當作惡性腫瘤治療,其他沒有確切組織學分類的惡性腫瘤被當作腎母細胞瘤來化療。因而強調在無病理組織學診斷情況下只對手術切除困難的巨大腫瘤進行化療。
4.復發及轉移腫瘤的治療 治療包括手術、放療及化療。除上述藥物外,尚可用順鉑(DDP)、依託泊苷(足葉乙甙)等肺轉移局部照射12Gy足矣。肝臟病變可因照射引起,必須由細胞學證實方可照射,30Gy經3~4周。轉移癌化療需同時用放線菌素D、長春新鹼、ADR。
5.雙側腎母細胞瘤的治療 雙側腎母細胞瘤占4.2%前後發病占1.6%,45%患者伴其他發育異常(單側4%),間歇可長達10年。雙側腎母細胞瘤多數細胞分化好,前後發病的預後不如同時發病者。有統計,同時發病生存率達87%前後發病者則為40%因此建議經腹腔探查如為預後好的組織結構,僅做活檢,包括取淋巴結活檢,如能保留患腎在2/3以上,也可切除活檢,三藥聯用加放療15Gy(1500rad),6個月內再次手術探查,如不能切除,繼續化療,6個月內第3次手術探查,需用監測。一般不主張雙腎切除後行腎移植,預後並不比姑息治療配合化療、放療好。
療效評價
1.治癒:手術切除腫瘤後,傷口I期癒合。
2.好轉:手術後留有轉移源或切除不完全。非手術治療者腫瘤體積縮小,症狀好轉。
3.未愈:腫瘤未切除,症狀體徵未改善。
