奇特原子化學
正文
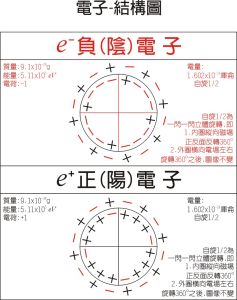 正電子-內部結構模型圖
正電子-內部結構模型圖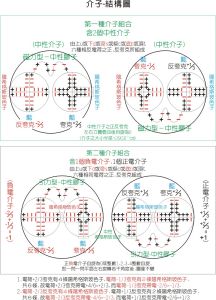 正介子、負介子-內部結構模型圖
正介子、負介子-內部結構模型圖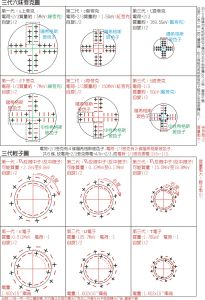 三代夸克及三代輕子-結構模型圖
三代夸克及三代輕子-結構模型圖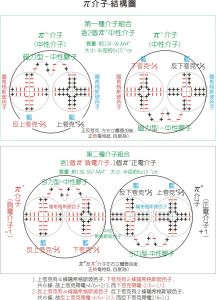 π介子-內部結構模型圖
π介子-內部結構模型圖由µ- 或π- 、K- 替換原子中的一個電子組成的奇特原子就稱為µ子原子、π介子原子、K介子原子等。
所有奇特原子都是不穩定的。它們的壽命最長不超過形成奇特原子的基本粒子在真空中的固有壽命 (τμ≈2.2×10-6 秒,τπ≈2.6×10-8 秒)。正電子本身是穩定的,但遇到電子會發生正電子湮沒;正電子素的壽命約為10-7 ~10-10 秒。
簡史 最早被證實的奇特原子是1940年發現的 µ子原子,1951年發現了正電子素,1952年證實了π介子原子發出的X射線,1960年測到了µ子素。60年代初期發現物質的化學性質對奇特原子釋放的介子 X射線譜的結構有影響,還發現一系列金屬氧化物捕獲µ- 的幾率比(等於Z/8)隨金屬原子序數Z呈周期性的變化,最小值出現在元素周期表的開始處,從而推斷化學鍵類型對奇特原子的形成和衰變有影響。至60年代中期,從實驗上肯定了奇特原子的形成幾率和隨後的衰變方式與化學環境有密切聯繫,由此發展出奇特原子化學這一新的研究領域。1970年發現了由反質子、Σ- 、Ξ- 組成的超子原子。
研究內容 該領域的研究可分兩個階段。第一階段是找出化學結構影響奇特原子的形成和衰變的規律。第二階段是根據觀測奇特原子的形成和衰變來獲取有關化學結構和化學反應動力學的新數據。在上述的奇特原子中,正電子素的研究已步入第二階段。
除了正電子來源於β+ 衰變的核素外,其他幾種粒子需要用中、高能加速器產生。正電子或用加速器產生的粒子束射入物質,經過慢化,正粒子與一個電子結合或負粒子被原子捕獲即形成奇特原子。
由µ- 、π- 等負粒子組成的奇特原子有兩個重要的特徵:①由於量子數相同時軌道半徑與軌道上粒子的質量成反比,它們的半徑比普通原子的小得多;②由於軌道能級與軌道上粒子的質量成正比,做同樣躍遷時輻射能比電子躍遷能高几百至幾千倍。形成奇特原子時,負粒子被捕獲在高激發態軌道上,隨後的躍遷過程放出一系列X射線,µ子原子釋放的X射線稱為µX射線。研究這類奇特原子化學主要靠測量這些X射線。
π- 被氫原子捕獲後與氫核發生特徵的電荷交換反應π- +p─→n+π0 ,π0 接著又放出2個光子。以此鑑定材料中的氫,其他元素干擾極小。氫的化學狀態強烈地影響其π介子原子的形成。利用π- 介子研究含氫材料的化學性質和氫鍵特徵是奇特原子化學中一個頗有實用價值的課題。
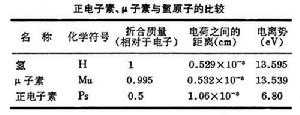
正電子素和µ子素都是類氫原子。µ+ 質量是e+ 的207倍, 所以µ子素更像氫原子(見表)。它們都具有特徵的短壽命,可以作為氫的示蹤劑。
 奇特原子化學
奇特原子化學E.Fluch and V.I.Goldanskii,et al., ed., Modern Physics in Chemistry,Vol.1,Academic Press,London, 1976.

