研究歷史
 威廉·拉姆塞
威廉·拉姆塞1868年8月18日,法國天文學家讓桑赴印度觀察日全食,利用分光鏡觀察日珥,從黑色月盤背面突出的紅色火焰,看見有彩色的彩條,是太陽噴射出來的熾熱的光譜。他發現一條黃色譜線,接近鈉光譜總的D1和D2線。日蝕後,他同樣在太陽光譜中觀察到這條黃線,稱為D3線。1868年10月20日,英國天文學家洛克耶也發現了這樣的一條黃線。
經過進一步研究,認識到是一條不屬於任何已知元素的新線,是因一種新的元素產生的,把這個新元素命名為 helium,來自希臘文helios(太陽),元素符號定為He。這是第一個在地球以外,在宇宙中發現的元素。為了紀念這件事,當時鑄造一塊金質紀念牌,一面雕刻著駕著四匹馬戰車的傳說中的太陽神阿波羅(Apollo)像,另一面雕刻著詹森和洛克耶的頭像,下面寫著:1868年8月18日太陽突出物分析。在詹遜從太陽光譜中發現氦時,英人J. N. Lockyer和E. F. Frankland認為這種物質在地球上還沒有發現,因此定名為“氦”(法文為hélium,英文為helium),源自希臘語ήλιος,意為“太陽”。
過了20多年後,拉姆賽在研究釔鈾礦時發現了一種神秘的氣體。由於他研究了這種氣體的光譜,發現可能是詹森和洛克耶發現的那條黃線D3線。但由於他沒有儀器測定譜線在光譜中的位置,他只有求助於當時最優秀的光譜學家之一的倫敦物理學家克魯克斯。克魯克斯證明了,這種氣體就是氦。這樣氦在地球上也被發現了。
在二十世紀初的幾十年里,世界各國都在尋找氦氣資源,在當時主要是為了充飛艇。但是到了二十一世紀,氦不僅用在飛行上,尖端科學研究,現代化工業技術,都離不開氦,而且用的常常是液態的氦,而不是氣態的氦。液態氦把人們引到一個新的領域——低溫世界。
英國物理學家杜瓦(Dewar)在1898年首先得到了液態氫。就在同一年,荷蘭的物理學家卡美林·奧涅斯也得到了液態氫。液態氫的沸點是零下253℃,在這樣低的溫度下,其他各種氣體不僅變成液體,而且都變成了固體。只有氦是最後一個不肯變成液體的氣體。包括杜瓦和卡美林·奧涅斯在內的科學家們和決心把氦氣也變成液體。
1908年7月13日晚,荷蘭物理學家卡美林·奧涅斯(Heike Kamerlingh Onnes昂納斯)和他的助手們在著名的萊頓實驗室取得成功,氦氣變成了液體。他第一次得到了320立方厘米的液態氦。
要得到液態氦,必須先把氦氣壓縮並且冷卻到液態空氣的溫度,然後讓它膨脹,使溫度進一步下降,氦氣就變成了液體。液態氦是一種與眾不同的液體,其沸點為零下269℃。在這樣低的溫度下,氫也變成了固體,與空氣接觸時,空氣會立刻在液態氦的表面上凍結成一層堅硬的蓋子。
1934年,在英國盧瑟福那裡學習的前蘇聯科學家卡比查發明了新型的液氦機,每小時可以製造4升液態氦。以後,液態氦才在各國的實驗室中得到廣泛的研究和套用。
含量分布
氦存在於整個宇宙中,按質量計占23%,僅次於氫。但在自然界中主要存在於天然氣體或放射性礦石中。在地球的大氣層中,氦的濃度十分低,只有5.2萬分之一。在地球上的放射性礦物中所含有的氦是α衰變的產物。氦在某些天然氣中含有在經濟上值得提取的量,最高可以含有7%,在美國的天然氣中氦大約有1%,在地表的空氣中每立方米含有4.6立方厘米的氦,大約占整個體積的0.0005%,密度只有空氣的7.2分之一,是除了氫以外密度最小的氣體。
| 地殼中含量 | 0.008(ppm) |
| 元素在太陽中的含量 | 230000(ppm) |
| 元素在海水中的含量 | 0.000006(ppm) |
地球上的氦主要是放射性元素衰變的產物,α粒子就是氦的原子核。在工業中可由含氦達7%的天然氣中提取。也可由液態空氣中用分餾法從氦氖混合氣體中製得。
物理性質
基本信息
 氦的原子光譜
氦的原子光譜元素符號He,原子序數2,原子量4.002602(氦4),為稀有氣體的一種。元素名來源於希臘文,原意是“太陽”。
 通電發光後的氦氣
通電發光後的氦氣氦有兩種天然同位素:氦3、氦4,自然界中存在的氦基本上是氦4。相對原子質量為4.003。1868年有人利用分光鏡觀察太陽表面,發現一條新的黃色譜線,並認為是屬於太陽上的某個未知元素,故名氦。氦在空氣中的含量為0.0005%。
氦在通常情況下為無色、無味的氣體;熔點-272.2℃(25個大氣壓),沸點-268.9℃;密度0.1785克/升,臨界溫度-267.8℃,臨界壓力2.26大氣壓;水中溶解度8.61厘米³/千克水。
氦是惰性元素之一,分子式為He,是一種稀有氣體,無色、無臭、無味。它在水中的溶解度是已知氣體中最小的,也是除氫氣以外密度最小的氣體。密度0.17847克/升,熔點-272.2℃(25個大氣壓)。沸點-268.9℃。它是最難液化的一種氣體,其臨界溫度為-267.9℃。臨界壓力為2.25大氣壓。當液化後溫度降到-270.98℃以下時,具有表面張力很小,導熱性很強,幾乎不呈現任何粘滯性。液體氦可以用來得到接近絕對零度(-273.15℃)的低溫。化學性質十分不活潑,既不能燃燒,也不能助燃。氦也是最難液化的氣體。
氦在通常情況下為無色、無味的氣體。是唯一不能在標準大氣壓下固化的物質。液態氦在溫度下降至2.18K時,性質發生突變,成為一種超流體,能沿容器壁向上流動,熱傳導性為銅的800倍,並變成超導體;其比熱容、表面張力、壓縮性都是反常的。
由於液氦的超低溫,在此溫度下出現了許多奇妙的物理現象。許多重要的物理實驗,都要在低溫下進行。世界各國的物理學家都在研究液態氦,希望通過液態氦達到更低的溫度,研究各種物質在低溫下會發生什麼變化,會有什麼我們還不知道的性質。這就產生了物理學的一個新的分支——低溫物理學。
| 熔點 | -272.2℃(25個大氣壓); |
| 沸點 | -268.9℃; |
| 密度 | 0.1785克/升 |
| 臨界溫度 | -267.8℃ |
| 臨界壓力 | 2.26大氣壓 |
| 水中溶解度 | 8.61立方厘米/千克水 |
| 熱導率 | 151.3W/(m·K) |
| 晶體結構 | 晶胞為六方晶胞 |
氦-4
下表為液氦(氦4)的一些基本物理性質(某些參數測定時的狀態不詳):
| 正常沸點/K | 4.224 |
| 密度/kg/m³ | 124 96 |
| 蒸發熱/kJ/kg | 20.73 |
| 比熱/kJ/(kg·K) | 4.56 |
| 粘度/MPa·s | 3.57 |
| 熱導率/mW/(m·K) | 2.72 |
| 介電常數 | 1.0492 |
| 臨界溫度/K | 5.201 |
| 臨界壓力/MPa | 0.227 |
氦-3
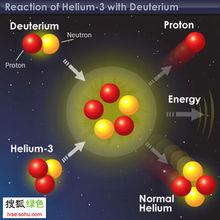 氦-3
氦-3氦3是自然界中氦的穩定同位素,原子量為3.016,原子核由2個質子和一個中子組成。通常情況下,氦3為無色、無味、無毒、不燃燒的惰性氣體,在0℃及0.101325MPa下密度是0.1345kg/m 。
下表為液氦(氦3)的一些基本物理性質:
| 正常沸點/K | 3.191 |
| 密度/kg/m³ | 82.3 |
| 蒸發熱/J/mol | 20.56 |
| 1.0K時的比熱/J/(mol·K) | 4.222 |
| 3.2K時的粘度/mPa·s | 3.57 |
| 3.2K時的熱導率/mW/(m·K) | 20 |
| 臨界溫度/K | 3.324 |
| 臨界壓力/MPa | 0.115 |
超流動性
卡美林·奧涅斯是第一個得到液氦的科學家。他又將溫度進一步降低,試圖得到固態氦,卻並沒有成功(固態氦是1926年基索姆用降低溫度和增大壓力的方法首先得到的)。
對於一般液體來說,隨著溫度降低,密度會逐漸增加。卡美林·奧涅斯使液態氦的溫度下降,液氦的密度增大了。但是,當溫度下降到零下271℃的時候,液態氦突然停止起泡,同時密度也突然減小了。
這是另一種液態氦。卡美林·奧涅斯把前一種冒泡的液態氦叫做氦Ⅰ,而把後一種靜止的液態氦叫做氦Ⅱ。
把一個小玻璃杯按在氦Ⅱ中。玻璃杯由空的漸漸裝滿了。把這個盛著液態氦的小玻璃杯提出來,掛在半空時,玻璃杯底下出現了液氦,不一會,杯中的液態氦就“漏”光了。
氦Ⅱ能夠倒流,它會沿著玻璃杯的壁向高處倒流。此現象只能在低溫狀態下才會發生,名為“超流動性”,具有“超流動性”的氦Ⅱ叫做超流體。
後來,許多科學家研究了這種怪現象,又有了許多新的發現。比如1938年阿蘭等人發現的氦刀噴泉。在一根玻璃管里,裝著很細的金剛砂,上端接出來一根細的噴嘴。將這玻璃管浸到氦Ⅱ中,用光照玻璃管粗的下部,細噴嘴就會噴出氦Ⅱ的噴泉,光越強噴得越高,可以高達數厘米。
氦Ⅱ噴泉也是超流體的特殊性質。在這個實驗中,光能直接變成了機械能。
超導現象
在液氦的溫度下,在一個鉛環上放置一個鉛球。鉛球會好像失重而飄浮在環上,與環保持一定距離。在同樣的溫度下,用細鏈子繫著磁鐵,慢慢放到一個金屬盤子裡去。當磁鐵快要碰到盤子的時候,可以觀察到,鏈子鬆了,磁鐵浮在盤子上,若此時輕輕拍打磁鐵,它會自行鏇轉。這種現象只能在低溫觀察到,高溫下不會產生。
這是低溫下的超導現象。有些金屬在液態氦的溫度下,原子核的運動幾乎停止,對電子的阻礙變得極小,因此電阻會消失,成為超導體;由於磁力線不可能穿過超導體 ,於是在超導體與磁體中間形成了較大的磁場,磁場的斥力托住了鉛球和磁鐵,使它們浮在半空中。這就是邁斯納效應(Meissner Effect),這一效應可以被利用來製造磁懸浮列車。
化學性質
 元素周期性質
元素周期性質氦是所有元素中最不活潑的元素,極難形成化合物,這是因為氦的原子核到電子層距離很小,並且達到了穩定結構。它的性質便決定了用途,氦的套用主要是作為保護氣體、氣冷式核反應堆的工作流體和超低溫冷凍劑等等。
2017年2月6日,中國南開大學的王慧田、周向鋒團隊及其合作者在《Nature Chemistry》上發表了有關在高壓條件下合成氦鈉化合物——Na2He的論文 ,結束了氦元素無化合物的歷史,標誌著我國在稀有氣體化學領域走到了最前沿。
氟化物製取猜想
Pimental等根據HeF₂的電子排布同穩定的HF₂⁻相似,提出了利用核轉變製備HeF₂的三種方法。
1.氚的β衰變法
氚經過β衰變後應變成氦。這樣,氚的化合物經β衰變後,就有可能成為氦化合物。為了便於進行反應,首先通過氘和氫的同位素交還,將氘固定在KHF₂的固體晶格中。俘集在晶格中的TF₂⁻發生核反應後,便會生成HeF₂。
TF₂⁻ → HeF₂ +β⁻
氘在衰變過程中的反衝能量,不致使新生成的二氟化氦斷鏈。氘衰變的半衰期為12.25年,估計¹⁰Ci的氚,經4~5個月,僅能生成10μmol的HeF₂ .
2.熱中子輻照法
用熱中子輻照LiF來產生核反應
₃⁶Li + ₀¹n → ₂⁴He + ₁³T
Li(n,α)反應後,生成的氦核同母體晶格中的F 相結合而生成HeF₂.
3.直接用α粒子轟擊固態氟來製備HeF₂
由此看來,這三種方法中,以第一種方法製成HeF₂的可能性最大,但至今還沒有見到已製成的報告。Malm等認為HeF₂和HF₂⁻的電子排布雖然相似,但HF₂⁻是H⁻同兩個F原子相作用而生成化合物,H⁻的電離勢僅為0.7eV,而氦的電離勢高達25eV,因此對HeF₂是否存在是值得懷疑的。
離子化合物
氦合氫離子,化學式為HeH⁺,是一個帶正電的離子。它首次發現於1925年,通過質子和氦原子在氣相中反應製得。它是已知最強的酸,質子親和能為177.8 kJ/mol。這種離子也被稱為 氦氫分子離子。有人認為,這種物質可以存在於自然星際物質中。這是最簡單的異核離子,可以與同核的氫分子離子H₂相比較。與H₂不同的是,它有一個永久的鍵偶極矩,使它更容易表現出光譜特徵。
HeH⁺不能在凝聚相中製備,因為這會使它與任何陰離子、分子、原子發生作用。但是,可以用蓋斯定律預測它在水溶液中的酸性。
電離過程-360 kJ/mol的自由能變化相當於p Ka為-63。
HeH中共價鍵的長度是0.772Å。
其他氦氫離子已經知道或者在理論上研究。HeH₂,已經被微波光譜觀測到,科學家計算出它的親和能為6 kcal/mol,而HeH₃為0.1 kcal/mol。
中性分子
不同於氦合氫離子,氫和氦構成的中性分子在一般情況下是很不穩定的。但是,它作為一個準分子在激發態是穩定的,於20世紀80年代中期首次在光譜中觀測到。
pka:-63(推測),比氟銻酸強得多。
| HHe( g) | → | H( g) | + He( g) | +178 kJ/mol |
| HHe( aq) | → | HHe( g) | +973 kJ/mol | |
| H( g) | → | H( aq) | – 1530 kJ/mol | |
| He( g) | → | He( aq) | +19 kJ/mol | |
| HHe( aq) | → | H( aq) | + He( aq) | – 360 kJ/mol |
即便如此,這些離子或分子僅出現於“瞬間”,或者僅通過計算得出,故它們尚且難以認為是存在的“化合物”。
氦鈉化合物
2017年2月6日,中國南開大學的王慧田、周向鋒團隊及其合作者在《Nature Chemistry》上發表了有關在高壓條件下合成氦鈉化合物——NaHe的論文 ,結束了氦元素無化合物的歷史,標誌著我國在稀有氣體化學領域走到了最前沿。
此前,研究人員已經找到其他元素與氦進行配對的方法。但一直以來,都沒有形成什麼能夠穩定存在的物質。最常見的例子就是氦與其他元素的范德華力,無需共價鍵或者離子鍵就可以存在。在極低的溫度下,氦確實可以形成范德華力,但極其微弱,無法長久保持。
氦元素堅固的穩定力源於其閉殼層電子組態:其外殼層是完滿的狀態,沒有空間和其他原子通過共用電子進行結合。不過這是地球表面環境中的情況。
作為宇宙中第二豐富的元素,氦在恆星和巨型氣體行星的構成中起著重要作用。在外太空或者地球深處的極端條件下,它可能遵循著不同尋常的規律。如今,研究人員剛剛驗證這種奇異的現象。
猶他州立大學的文章共同作者Alex Boldyrev說:“極高的壓力,比如在地球的核心或者其他巨型星體中,能夠完全改變氦的化學特性。”
研究人員通過“晶體結構預測”模型進行演算發現,在極度的壓力之下,一種穩定的氦鈉化合物能夠形成。然後他們在金剛石壓腔實驗中真的創造出了前所未見的化合物:NaHe。實驗可以為氦和鈉原子提供相當於110萬倍地球大氣壓的條件。
這一結果太出人意料,因此發表的時候遇到了巨大的困難,研究人員花了兩年多的時間去說服審稿人和編輯。
基於這些結果,研究團隊預測,如果壓力達到他們實驗水平的一千萬倍,那么鈉將可以很容易地和氦氣反應生成穩定的NaHe。更為奇妙的是,這種化合物的構成並不需要任何化學鍵。
南開大學王慧田教授是本次研究的共同通訊作者,據他介紹:“所發現的化合物非常奇特:氦原子通常不會形成任何化學鍵,而新物質的存在從根本上改變了鈉原子間的化學相互作用,迫使電子集中在該結構的立方空間內,同時具有絕緣能力。”
![氦[化學元素]](/img/9/0e7/wZwpmLyEDM1MzMxcTMxMDN0UTMyITNykTO0EDMwAjMwUzL3EzL1gzLt92YucmbvRWdo5Cd0FmLzE2LvoDc0RHa.jpg) 氦[化學元素]
氦[化學元素]NaHe的晶體結構,由鈉原子(紫色)和氦原子(綠色)交替,共用電子(紅色)存在於其間的區域。
“這並不是真的化學鍵,”Popov說,“但是氦能夠使這一結構穩定存在。如果你把氦原子挪走,該結構將無法保持穩定。”
下面是該化合物的其他表現形式,左圖中粉色為鈉,白色為氦;右圖中鈉和氦成立方體狀,紅色的點則是電子。
![氦[化學元素]](/img/c/056/wZwpmLzUDN4gzNxEDNxMDN0UTMyITNykTO0EDMwAjMwUzLxQzL0czLt92YucmbvRWdo5Cd0FmLwE2LvoDc0RHa.jpg) 氦[化學元素]
氦[化學元素]亞晶格分析表明,He的占位導致電子被局域到了原子縫隙中並在Na原子核的引力下形成多中心鍵,從而整個體系變成了電子鹽體系。該過程中,孤立電子,Na的內層電子與He的內層1s電子和外層的2s,2p軌道產生強烈的交疊。受泡利不相容原理的影響,He的1s電子密度和外層電子軌道的分布被迫發生變化導致在NaHe形成過程中He得到了0.15個電子。該工作證實了高壓下He會具有弱的化學活性能夠與在高壓下還原性顯著增強的Na形成化合物。
雖然最近關於金屬氫的突破研究遇到很大的質疑,但這篇文章的數據要紮實很多。來自倫敦帝國學院的物理學家Henry Rzepa在把這項研究和金屬氫的發現對比時表示:“這是更為可靠的科學,氦化合物是一項重大突破。”
這一研究涉及中、美、俄、意、德五國學者。參與的中國研究單位還有北京高壓科學研究中心、西北工業大學、中科院固態物理研究所和南京大學。特別值得一提的是,這一研究開始於南開大學研究生Xiao Dong在美國交換訪問期間,根據作者貢獻介紹,Xiao Dong設計了研究工作、並展開了相關計算。Xiao Dong目前已經在上海高壓科學研究中心工作。
據了解,這一工作2013年就投稿Nature,但作者與評審人就NaHe成健性質無法達成一致,最後改投Nature Chemistry發表。當然,並不是所有人都被說服。愛丁堡大學Eugene Gregoryanz就認為XRD數據有待提高,最終還要看這一工作是否能被其他團隊所重複。不過,具備條件的實驗室全世界沒有幾家。
同位素
已知的氦同位素有八種,包括氦3、氦4、氦5、氦6、氦8等,但只有氦3和氦4是穩定的,其餘的均帶有放射性。在自然界中,氦同位素中以氦4占最多,多是從其他放射性物質的α衰變,放出氦4原子核而來。而在地球上,氦3的含量極少,它們均是由超重氫(氚)的β衰變所產生。
氦-2:它的原子核只有2個質子,到目前為止只是假想粒子,但如果強核力增強2%,它就有可能存在。
氦-5,是氦的同位素之一,元素符號為He。它的原子核由二顆質子和三顆中子所組成。並帶有放射性,會放出中子,其半衰期為0.6 MeV。
氦-6:原子核包含2個質子和4箇中子,非常不穩定。
氦-7:原子核包含2個質子和5箇中子,會衰變成氦-6,非常不穩定。
氦-8:原子核包含2個質子和6箇中子,非常不穩定。
氦-9:原子核包含2個質子和7箇中子,非常不穩定。
氦-10:原子核包含2個質子和8箇中子,非常不穩定。
| 符號 | Z(p) | N(n) | 同位素質量(u) | 半衰期 | 原子核自鏇 | 相對豐度 | 相對豐度的變化量 |
| He | 2 | 0 | 2.02946 # | 非常不穩定(假想粒子) # | 0+ #(推測) | 0 | 未知 |
| He | 2 | 1 | 3.0160293191(26) | 穩定 | 1/2+ | 0.00000134(3) | 4.6×10-0.000041 |
| He | 2 | 2 | 4.002,603,254,15(6) | 穩定 | 0+ | 0.99999866(3) | 0.999959-1 |
| He | 2 | 3 | 5.01222(5) | 700(30)E-24 s [0.60(2) MeV] | 3/2- | ||
| He | 2 | 4 | 6.0188891(8) | 806.7(15) ms | 0+ | ||
| He | 2 | 5 | 7.028021(18) | 2.9(5)E-21 s [159(28) keV] | (3/2)- | ||
| He | 2 | 6 | 8.033922(7) | 119.0(15) ms | 0+ | ||
| He | 2 | 7 | 9.04395(3) | 7(4)E-21 s [100(60) keV] | 1/2(-#) | ||
| He | 2 | 8 | 10.05240(8) | 2.7(18)E-21 s [0.17(11) MeV] | 0+ |
備註:畫上#號的數據代表沒有經過實驗的證明,只是理論推測而已,而用括弧括起來的代表數據不確定性。
製取方法
天然氣分離法:工業上,主要以含有氦的天然氣為原料,反覆進行液化分餾,然後利用活性炭進行吸附提純,得到純氦。合成氨法:在合成氨中,從尾氣經分離提純可得氦。
空氣分餾法:從液態空氣中用分餾法從氖氦混合氣中提出。
鈾礦石法:將含氦的鈾礦石經過焙燒,分離出氣體,再經過化學方法,除去水蒸氣、氫氣和二氧化碳等雜質提純出氦。
作用用途
 氦氖雷射治療儀
氦氖雷射治療儀 用途
用途由於氦很輕,而且不易燃,因此它可用於填充飛艇、氣球、溫度計、電子管、潛水服等。也可用於原子反應堆和加速器、雷射器、火箭、冶煉和焊接時的保護氣體,還可用來填充燈泡和霓虹燈管,也用來製造泡沫塑膠。
由於氦在血液中的溶解度很低,因此可以加到氧氣中防止減壓病,作為潛水員的呼吸用氣體,或用於治療氣喘和窒息。
液體氦的溫度(-268.93 ℃)接近絕對零度(-273℃),因此它在超導研究中用作超流體,製造超導材料。液態氦還常用做冷卻劑和製冷劑。在醫學中,用於氬氦刀以治療癌症。它還可以用作人造大氣層和鐳射媒體的組成部分。
危險性
引起窒息
如果大量吸入氦氣,會造成體內氧氣被氦取代,因而發生缺氧(呼吸反射是受體內過量二氧化碳驅動,而對缺氧並不敏感),嚴重的甚至會死亡。 另外,如果是由高壓氣瓶中直接吸入氦氣,那么其高流速就會嚴重地破壞肺部組織。大量而高壓的氦和氧會造成高壓緊張症狀High pressure nervous syndrome (HPNS),不過少量的氮就能夠處理這個問題。而空氣中百分之七十八都是氮氣,所以不用擔心。據介紹,大量及長時間吸入氦氣可導致腦損傷甚至死亡。在大部分薯條類包裝袋裡也含有少量氦氣,不過不必擔心,沒有危害。
安全事項-氦氣瓶
壓力通常有15MPa,使用時套用YQY-12或152IN-125等減壓器減壓後使用,使用前套用肥皂水檢漏氣體管道,確保氣體管道不漏氣。
確保氦氣不泄露、工作場所保持通風。
包裝的氣瓶上均應記上生產日期、包括使用年限,凡到期的氣瓶必須送往有部門進行安全檢驗,方能繼續使用。
每瓶氦氣在使用到尾氣時,應保留瓶內余壓在0.5MPa,最小不得低於0.25MPa余壓,應將瓶閥關閉,以保證氣體質量和使用安全。
瓶裝氦氣在運輸儲存、使用時都應分類堆放。
不準靠近明火和熱源,應做到勿近火、勿沾油臘、勿爆曬、勿重拋、勿撞擊,嚴禁在氣瓶身上進行引弧或電弧。
嚴禁野蠻裝卸,短距離移動氦氣鋼瓶應使用鋼瓶專用手推車,長距離移動鋼瓶套用危險品運輸車輛運輸。
液氦的溫度為-268.9℃,與皮膚接觸能引起嚴重凍傷。
1.壓力通常有15MPa,使用時套用YQY-12或152IN-125等減壓器減壓後使用,使用前套用肥皂水檢漏氣體管道,確保氣體管道不漏氣。
2.確保氦氣不泄露、工作場所保持通風。
3.包裝的氣瓶上均應記上生產日期、包括使用年限,凡到期的氣瓶必須送往有部門進行安全檢驗,方能繼續使用。
4.每瓶氦氣在使用到尾氣時,應保留瓶內余壓在0.5MPa,最小不得低於0.25MPa余壓,應將瓶閥關閉,以保證氣體質量和使用安全。
5.瓶裝氦氣在運輸儲存、使用時都應分類堆放。
6.不準靠近明火和熱源,應做到勿近火、勿沾油臘、勿爆曬、勿重拋、勿撞擊,嚴禁在氣瓶身上進行引弧或電弧。
7.嚴禁野蠻裝卸,短距離移動氦氣鋼瓶應使用鋼瓶專用手推車,長距離移動鋼瓶套用危險品運輸車輛運輸。
8.液氦的溫度為-268.9℃,與皮膚接觸能引起嚴重凍傷。
氦氣對人體的不良反應
當身體內的氦氣含量增加導致氧氣含量低於19.5%時,患者先出現呼吸加快、注意力不集中、共濟失調;繼之出現疲倦無力、煩躁不安、噁心、嘔吐、昏迷、抽搐,以致死亡。
化學元素周期表
| 族→ | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 電子層 | 0族電子數 | |
| 周期↓ | I A | 0 | |||||||||||||||||||
| 1 | 1 H 氫 | 2 He 氦 | K | 2 | |||||||||||||||||
| II A | III A | IV A | V A | VI A | VII A | ||||||||||||||||
| 2 | 3 Li 鋰 | 4 Be 鈹 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 | L K | 8 2 | |||||||||||
| 3 | 11 Na 鈉 | 12 Mg 鎂 | 13 Al 鋁 | 14 Si 矽 | 15 P 磷 | 16 S 硫 | 17 Cl 氯 | 18 Ar 氬 | M L K | 8 8 2 | |||||||||||
| III B | IV B | V B | VI B | VII B | VIII | I B | II B | ||||||||||||||
| 4 | 19 K 鉀 | 20 Ca 鈣 | 21 Sc 鈧 | 22 Ti 鈦 | 23 V 釩 | 24 Cr 鉻 | 25 Mn 錳 | 26 Fe 鐵 | 27 Co 鈷 | 28 Ni 鎳 | 29 Cu 銅 | 30 Zn 鋅 | 31 Ga 鎵 | 32 Ge 鍺 | 33 As 砷 | 34 Se 硒 | 35 Br 溴 | 36 Kr 氪 | N M L K | 8 18 8 2 | |
| 5 | 37 Rb 銣 | 38 Sr 鍶 | 39 Y 釔 | 40 Zr 鋯 | 41 Nb 鈮 | 42 Mo 鉬 | 43 Tc 鎝 | 44 Ru 釕 | 45 Rh 銠 | 46 Pd 鈀 | 47 Ag 銀 | 48 Cd 鎘 | 49 In 銦 | 50 Sn 錫 | 51 Sb 銻 | 52 Te 碲 | 53 I 碘 | 54 Xe 氙 | O N M L K | 8 18 18 8 2 | |
| 6 | 55 Cs 銫 | 56 Ba 鋇 | 57- 71 鑭系 | 72 Hf 鉿 | 73 Ta 鉭 | 74 W 鎢 | 75 Re 錸 | 76 Os 鋨 | 77 Ir 銥 | 78 Pt 鉑 | 79 Au 金 | 80 Hg 汞 | 81 Tl 鉈 | 82 Pb 鉛 | 83 Bi 鉍 | 84 Po 釙 | 85 At 砹 | 86 Rn 氡 | P O N M L K | 8 18 32 18 8 2 | |
| 7 | 87 Fr 鍅 | 88 Ra 鐳 | 89- 103 錒 | 104 Rf 鑪 | 105 Db | 106 Sg | 107 Bh | 108 Hs | 109 Mt | 110 Ds 鐽 | 111 Rg 錀 | 112 Uub | 113 Uut | 114 Uuq | 115 Uup | 116 Uuh | 117 Uus | 118 Uuo | |||
| 鑭系元 素 | 57 La 鑭 | 58 Ce 鈰 | 59 Pr 鐠 | 60 Nd 釹 | 61 Pm 鉕 | 62 Sm 釤 | 63 Eu 銪 | 64 Gd 釓 | 65 Tb 鋱 | 66 Dy 鏑 | 67 Ho 鈥 | 68 Er 鉺 | 69 Tm 銩 | 70 Yb 鐿 | 71 Lu 鑥 | ||||||
| 錒系元 素 | 89 Ac 錒 | 90 Th 釷 | 91 Pa 鏷 | 92 U 鈾 | 93 Np 鎿 | 94 Pu 鈽 | 95 Am 鎇 | 96 Cm 鋦 | 97 Bk 錇 | 98 Cf 鐦 | 99 Es 鑀 | 100 Fm 鐨 | 101 Md 鍆 | 102 No 鍩 | 103 Lr 鐒 | ||||||
![氦[化學元素] 氦[化學元素]](/img/b/1f1/nBnauM3XzETMyYTM5gjM5EDN0UTMyITNykTO0EDMwAjMwUzL4IzLwczLt92YucmbvRWdo5Cd0FmLyE2LvoDc0RHa.jpg)
