學科簡介
 核化學
核化學核化學,又稱為核子化學,是用化學方法或化學與物理相結合的方法研究原子核(穩定性和放射性)的反應、性質、結構、分離、鑑定等的一門學科。例如,研究不同的次原子粒子怎樣共同形成一個原子核以及研究原子核之中的物質究竟是如何變化的。
早期歷史
 核
核究把放射線離子化。他們的其中之一就是亨利·貝克勒爾,他研究磷光與相片板變黑的關係。當貝克勒爾(在法國工作)發現這個時,沒有其他能量來源,鈾產生了射線可以令相片板變黑,放射線被發現。瑪麗亞·居里(在巴黎工作)與她的丈夫皮埃爾·居里從鈾離析了兩種新的放射性元素。他們用輻射來識別哪一種是化學離析後放射線的光束;他們把鈾離析至各不同已知的化學元素,並量度各元素的放射線。之後他們試圖更進一步地離析這些放射性級分去離析一種更活躍的更小的級分。就這樣他們離析出了釙和鐳。大約1901年,人們發現吸收過多輻射會在人體造成傷害,貝克勒爾常在袋中帶著一個鐳的樣本,他吸收了過多輻射,因而造成輻射灼傷。
核化學起始於1898年M.居里和P.居里對釙和鐳的分離和鑑定。後來30年左右的時間內,通過大量化學上的分離和鑑定,以及物理上探測α、β和γ射線等技術的發展,確定了鈾、釷和錒的三個天然放射性衰變系,指數衰變定律,母子體生長衰變性質(見放射性衰變規律),明確了一個元素可能具有不止一個核素的同位素概念,以及同一核素的不同能態鏤Z和UX2的同質異能素)等事實。此外,還陸續找到了其他十幾種天然放射性元素。
1919年E.盧瑟福等發現由天然放射性核素髮射的 α粒子引起的原子核反應,導致1934年F.約里奧-居里和I.約里奧-居里製備出第一個人工放射性核素磷30。由於中子的發現和粒子加速器的發展,通過核反應產生的人工放射性核素的數目逐年增加,而1938年O.哈恩等發現原子核裂變更加速了這種趨勢,並且為後來的核能利用開闢了道路。此外,核譜學(包括α、β、γ和X射線譜學)的工作也有相應的發展。由於粒子加速器、反應堆、各種類型的探測器和分析器、質譜儀、同位素分離器及計算機技術等的發展,核化學研究的範圍和成果還在繼續擴展和增加,如質量大於氦核的重離子引起的深度非彈性散射反應研究,107、108、109號元素的合成,雙質子放射性和碳放射性的發現等。另外,核化學與核技術套用於化學、生物學、醫學、地學、天文學和環境科學等方面,已取得了令人矚目的進展。
研究範圍
 原子核/核子-內部結構模型圖
原子核/核子-內部結構模型圖 核化學主要研究核性質、核結構、核轉變的規律以及核轉變的化學效應、奇特原子化學,同時還包括有關研究成果在各個領域的套用。核化學、放射化學和核物理,在內容上既有區別卻又緊密地聯繫和交織在一起。
 核化學武器內部聚變
核化學武器內部聚變1.核性質
核有不穩定和穩定之分,前者又稱放射性核,放射性核經過衰變(如發射氦核、電子、光子、中子或質子,俘獲電子和自發裂變等)最終成為穩定核。任何衰變過程必須遵從能量守恆、動量守恆、角動量守恆和量子力學方面的一些規則。核的不穩定性有程度上的差別,它表現為壽命或半衰期的長短(見放射性壽命),壽命越短,不穩定性越高,反之亦然(見核穩定性)。
除了衰變方式和穩定性外,核的其他性質有電荷、質量(包括能量)、半徑、自鏇、磁矩、電四極矩、宇稱和統計性質等。另外,核不僅可處於相對穩定的基態,還可以處於能量稍高的激發態。處於激發態的核也有以上各種性質,一般以發射光子的方式到達基態。核性質反映了核的結構,通過對核性質的研究,可以更深入地認識原子核的本質。
2.核結構
原子核的結構對於原子核的變化起著決定性的作用。通過研究核結構的各類實驗數據,為核能的利用提供了可靠的基礎。核結構研究的依據及出發點是核物理實驗,包括原子核的自發衰變和裂變的實驗和核反應實驗。核結構研究中基本問題是核力、運動方程和多體問題。
3.核轉變
包括原子核在其他原子核或粒子作用下發生的各種變化(即核反應)和不穩定的原子核自發發生的核衰變。核反應是取得新核的主要途徑。
反應堆產生的中子引起的核反應是新核的一個重要來源,它主要包括中子俘獲反應和中子裂變反應(見裂變化學)。這些反應產生的裂片核(包括尚未發現的新核)都處於β穩定線的豐中子的一面,並以發射電子(或隨後再發射一個中子,稱緩發中子)的方式衰變(見新核素的合成)。
新核還可以用各類加速器所產生的不同能量的離子(氫一直到鈾)和電子以及由核反應所產生的次級粒子(如快中子、光子、π介子和μ子等)轟擊各種靶核來產生。根據轟擊粒子的不同可將核反應分為中子核反應、帶電粒子核反應、光核反應和重離子核反應等。按轟擊粒子的能量又可將它們分為高、中和低能核反應。每個核子的能量高於 10電子伏的粒子稱為高能粒子,10~10電子伏的為中能粒子,10電子伏以下的為低能粒子。但是,這類規定並不絕對,對於各種轟擊粒子如重離子、電子和次級粒子,能量高低的含義有所不同(見低能核化學、高能核化學)。這些由加速器產生的核多處於β穩定線缺中子的一面,並以發射正電子(或隨後再發射一個質子,稱緩發質子)、俘獲電子或發射質子的方式衰變。
根據以上兩種途徑,已找到2000多種不穩定核素,但仍有很多尚待發現。它們的壽命極短,需要產物核的快速傳輸、快速化學分離和線上(指在產物核產生的同時)同位素分離(原理同質譜儀)技術才能鑑定它們。重離子核反應是發現新元素的主要途徑(見重離子核化學)。
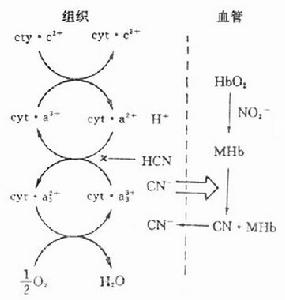 毒理作用核化學武器
毒理作用核化學武器此外,對核反應的研究還包括測量各種核反應截面及其與轟擊粒子的能量的關係(稱激發函式),測量出射粒子和產物核的質量、電荷、能量和角度(方向)的分布情況,並由此探索核反應的機理。這是深入了解核力和核子在核內運動和相互作用規律的重要方法。
4.核轉變的化學效應,即熱原子化學。
在核轉變中,產物核由於動量守恆獲得反衝動能,這一能量足以使起始核所屬原子與周圍原子之間的化學鍵斷裂,從而形成脫離原來分子的具有一定動能的熱原子。在核衰變中,有時會因電子震脫或空穴級聯而引起化學變化(見核衰變化學)。核轉變過程中產生的熱原子與周圍介質之間所起的化學變化就是熱原子化學研究的內容。
5.奇特原子化學
普通原子中的電子或質子被其他基本粒子代替後形成奇特原子,如正電子素和μ子素等。奇特原子化學主要研究化學環境對奇特原子的影響,並利用奇特原子來研究物質結構和化學反應。
學科特點
核化學研究中所用的化學操作和分離技術與一般化學分析中所用的有所不同,這主要在於前者著重速度快和放射性純度高,一般回收率在20%~50%即可。對半衰期極短的核素,為了爭取速度而允許回收率低於20%。原則上,一般化學分析中的分離方法都可用於核化學研究,但對半衰期短的核素,需採取熱色譜、反衝技術等快速分離步驟。放射性純度是指最終產品中放射性雜質與待測放射性核素之間的相對含量。放射性雜質的相對含量越低,則放射性純度越高。只要不影響回收率的測定,對化學純度的要求不高(見放射化學純度)。
一般樣品中放射性物質的質量極微,為了測定回收率和便於純化,常須加入一定量(如10~20毫克)的待測核素的穩定同位素作為載體。另外,為了提高產品的放射性純度有時需要加入雜質元素作為反載體和採用清除劑,進行反覆沉澱以提高產品的放射性純度。為了製備高比活度的或無穩定同位素的產品,必須採用化學性質相似的非同位素載體,並在最後的分離步驟中將它們除去。在定量測定方面,核化學研究中採用放射性測量。樣品的製備,特別是面密度低於100微克/厘米的極薄樣品的製備,以及各種計數技術的設計使用至關重要。
武器套用
核化學研究成果已廣泛套用於各個領域。例如利用測定由中子俘獲 A(n, γ)B反應的中子活化分析,可較準確地測定樣品中50種以上元素的含量,並且靈敏度一般很高;該法已廣泛套用於材料科學、環境科學、生物學、醫學、地學、宇宙化學、考古學和法醫學等領域。一些短壽命(特別是發射正電子)核素的放射性標記化合物廣泛套用於醫學。熱原子化學方法可用於製備某些標記化合物。正電子湮沒技術已用於材料科學及化學動力學等方面的研究。
 核化學武器的套用
核化學武器的套用核化學武器是隨著這三種武器的相繼出現與發展而形成的。第一次世界大戰期間,德軍首先對英、法聯軍使用化學武器,使對方傷亡1.5萬人。隨後,交戰國爭相使用化學武器,其防護措施也不斷完善(見化學防護)。第二次世界大戰期間,某些國家秘密地加強了生物武器的研製。日軍在侵華戰爭中,除使用化學武器外,也使用過生物武器。許多國家的軍隊在重視防化學武器的同時,增加了對生物武器的防護(見生物武器防護)。1945年8月6日和9日,美軍在日本 廣島和長崎使用了核子彈,造成很大的傷亡和破壞。各國軍隊又相繼展開了防核武器的研究(見核防護)。由於核、化學、生物武器既可分別使用,也可結合使用,在防護的組織和措施方面又有許多共同之處,因此,通常把防這三種武器聯繫在一起,簡稱“三防”。
核化學武器有巨大的殺傷破壞威力,可用飛彈、火箭、飛機、火炮等多種投射工具廣泛使用於戰場。因此,在現代條件下作戰,對這三種武器的防護,已成為作戰保障的重要內容。許多國家的軍隊都很重視研究和採取相應的措施,加強軍隊和軍事設施的防護能力,並編有專業部門、專業人員和專業部隊、分隊,負責指導部隊防護,遂行各種專業保障任務。

