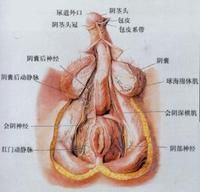
概述
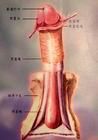 陰莖纖維性海綿體炎
陰莖纖維性海綿體炎病因學
病因不甚明了。60年代曾認為是陰莖白膜和勃起組織之間的血管周圍炎症。然而,抗炎治療並不奏效。目前認為,陰莖斑塊是瘢痕,不是炎症是自身免疫過程的結果。調節膠原合成的各種內源性和外源性因子,例如:抗壞血酸因子、EGF、IGF等,對陰莖纖維性海綿體炎發病起到重要作用。TGF-β作為細胞因子影響細胞外基質沉積,可誘發陰莖白膜纖維化。
發病原因
1.創傷 創傷是Peyronie病的促進因子。許多作者已經闡述了敏感個體在性交過程中造成的陰莖創傷可發展成Peyronie病。Kadioglu等報導Peyronie病與陰莖血管疾病及勃起功能障礙有關:該作者調查了136例Peyronie病患者,76.5%有陰莖血管異常;而自訴有勃起障礙史的患者中87.5%有陰莖血管異常,動脈病變使陰莖勃起硬度下降,易患Peyronie病。有些病人經尿道前列腺切除術TURP後出現Peyronie病,陰莖彎曲的機制同樣適合這些病人,但造成陰莖彎曲損傷的原因是因為術後常規留置粗口徑導尿管,當陰莖夜間勃起時易造成上述損傷。除了陰莖彎曲損傷,其他外力因素對白膜組織的創傷也可能導致相同結果。有些車禍或工傷事故直接導致陰莖創傷,也可逐漸發展成類似於Peyronie病的病變。而有部分病人否認性交或其他誘因引起的陰莖損傷病史,這些人群的確切發病機制尚不清楚。2.其他可能原因
(1)遺傳因素:Perichery等首次發現斑塊細胞3、8、9號染色體的微衛星不穩定性(MSI)和雜合型缺失(LOH)發生頻率很高,推測Peyronie病的發生與此有關。
(2)免疫因素:Schiavino等檢測64個Peyronie病人的淋巴細胞轉化試驗、血清IgA、IgG、IgM、抗DNA抗體、抗核抗體、抗平滑肌細胞抗體、C3、C4補體片段、抗鏈球菌溶血素以及C-反應蛋白滴度,發現75.8%病人至少有一項異常,而對照組僅10%異常。
發病機制
1966年,Smith描述了Peyronie病的病理學,認為病損是由於位於勃起組織與白膜之間的間隙(該間隙被稱為Smith間隙)中的血管周圍炎症所引起。組織學顯示該間隙中有炎症存在,有時這種炎症也可見於Bucks筋膜中及筋膜下。至今已證明病損的斑塊是瘢痕組織。Somers1997年用Peyronie病斑塊、Dupuytren攣縮結節和正常人的陰莖海綿體白膜組織(對照組)做膠原、彈性蛋白纖維結構及分布的研究,發現32/33(97%)Peyronie病斑塊有顯著的膠原染色,31/33(94%)彈性纖維斷裂,18/19例斑塊組織中有纖維蛋白沉積(免疫斑點試驗證實),而對照組未發現纖維蛋白沉積;7/8Dupuytren攣縮結節中也見到顯著的膠原染色和纖維蛋白沉積。斑塊組織中纖維蛋白沉積的事實與反覆的微血管損傷引起組織間隙纖維蛋白沉積的理論相符。Mulhall等測定病人的斑塊組織和包皮中的b-FGF(鹼性成纖維細胞生長因子),發現斑塊中的b-FGF蛋白表達遠高於包皮中的表達;El-Sakka等用β-FGF類似物細胞調節素(Cytomodulin)注入鼠的陰莖海綿體白膜製作成功類似於Peyronie病的動物模型,證實β-FGF參與了Peyronie病的發病過程。多數Peyronie病人存在勃起功能障礙。在多數病例中,勃起障礙先於Peyronie病,根據軸向不穩定的勃起硬度機制(可能由輕微的勃起障礙引起),這些患者發生過潛在的慢性或急性陰莖彎曲損傷。
白膜在其周圍大部分區域是分層結構,外層為縱行纖維,內層為環形,兩層在背側及腹側均存在。在腹側中線縱行纖維較薄,這部分白膜可能是單層的。海綿體中隔纖維絲呈扇形排列,並與白膜內層的纖維緊密交織在一起。正常情況下,海綿體組織具有對稱的彈性,陰莖勃起引起白膜組織伸展、變薄,如沒有內層纖維支持結構,陰莖勃起就不夠堅硬,而海綿體內的纖維骨架提供這種支持結構,海綿體中隔纖維絲擔負了勃起時大部分腹-背軸向硬度的支持。當白膜鞘和中隔纖維伸展到極限時,中隔和腹-背側白膜鞘形成“工”字梁狀結構,以抵禦來自背-腹側的彎曲力。積聚在海綿體內的血液產生液壓,對四周的白膜施加的作用力成直角,背側與腹側力的向量作用力使中隔纖維小絲伸展。當陰莖在背-腹面形成彎曲時,施加於這一系統中的應力集中在中隔絲與白膜連線的部位,而這裡正是Peyronie病斑塊發生的部位。因此彎曲的剪力導致白膜的層脫離在該處中隔纖維小絲與白膜相連線,層分離後引起血液滲入該分離層間隙,或引起中隔纖維小絲撕斷。所造成的創傷與血液內滲在敏感的病人中引起炎症、硬結,最終瘢痕形成。
陰莖彎曲損傷引起Peyronie病的過程始於海綿體白膜組織老化,彈性伸縮力降低。此外,似乎並非必須是嚴重的創傷才會啟動該過程,對膨脹陰莖外層圓柱體急促的彎曲所產生的張力,就足以使中隔纖維絲與白膜分離,這種張力使許多小血管破裂,導致白膜中出血和血腫形成。隨著血塊的溶解,纖維蛋白仍保留在損傷的組織中,存留的纖維蛋白激活成纖維細胞,增強血管的滲透性,並產生炎性細胞化學趨化因子。儘管這是正常組織的修復過程,但因白膜缺少血管,在組織重建過程中纖維蛋白並沒有被清除,反覆的創傷導致纖維蛋白的進一步沉積,炎症繼續存在,膠原沉積,病理學上纖維化隨之發生。這個過程大約進行1~1.5年,在此期間機體重建這些瘢痕組織。
然而,並非所有遭受陰莖彎曲損傷的病人都會在白膜中形成瘢痕。陰莖創傷後,大多數病人有硬結加炎症發生,這一反應發生在白膜和白膜的周圍間隙和組織。有證據表明炎症明顯波及白膜與Buck’s筋膜間的間隙。許多病人在炎症和硬結期,Peyronie病徵象似乎完全消失,實際上是創傷在癒合過程中沒有發生強烈瘢痕反應(而嚴重的瘢痕是Peyronie病的特徵)。在創傷後易發生彈力組織纖維瘤病的病人易於產生嚴重的瘢痕反應。
Peyronie病好發於中年人,而在年輕人和老年人中較少見。年輕人勃起時陰莖海綿體中的壓力足以抵禦性交中陰莖變形的剪力,並可限制陰莖的彎曲,如果發生彎曲,良好的彈性伸縮力也保證陰莖白膜及中隔纖維絲能承受足夠的伸展而不致發生撕裂;然而在中年男性,隨著白膜組織彈性下降,陰莖勃起的硬度也隨之降低,如果性交過程中有外力使陰莖發生彎曲就可能引發上述病理過程;在老年男性中,性交動作沒有那么激烈了,即使陰莖海綿體白膜彈性和陰莖勃起硬度下降,也不易發生此類損傷。
Peyronie病多發生在那些性交頻度高(性交3~4次/周)、性交動作猛烈的中年男性。有些患者可能經常嘗試易致陰莖創傷的一些性交姿勢。
Peyronie病的兩種進程代表該病的兩個亞群。許多Peyronie病的發病呈隱匿過程,病人在性交時陰莖勃起不佳,在性交時中隔纖維絲張力下降,使得白膜附著處發生往復運動(workbackandforth),並產生組織疲勞,因而中隔絲白膜附著處易於斷裂,結果引起血管的破裂或中隔絲的完全斷裂,患者訴陰莖疼痛或出現痛性腫塊,緊接著會出現陰莖輕微彎曲,隨後病情可能緩慢發展。另一類發病形式:病人訴突然發病,但極少或沒有進展,患者發現陰莖彎曲幾乎是突然的,自起病後,陰莖彎曲既不進展也無改善。
病理改變
創傷促成陰莖纖維性海綿體炎發病的觀點已被普遍接受。臨床和病理檢查發現,所有斑塊位於陰莖背側或腹側中線,並附著於中隔纖維。陰莖白膜是分層結構,主要在陰莖背側和外側分層,外層為縱行纖維,內層為環行。在腹側中線陰莖白膜外層纖維稀少,形成單層。中隔纖維形成扇形和白膜內層纖維交織在一起形成環狀結構。當白膜鞘及中隔纖維伸展到最大限度時,中隔形成一個工字形;海綿體內形成的靜水壓力作用的應力。而外界過度張力(背屈或腹屈)可破壞這一平衡機制,導致白膜內外層之間分離形成潛腔。血液外滲進入腔內而引起炎症反應,產生硬結。潛腔中的血塊溶解後纖維蛋白原仍存在於該腔隙中。滯留的血塊溶解後纖維蛋白原仍存在於該腔隙中。滯留的纖維蛋白原可激活成纖維細胞,增加血管通透性的纖維蛋白原可激活纖維細胞,增加血管通透性以及產生炎性因子。雖然這是一個正常的癒合反應,但由於白膜缺乏血管分布,因此,瘢痕體質的患者在塑形期纖維蛋白原不易被清除,而容易產生瘢痕化,而大多數陰莖創傷後,春白膜及周圍組織產生的炎症反應及硬結無可完全恢復,不出現瘢痕化。
陰莖白膜創傷可由於性交、器械檢查、直接外傷引起。也有患者未有任何外傷病史,甚至無性活動亦可發生陰莖纖維性海綿體炎。此病多見於中看人,而青年及老年人少見。這同青年人陰莖白膜彈性好,抗屈伸能力強;而老年人與劇烈性活動減少有關。而在中年人,其白膜彈性有所下降,若加之劇烈而頻繁的性活動,均易於導致陰莖纖維性海綿體炎的發生。
臨床表現
陰莖纖維性海綿體炎可分為急性期和慢性期,前者特徵是急性炎症反應和疼痛,疼痛主要發生在陰莖勃起時,30%~40%患者疼痛症狀明顯。此期可持續數月,在些期間陰莖可形成結節,陰莖不斷向病側彎曲。陰莖白膜活動性炎症停止時,即進入慢性期。此期疼痛症狀通常消失,斑塊形成硬結,彎曲的陰莖不能復原。陰莖纖維性海綿體炎又被認為是陰莖纖維瘤病。在人體一些重要組織也會出現類似於陰莖纖維性海綿體炎的生理過程,如掌筋膜瘢痕化形成的Dupuytren攣縮;足底筋膜瘢痕攣縮造成的Ledderhose征,以及鼓膜瘢痕化產生的鼓膜硬化症。約30%的陰莖纖維性海綿體炎合併Dupuytren攣縮,而Dupuytren攣縮中僅3%患陰莖纖維性海綿體炎。雖然注意到有家族發病的傾向,但未發現該病同HLA-B7 或HLA-B 27之間的相關性。
多為中年人罹患,主要是45~60歲發病。
多數陰莖纖維性海綿體炎是隱匿性發病,患者陰莖勃起功能不滿意,發現陰莖有痛性斑塊,陰莖彎曲緩慢進展。也有急驟發病者,突然發現陰莖彎曲,一般不進展。
陰莖彎曲變形引起性交困難。若有陽瘺則是存在心理障礙,或陰莖血管器質性病變。
陰莖背側可觸及硬結或索狀斑塊,大小不一,單發或多發,無壓痛或輕壓痛,陰莖勃起時可疼痛。病變不侵犯尿道,無排尿或射精障礙。斑塊有鈣化或骨化時,X線平片可顯示病灶,並可測量大小。
該病應與先天性陰莖彎曲畸形,陰莖背側動脈栓塞,陰莖局部創傷後纖維化,陰莖海綿體白細胞浸潤等疾病進行鑑別。
輔助檢查
高分辨淺層彩色超聲Doppler檢查可以客觀地判斷斑塊或鈣化的大小、病變數量以及評估療效。在陰莖海綿體內注射血管活性劑前後,套用彩色超聲Doppler檢查陰莖海綿體白膜,海綿體動脈和靜脈功能,還可觀察陰莖背動脈與海綿體、海綿體與海綿體動脈之間的側支動脈。有些病例由陰莖血管時,若損傷這個血管分支,就可能發生陽瘺。
海綿體灌注動力學測定和海綿體造影。陰莖海綿體注射血管活性劑之後,灌注生理鹽水,測量靜脈溢漏的速度,海綿體內注入稀釋的造影劑,拍攝X線平片,可觀察靜脈血漏出的部位。有報導,約36%陽瘺合併陰莖纖維性海綿體炎的患者有陰莖動脈血流異常,59%則存在靜脈閉合功能異常。由此可見,陰莖纖維性海綿體炎患者合併陽瘺的一個重要原因是存在陰莖血管功能不全。
鑑別診斷
1.陰莖骨化陰莖骨化比較少見,是由陰莖海綿體鈣化及纖維化所致,其結節常突出,看似犄角。可引起陰莖勃起時疼痛,並可導致性交困難。X線檢查可見陰莖內有密度增高的陰影。2.陰莖癌 陰莖癌最常發生在陰莖頭、包皮內板及冠狀溝等處。陰莖癌侵犯陰莖海綿體時可在海綿體內出現硬結。局部活組織檢查有助於確定診斷。
3.陰莖結核陰莖結核相當少見,多表現為陰莖頭的結節或慢性潰瘍,潰瘍分泌物檢查可發現結核桿菌。疼痛一般不明顯。陰莖結核在海綿體內蔓延時,可使局部纖維化並導致陰莖側彎。確診需依靠病理檢查。
4.還應與先天性陰莖彎曲畸形,陰莖背側動脈栓塞,陰莖局部創傷後纖維化,陰莖海綿體白細胞浸潤等疾病進行鑑別。
治療措施
陰莖纖維性海綿體炎的轉歸,約13%可緩解,47%無變化,40%則逐漸進展。未經治療而病變完全消失的病例雖有報導,但甚為罕見。即使病變自行消失,也需要經過數年時間。年輕患者,斑塊質軟,小於2cm,症狀期短者預後好。陰莖早期形成大於45º角,則變形的陰莖不易恢復正常。斑塊發生鈣化,預後不佳。
需要充分時間觀察病變的發展,待病情穩定後再決定治療方案。
陰莖雖有斑塊病灶存在,不影響勃起和性交者通常主張藥物治療。維生素E(400mg,2/d)是自由基清除劑,能促進結締組織修復,無明顯副作用。套用對氨基甲酸(PABA,痛性勃起為主的年輕患者可試用)、美芬胺(allerga),秋水仙鹼、他莫苷芬、類固醇、甲基苄肼等藥物治療,均有臨床報導,但其中一些藥物毒副作用嚴重,要慎用。也有主張斑塊內注射藥物,常用藥物有副甲狀腺素、二亞楓、考的松、膠原酶、超氧化物岐化酶、干擾素、導搏定等。報導的病例多數為非隨機選擇,無安慰劑對照,或不是大宗病例總結,對藥物的真實療效難以評定。綜合文獻報導,藥物治療有效率幾乎均不足50%。此外,尚有套用X線、超音波、離子透入、雷射治療的報導,療效也不肯定。
手術治療的目的旨在矯正陰莖彎曲畸形,恢復性交能力。Nesbit倡導的方法是在陰莖的彎曲凸側面剪除一小塊橢圓形白膜,再縫合剪開的白膜,關閉缺損,伸直陰莖。若陰莖長度足夠,輕度彎曲,無面切開白膜,僅單純縫扎較長一側的白膜即要,方法簡單,併發症少。這兩種方法均不損傷陰莖海也較滿意,術後一般不支影響陰莖勃起功能,療效也較滿意,故較廣泛地套用於臨床。Gelbard和Hayden(1991)建議不切除白膜,在彎曲陰莖的凹面橫向切開白膜,做數個鬆弛切口,在切口內填補移植物。也有主張切除陰莖斑塊,局部缺損需用移植物修補。常用的移植有真皮、大隱靜脈、睪丸鞘膜、人工合成材料等。因為病損往往超出斑塊範圍,浸潤周圍勃起組織,如果切除斑塊及周圍組織過多,就有發生陽瘺之慮。Montorsi等(1994)強調術前套用彩色超聲Doppler檢測陰莖血流動力學參數,正確判斷陰莖海綿體結構和海綿體的靜脈功能。若存在陰莖靜脈閉合功能不全,不主張實施斑塊切除和缺損修補術,因為術後陽瘺生率可高達70%。
陰莖彎曲合併陽瘺時,先矯正陰莖彎曲,再採用微創方法治療陽兼,如陰莖海綿體內注射血管活性藥物,尿道內注入Muse,真空助勃裝置等,均有可能達到治療陽瘺的效果。非手術療法失敗,再考慮陰莖海綿體內值入假體。
藥物治療
(1)維生素E400mg,2次/d。價廉且極少有副作用,是一種自由基清除劑,可改善一些病人的症狀。(2)氨苯甲酸(對氨基苯甲酸):在一些零星的小樣本報告中PABA對Peyronie病是有效的。但每天必須服用12g,劑量大易起顯著的胃腸道反應。
(3)抗組胺藥:基於Peyronie病早期的炎性特徵由組織胺所介導,對於一些以陰莖勃起疼痛為主訴症狀的年輕病人,可套用非特異抗組胺藥特非那定(特非拿汀)。特非那定能引起許多副作用,因此最近有人套用非索那定,用法是60mg,2次/d,3個月1療程。儘管藥理學研究沒有任何支持性結論,但一些零星的報導支持特非那定或非索那定對Peyronie病的有效。
(4)秋水仙鹼(秋水仙素):秋水仙鹼能誘髮膠原酶的活性,減少膠原的合成。有些作者用秋水仙鹼0.6mg,2次/d,共3~4周,然後取外周血作檢查看是否有骨髓抑制的證據。如果無異常發現,則繼續服藥0.6mg,3次/d,共3~4個月為1療程。該藥對精子計數有負面影響,另有許多病人因胃腸道副反應很大而不能耐受治療。
(5)類固醇局部注射:國內有一些散在的報導:用醋酸曲安奈德(去炎舒松)行斑塊內注射取得滿意療效。然而,許多病人在局部用類固醇之前有一段相對穩定的時期,但因注射而致創傷後,導致炎症進一步發展,硬結和彎曲加重。
(6)鈣通道阻滯藥:Levine(1994)向斑塊內注射鈣通道阻滯藥,儘管未能減輕陰莖彎曲,但似乎減緩了瘢痕化過程。
(7)膠原酶:Gelbard等(1985)研究膠原酶用於Peyronie病的斑塊,在最初雙盲試驗中,未能證明該藥對病變有顯著的改善,在另一樣本量較大的平行雙盲試驗中,提示用膠原酶注射斑塊的較好的治療效果。
(8)三尖杉鹼(三尖杉脂鹼):陳林等用三尖杉鹼行局部注射共12例,其中6例斑塊完全消失。
(9)L-乙醯卡米丁(acetyl-L-camitime)及他莫西芬(他莫西酚):Biahiottig等報導L-乙醯卡米丁1g,2g/d,共3個月,能顯著減輕陰莖彎曲和疼痛,抑制疾病的發展,副作用小。用他莫西芬(Tamoxifen)治療Peyronie病,20mg/次,2次/d,共3個月,能使斑塊縮小,但不能減輕陰莖的彎曲,並且副作用大。
(10)中草藥:郭應祿用中草藥(柴胡、赤白芍、白芷、夏枯草、制角刺、桃仁泥、制乳末、莪術、生薏仁)加服維生素C,取得一定的療效。
物理治療
Culibrk綜合超聲、紅外線和離子電滲療法(Iontophoresis)治療35例Peyronie病患者,10例治癒,其餘症狀緩解。超聲療法用於治療Peyronie病似乎僅減輕斑塊的炎性反應。用直線加速器的γ射線實施治療,要格外謹慎,適應證應嚴格限制,只有那些病情遷延不愈並且病程早期伴有勃起疼痛的病人才套用放療。外科干預
(1)術前評估:評估應包括性伴雙方,一定要向患者及性伴侶說明陰莖病損不是腫瘤或癌,並告訴他們Peyronie病是可以治療的,患病並不意味著從此無性活動。許多醫生告訴病人Peyronie病不可治癒的,但若以恢復或延續性活動為治療目標,則Peyronie病是可以治療的。有一點也很重要,那就是醫生應認識到Peyronie病是一個發展變化的疾病,有些病人可以明顯縮小或改善,外科手術無必要,因此患者需要等待一段時間,也就是初發病至決定性治療期間要觀察病情的變化。等待手術期間對於他們來說是相當重要的,因為等待會使他們產生嚴重的焦慮,所以,要設法讓病人感覺到此期間似乎醫生正在對他們的疾病進行治療,即不是純粹的等待,例如給他們服藥。Peyronie病病變已穩定,陰莖嚴重彎曲,並且存在嚴重勃起功能障礙,此時就是Peyronie病需要外科手術糾正的指征。基於這一點,術前對預手術患者進行勃起功能評估是必要的。有些病人用海綿體內注射血管活性藥物或真空吸引等方法可以改善勃起功能,提示陰莖彎曲本身並未引起勃起障礙,不需外科治療。用海綿體內注射血管活性藥物後行都卜勒檢查及夜間勃起試驗評估勃起功能狀況,對判斷是否需要手術及術後療效是有益的。
最後在外科干預前,應讓病人明白手術的最終效果。儘管多數病人希望外科手術能使他們陰莖恢復患病以前的水平,但應該讓他們知道這是不可能的,應不厭其煩地向病人解釋清楚,最好的結果是:外科手術能恢復陰莖彎曲得以糾正,即使有些許彎曲也不影響性交,勃起功能可能保持術前的水準,任何超過實際的期望是不可能獲得的。病人必須接受忠告以確定對手術的期望值。
(2)外科矯正:
①海綿體白膜摺疊法:Pryor等(1979)描述在Peyronie斑塊的對側切除和摺疊部分海綿體以糾正陰莖彎曲,其原理是通過縮短病損斑塊對側的陰莖海綿體白膜以抵消由於病損處無彈性所致的效應。Lue(1989)改用Pryor方法,省去切除病損對側白膜這一步驟而僅行摺疊術,治療Peyronie病取得良好的早期效果。Savoca等隨訪157例接受Nesbit手術的Peyronie病人,平均隨訪時間為72個月,對手術的滿意度87.9%,136例勃起滿意(IIEF-5評分大於21分),22例陰莖縮短(1.5~3cm)但只有2例影響性交;雖然上述兩種術式在其他病人中取得良好的療效,但許多病人非常在意Peyronie病本身引起的陰莖縮短,並且他們被告知這些外科手術會使陰莖進一步縮短,因此他們可能不願接受這類手術方式。
②斑塊小切口法:Gdlbard(1989)也描述了一種外科術式,在Peyronie斑塊上作許多小切口,然後用顳筋膜移植於填充缺損,他報導說取得良好的結果。該術式的理論基礎是:在一個病損上做很多小切口,然後用一些柔順性好的材料填充之,癒合後形成一更平滑的彎曲。術後陰莖勃起障礙發生率較低。
③斑塊切除並用替代材料修補:切除病損斑塊後可用以下自體組織修補:皮片、睪丸鞘膜、靜脈片等。Chun等報導屍體心包用於切除斑塊後的修補手術,效果與自體皮膚移植相似,但術前準備簡單,併發症少,材料的柔順性好。Hellstrom報導用矽膠補片修補斑塊切除後的缺損取得良好的效果。
④手術概要:切口選擇取決於病損斑塊所在部位,斑塊如在腹側則取陰莖腹側正中切口;背側斑塊則取包皮環切切口,將陰莖幹皮膚脫套到陰莖根部,這樣易於暴露位於陰莖中部及遠端的病損,陰莖近端的病損或包皮特別長,則在陰莖根部加第2個切口,沿陰莖根部側面向陰囊延伸,並將陰莖幹從該切口牽出;處理陰莖背側血管神經束時,應與Buck’s筋膜一同提起,方法:在尿道海綿體的側面作切口,將Buck’s筋膜和陰莖背血管神經束一起提起游離,使之離開陰莖海綿體。
暴露了背側或腹側的白膜後,無彈性的斑塊即明顯暴露,斑塊的範圍可以在白膜上描繪出來,人工勃起有助於確定陰莖彎曲的程度。如果選用斑塊切除術,根據需要沿斑塊周邊作卵圓形或衛星形切口,以減少缺損邊緣的張力,並使缺損面積增加1.5~2倍。移植物的面積應比缺損面積大30%,供皮去掉表皮並仔細去脂肪以獲得真皮移植物。用PDS線關閉缺損部位。術中做人工勃起測驗,看陰莖是否伸直及縫合邊緣是否漏血。如術中陰莖未能伸直,則應進一步設計切口和重新修補缺損。最後在Buck’s筋膜與肉膜之間放2條細的矽膠引流管,將陰莖解剖學復位。2周后,鼓勵病人使陰莖勃起(不鼓勵性交),目的是希望移植皮膚不與陰莖深層粘連,並有助於移植物的存活。在術後頭3個月,移植物收縮可重新產生輕微的陰莖彎曲,但當移植物變軟後陰莖又恢復伸直,因此術前必須告知病人。
儘管放置陰莖假體可治療Peyronie病的勃起障礙,但是大多數Peyronie病患者無需放置陰莖假體。