成份
 阿爾馬爾
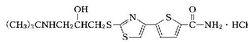
阿爾馬爾化學名稱:5-[2-[(3-tert-butylamino-2-hydroxypropyl) thio]-4-thiazolyl]-2-thiophenecarboxamide monohydrochloride
結構式:
分子式:CHNOS·HCL
分 子 量:408.01
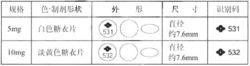
性狀
 阿爾馬爾
阿爾馬爾適應症
•原發性高血壓(輕度一中度)
•心絞痛
•心動過速性心律失常
•原發性震額
規格
5mg;10mg。
用法用量
原發性高血壓(輕度一中度)、心絞痛、心動過速性心律失常:
通常成人套用鹽酸阿羅洛爾的劑量為每次lOmg,每日二次口服。根據病人年齡、症狀等適當增減劑量,療效不充分時,可增至每日30mg。
原發性震顫:
通常成人套用鹽酸阿羅洛爾從每日lOmg開始給藥。療效不充分時,可按照每次10mg。每日二次的維持量口服。根據病人年齡、症狀等適當增減,但不得超過1天30mg。
不良反應
 阿爾馬爾
阿爾馬爾調查總例數12978例中有496例(3.8%)出現不良反應及實驗室檢驗值異常。主要的不良反應有心動過緩141例(1.1%),眩暈及站立不穩77例(0.6%),乏力及倦怠感51例(0.4%)。主要實驗室檢查值異常有AST(GOT)升高34例(0.3%),ALT(GPT)升高34例(0.3%),甘油三酯升高29例(0.2%),尿酸值升高15例(0.1%)。
1.嚴重不良反應
心力衰竭、房室傳導阻滯、竇房傳導阻滯、病態竇房結綜合徵([0.1%),心動過緩(0.1~5%):
定期檢查心功能,出現上述症狀時,採取減量或停藥等適當處置。
2.其它不良反應
出現以下不良反應時,應根據需要採取減量或停藥等適當處置。
禁忌
不得用於下列病人:
1.高度心動過緩(明顯竇性心動過緩)、房室傳導阻滯('II: III度)、竇房傳導阻滯、病態竇房結綜合徵的病人[有可能導致上述症狀惡化]。
2.糖尿病酮症、代謝性酸中毒的病人[有可能增強酸中毒對心肌收縮力的抑制]。
3.有可能出現支氣管哮喘、支氣管痙攣的病人[有可能收縮支氣管,誘發支氣管哮喘甚至惡化]。
4.心源性休克的病人[有可能抑制心功能,導致症狀惡化]。
5.肺動脈高壓所致右心衰的病人[有可能抑制心功能,導致症狀惡化]。
6.充血性心力衰竭的病人[有可能抑制心功能,導致症狀惡化]。
7.未治療的嗜鉻細胞瘤病人[參考“注意事項”中的“與用法用量有關的注意事項”]。
8.孕婦或有懷孕可能的婦女[參考“孕婦及哺乳期婦女用藥”]。
9.對本藥成分有過敏史的病人。
注意事項
1.慎重給藥(對下列病人應慎重給藥)
(1)有充血性心力衰竭可能的病人(充分觀察,對聯合套用毛地黃藥物的病人,須慎重給藥)[有可能抑制心功能,導致充血性心力衰竭症狀惡化]。
(2)特發性低血糖症、控制不充分的糖尿病、長期間禁食狀態的病人[由於容易掩蓋低血糖的前期症狀心動過速等交感神經系統反應,故須注意血糖值]。
(3)低血壓、心動過緩、房室傳導阻滯(I度)病人[有可能導致症狀惡化]。
(4)嚴重肝功能、腎功能障礙的病人[有可能影響藥代動力學]。
(5)老年患者[參考“老年患者用藥”]。
(6)末梢循環障礙的病人(雷諾氏綜合徵、間歇性跛行症等)[有可能抑制末梢血管擴張,導致症狀化]。
(7)運動員慎用。
2.重要注意事項
(1)長期給藥時,須定期進行心功能檢查(心率、血壓、心電圖、X光等)。尤其在出現心動過緩及低血壓時,須減量或停藥。必要時使用阿托品。 須注意肝功能、腎功能、血像等。
(2)有報告指出,正在服用類似化合物(鹽酸普奈洛爾)的心絞痛病人突然停藥時,有的病人出現症狀惡化或引起心肌梗塞。故在需要停藥時,須緩慢減量,充分觀察。
須事先告誡病人:沒有醫生的指示不要停藥。用於心絞痛以外的患者,例如用於心律失常患者及老年患者時,也須予以同樣的注意。
(3)手術前48小時內不宜給藥。
(4)用於原發性震顫病人時,應充分觀察,同其它震顫性疾病進行鑑別診斷,只能用於確診為原發性震顫的病人.
(5)用於原發性震顫病人時,與用於高血壓病人相比,多見心動過緩、眩暈、低血壓等不良反應,故應充分觀察,出現症狀時,採取減量或停藥等適當處理。
(6)有可能出現眩暈、站立不穩症狀,應提醒服用本藥的病人(尤其在服用初期).在駕駛汽車等伴有危險的機械作業中予以注意。
3.與用法用量有關的注意事項
用於嗜鉻細胞瘤病人時,由於可引起血壓急劇升高,故不得單獨套用本藥。對嗜鉻細胞瘤病人,須在套用α受體阻斷劑進行初期治療後,套用本藥,並始終聯合套用α受體阻斷劑。
4.套用注意事項
本藥交與病人時,對PTP包裝的藥品,指導病人從PTP密封袋中取出藥片服用。(據報告,有人因誤咽PTP密封袋,導致鋒利的銳角刺入食管黏膜,引起食管穿孔、縱隔竇炎等嚴重併發症。)
5.聯合用藥注意事項
參考“藥物相互作用”。
孕婦及哺乳期婦女用藥
1.不得用於孕婦或有懷孕可能的婦女[參考“生殖毒性”]。
2.在服藥期間應避免授乳[參考“生殖毒性”]
兒童用藥
尚未確立本藥對早產兒、新生兒、乳兒及嬰幼兒的安全性。
老年用藥
用於老年患者時,應注意下列事項,從小劑量(例如,每次5mg)開始,邊觀察病人狀態邊慎重給藥。
1.老年患者一般不宜過度降壓(有引起腦血栓等的可能)。
2.老年患者多見心功能等低下,易引起血壓過度下降和心動過緩。
3.需停藥時,應緩慢減量(參考“重要注意事項”)。
藥物相互作用
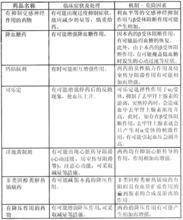 阿爾馬爾
阿爾馬爾(並用時注意事項)
藥物過量
症狀:超量給藥有可能產生心動過緩、III度房室傳導阻滯、心衰、低血壓、支氣管痙攣等。
處理:超量給藥時。應停藥,並根據需要給予洗胃等處理,同時採取以下措施。
1.心動過緩、完全房室傳導阻滯:給予阿托品、異丙腎上腺索等,或安裝心臟起搏器。
2.心力衰蠍、低血壓:給予強心劑、升壓藥、輸液等,或採取其它改善循環的措施。
3.支氣管痙攣:靜脈給予β2受體激動劑或氨茶鹼,或採取其它改善呼吸的措施。
藥理毒理
 阿爾馬爾
阿爾馬爾1.藥理
(1)α,β受體阻斷作用
在以高血壓及血壓控制良好的病人為對象進行的試驗中,證實本藥有α及β受體阻斷作用,其作用比值約為1:8。
(2)降壓作用
在自發性高血壓大鼠(SHR)及易發腦卒中大鼠(SHR-SP)等病態動物模型所做的動物試驗中,證實具有明顯降低血壓的作用;並在SHR-SP試驗中,證實本藥具有抑制高血壓所致心、腎等血管病變的作用。本藥通過適宜的α受體阻斷作用,在不使末梢血管阻力升高的情況下,通過β受體阻斷作用產生降壓效果。
(3)抗心絞痛作用
通過β受體阻斷作用抑制亢進的心功能,減少心肌耗氧量,糾正心肌的氧氣供需不均狀態。另外,在套用心絞痛模型動物(狗)的試驗中,證實α受體阻斷作用有減少冠狀動脈阻力的趨勢。
(4)抗心律失常作用
在三氯甲烷誘發心律失常(小鼠)及三氯甲烷-腎上腺素誘發心律失常(狗)的試驗中證實具有抗心律失常作用。
(5)抗震顫作用
在氧代1,4-二吡咯烷-2-丁炔誘發震顫(小鼠),TRH誘發震顫(小鼠)及MPTP誘發震顫(猴)試驗中,證實具有抗震顫作用。
本藥的抗震顫作用為骨骼肌β2受體阻斷作用,其作用為末梢性。
(6)其它藥效動力學
在大鼠、家兔的試驗中,未發現有內在擬交感活性及膜穩定作用。
2.毒理
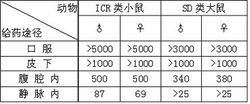
(1)急性毒性
(2)慢性毒性
對SD類大鼠按照5,20,80,320mg/kg/天,對小獵狗按照20,50,125mg/kg/天的劑量分別連續口服給藥6個月後,大鼠出現眼瞼下垂,後肢腫脹,心臟重量增加等變化,小獵狗出現潮紅,心率減慢等變化。這類變化均起因於主藥理作用,停藥後可恢復,是可逆性變化。
(3)生殖毒性
①妊娠前,妊娠初期給藥試驗
對Wistar類大鼠(雌雄)的生殖功能沒有影響,未發現對胚胎、幼仔有致死作用及致畸作用,不影響胎仔發育和器官形成。
②器官形成期給藥試驗
對Wistar類大鼠給藥劑量為100mg/kg(臨床劑量的約250倍)以上時出現腎盂擴大,250mg/kg(臨床劑量的約600倍)時視神經缺損的自然發生頻度增大,但在小鼠及家兔的試驗中未見影響。
③圍產期,授乳期給藥試驗
對Wistar類大鼠大劑量給藥時,發現影響幼仔發育。與此相關,幼仔(雄性)的交配能力降低,但母乳哺育試驗結果表明,是由於母體的繼發性生後發育遲緩所致。
(4)其它毒性
未見抗原性(小鼠、豚鼠、家兔)、致突變性(微生物)及致癌性(小鼠、大鼠)。
藥代動力學
健康成人一次口服lOmg後,吸收迅速,約2小時後達到最高血中濃度 (117ng/mL),其血中濃度半衰期約10小時。本藥口服吸收較完全,服藥後24小時的AUC值為0.71pg•hr/mL。本藥在肝臟無首過效應。血漿蛋白結合率為91%。連續給藥時,無蓄積性。本藥在肝臟中分布濃度最高,其次為腎臟、肺組織。本藥經肝、腎代謝,在血中及尿中的活性代謝產物為氨基甲醯基水解物,其血中濃度為本藥在血中濃度的1/5,其尿中排泄率為3-5%。在尿中測定到了微量的另2種無活性代謝產物,其尿中排泄率約為0.3-0.5%。本藥主要經腸道排泄(大鼠糞中排泄率為84% ),在尿中原型排泄率為4-6%。
貯藏
密封,室溫保存。
包裝
PTP包裝。
5mg:10片/盒;lOmg:10片/盒。
有效期
36個月。
執行標準
進口藥品註冊標準JX20000375。
批准文號
分包裝批准文號:國藥準字J20110017(5mg);國藥準字J20110018(10mg);
小包裝進口藥品註冊證號:H20090776(5mg);H20090777(l0mg);
大包裝進口藥品註冊證號:H20090778(5mg);H20090779(lOmg)。
生產企業
住友製藥株式會社
核准日期
2007年2月20日
修訂日期
2007年7月3日 2009年12月25日 2011年03月23日