基本簡介
 銀氨溶液
銀氨溶液銀氨溶液又叫多倫試劑,化學式為[Ag(NH3)₂]OH·XH₂O。
基本性質
即硝酸銀的氨水溶液。一種弱氧化劑。可將醛氧化為羧酸,並產生金屬銀沉積於玻璃反應器皿壁上(銀鏡)。用於鑑別醛,而酮則不反應。該試劑應現配現用,不宜保存,久置易生成易爆的雷爆銀(主要成分為氮化銀)。
配製方法
1.配製方法是:
1.準備試管:在試管里先注入少量氫氧化鈉溶液,振盪,然後加熱煮沸。把氫氧化鈉倒去後,再用蒸餾水洗淨備用。
2.配製溶液:在洗淨試管中,注入1mL硝酸銀溶液,然後逐滴加入氨水,邊滴邊振盪,直到最初生成的沉澱剛好溶解為止
2.教材中銀氨溶液配製過程中:
向溶液里逐滴滴加氨水首先析出AgOH: AgNO+NH·H2O==AgOH↓+NHNO 常溫下AgOH極不穩定,分解為AgO暗棕色沉澱 2AgOH==AgO+HO 繼續滴加氨水,沉澱溶解: AgO+4NHHO=2Ag(NH)+2OH+3HO 同時,生成的OH與前面反應生成的NH反應:OH+NH==NH·HO
因此,向AgNO溶液里加入稀氨水至沉澱溶解的總離子方程式為: Ag+2NH·HO==Ag(NH)+2HO此時溶液中只含NO和Ag(NH),即得到Ag(NH)NO,不是氫氧化二氨合銀。
銀鏡反應
 銀氨溶液
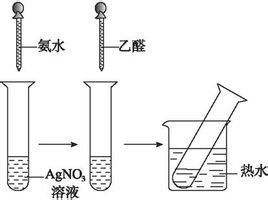
銀氨溶液在潔淨的試管里加入1mL2%的硝酸銀溶液,再加入氫氧化鈉水溶液,然後一邊振盪試管,可以看到白色沉澱。再一邊逐滴滴入2%的稀氨水,直到最初產生的沉澱恰好溶解為止(這時得到的溶液叫銀氨溶液)。
乙醛的銀鏡反應:再滴入3滴乙醛,振盪後把試管放在熱水中溫熱。不久可以看到,試管內壁上附著一層光亮如鏡的金屬銀。(在此過程中,不要晃動試管,否則只會看到黑色沉澱而無銀鏡。)
葡萄糖的銀鏡反應:滴入一滴管的葡萄糖溶液,振盪後把試管放在熱水中溫熱。不久可以看到,試管內壁上附著一層光亮如鏡的金屬銀。反應本質:這個反應里,硝酸銀與氨水生成的銀氨溶液中含有氫氧化二氨合銀,這是一種弱氧化劑,它能把乙醛氧化成乙酸(即-CHO被氧化成-COOH),乙酸又與生成的氨氣反應生成乙酸銨,而銀離子被還原成金屬銀。從葡萄糖的角度來說,葡萄糖中有醛基,具有還原性,把硝酸銀里的銀離子還原成金屬銀。
注意事項
1.銀鏡反應的成敗關鍵之一,是所用的儀器是否潔淨。
2.配製銀氨溶液時,應防止加入過量的氨水。銀氨溶液必須隨配隨用,不可久置。
3.實驗完畢,試管內的銀氨溶液要及時處理,先加入少量鹽酸,倒去混和液後,再用少量稀硝酸洗去銀鏡,並用水洗淨。否則可能會生成雷爆銀(主要成分是氮化銀)。
銀氨溶液有一個作用是檢驗有還原性的糖(葡萄糖、麥芽糖、果糖)也是發生銀鏡反應
銀鏡反應:2[Ag(NH₃)2OH]+R-CHO→R-COONH₄+2Ag↓+H₂O+3NH₃{因為氨氣極易溶於水,所以不標氣體逸出符號“↑”} (甲醛除外)甲醛與銀氨溶液反應方程:HCHO + 4[Ag(NH₃)₂]OH = (NH₄)2CO₃ + 4Ag↓+ 6NH₃ +2H₂O{因為氨氣極易溶於水,所以不標氣體逸出符號“↑”})
在製備銀氨溶液時,一般用稀氨水而不用濃氨水。這是因為在配製銀氨溶液時,若氨水太濃,NH₃容易過量,使Ag過度地被絡合,降低銀氨溶液的氧化能力。
常見謠言
謠言:銀氨溶液放久後會產生疊氮化銀(AgN3)而引起爆炸
駁斥:銀氨溶液析出的爆炸物是氮化銀Ag3N或者氨基銀AgNH2,從來不會形成疊氮化銀
 銀氨溶液
銀氨溶液文獻結論如下圖