簡介
造血幹細胞移植是指通過大劑量放、化療,阻斷原發疾病的發病機制,如殺滅體內的腫瘤細胞、清除異常免疫細胞克隆等等,再將造血幹細胞移植給受者,重建受者的正常造血、免疫系統,達到治療效果的一種治療手段。
根據造血幹細胞來源可分為骨髓造血幹細胞移植、外周血造血幹細胞移植、臍帶血造血幹細胞移植。
造血幹細胞
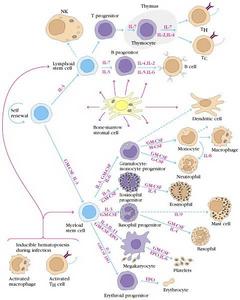
通俗地講,幹細胞是指尚未發育成熟的細胞,是所有造血細胞和免疫細胞的起源,它不僅可以分化為紅細胞、白細胞和血小板,還可跨系統分化為各種組織器官的細胞, 造血幹細胞移植
造血幹細胞移植造血幹細胞有兩個重要特徵:
其一,高度的自我更新或自我複製能力;其二,可分化成所有類型的血細胞。造血幹細胞採用不對稱的分裂方式:由一個細胞分裂為兩個細胞。其中一個細胞仍然保持幹細胞的一切生物特性,從而保持身體內幹細胞數量相對穩定,這就是幹細胞自我更新。而另一個則進一步增殖分化為各類血細胞、前體細胞和成熟血細胞,釋放到外周血中,執行各自任務,直至衰老死亡,這一過程是不停地進行著的。適應症
造血幹細胞移植迄今仍然是一種高風險治療方法,目前主要用於惡性血液疾病的治療,也試用於非惡性疾病和非血液系統疾病,如重症難治自身免疫性疾病和實體瘤等。(1)血液系統惡性腫瘤:慢性粒細胞白血病、急性髓細胞白血病、急性淋巴細胞白血病、非霍奇金淋巴瘤、霍奇金淋巴瘤、多發性骨髓瘤、骨髓增生異常綜合徵等。
(2)血液系統非惡性腫瘤:再生障礙性貧血、范可尼貧血、地中海貧血、鐮狀細胞貧血、骨髓纖維化、重型陣發性睡眠性血紅蛋白尿症、無巨核細胞性血小板減少症等。
(3)其它實體瘤:乳腺癌、卵巢癌、睪丸癌、神經母細胞瘤、小細胞肺癌等。
(4)免疫系統疾病:重症聯合免疫缺陷症、嚴重自身免疫性疾病。
由於移植存在致命性合併症,因而非血液系統疾病的造血幹細胞移植治療還未被廣泛接受。
分類介紹
(1)按照採集造血幹細胞的來源不同分為:骨髓移植、臍血移植、外周血造血幹細胞移植等。(2)按照供體與受體的關係分為:自體骨髓移植/臍血移植/外周血造血幹細胞移植、異體骨髓移植/臍血移植/外周血造血幹細胞移植。異體移植又稱異基因移植,當供者是同卵雙生供者時,又稱同基因移植。
(3)根據供者與受者HLA配型相合程度,異體骨髓移植/臍血移植/外周血造血幹細胞移植分為:HLA全相合移植、不全相合移植、單倍體相合移植。
(4)根據供者與受者的血緣關係分為:血緣相關移植、非血緣移植即骨髓庫來源供者。
(5)根據移植前的預處理方案強度可分為:清髓性造血幹細胞移植和非清髓性造血幹細胞移植(減低預處理劑量的造血幹細胞移植)。
一般根據患者的疾病種類、疾病狀態及預後、HLA配型結果及供者年齡等因素綜合考慮來選擇造血幹細胞移植方式。目前異基因造血幹細胞移植絕大多數為配型相同的同胞間、半相合父母與子女間、不全相契約胞間的移植,而隨著全世界及我國骨髓庫的增加,非血緣供者的異基因造血幹細胞移植數量也在不斷增加。不同移植類型各自優劣不同,自體造血幹細胞移植的優點在於不受供者的限制,移植後不發生移植物抗宿主病,不需要使用免疫抑制劑,嚴重併發症較少,費用較低,缺點是復發率高。異基因造血幹細胞移植治療惡性疾病,植入的供者細胞有持久的抗腫瘤作用,復發率低,但嚴重併發症多,費用相對較高。
造血幹細胞移植技術的發現和套用
生命科學是二十世紀發展最為迅猛的學科之一,已經成為自然科學中最引人注目的領域。造血幹細胞移植技術的發現和套用為人類戰勝疾病帶來新的希望,是現代生命科學的重大突破。造血幹細胞移植可治療惡性血液病、部分惡性腫瘤、部分遺傳性疾病等75種致死性疾病。包括急性白血病、慢性白血病、骨髓增生異常綜合徵、造血幹細胞疾病、骨髓增殖性疾病、淋巴增殖性疾病、巨噬細胞疾病、遺傳性代謝性疾病、組織細胞疾病、遺傳性紅細胞疾病、遺傳性免疫系統疾病、遺傳性血小板疾病、漿細胞疾病、地中海貧血、非血液系統惡性腫瘤、急性放射病等。造血幹細胞移植可治療的疾病
1、造血系統惡性疾病:各型急性白血病,慢性白血病,何杰金淋巴瘤,非何杰金淋巴瘤,骨髓增生異常綜合症,多發性骨髓瘤;2、造血系統非惡性疾病:再生障礙性貧血,慢性血小板減少性紫癜,陣發性睡眠性血紅蛋白尿,骨髓纖維化;
3、實體瘤:神經母細胞瘤,髓母細胞瘤,腎母細胞瘤,橫紋肌肉瘤、骨肉瘤;
4、自身免疫性疾病:系統性紅斑狼瘡,皮肌炎,多發性硬化,類風濕關節炎;
5、遺傳代謝病:粘多糖病,腎上腺腦白質營養不良,聯合免疫缺陷病,范可尼貧血,地中海貧血,慢性肉芽腫。
造血幹細胞移植方式
不同的疾病選擇不同的移植方式。自身免疫系統疾病和未侵犯骨髓的實體瘤(包括淋巴瘤)通常都採用自體幹細胞移植,可使用自體外周血幹細胞也可採用自體骨髓;急性白血病中除了M2、M3可以考慮採用自體造血幹細胞移植外,其餘的均應採用異基因造血幹細胞移植,慢性白血病必須採用異基因造血幹細胞移植;再生障礙性貧血、骨髓纖維化等幹細胞異常所引起的造血系統非惡性疾病也應採用異基因造血幹細胞移植,而慢性血小板減少性紫癜的病因主要是免疫因素,可以採用自體造血幹細胞移植;遺傳代謝病通常都採用異基因造血幹細胞移植。對於造血系統的惡性疾病、部分遺傳代謝病通常都採用清髓移植,自身免疫系統疾病通常採用非清髓的移植。造血幹細胞移植治療的基本過程
首先進行供、受者間的HLA配型,選擇合適的供者;其次,對供者僅進行幹細胞動員、採集,將採集的乾細胞凍存備用;第三,對受者進行預處理,回輸已採集的幹細胞,也可再供者動員和受者的預處理同步進行,採集後直接回輸。最後採用刺激因子刺激造血恢復。同時預防治療各種併發症。移植準備
移植前患者的準備患者進入移植倉前,要進行全面查體,以了解患者疾病緩解狀態、重要器官功能狀態、有無潛在感染灶。患者需要在層流潔淨病房住1-1.5月,需準備在潔淨室內所用的生活用品,剃掉頭髮。
移植前供者的準備
供者移植前需做全面查體,以了解重要器官功能有無缺陷、有無感染性疾病。目前多數供者需要採集骨髓加外周血幹細胞,因此采髓前2周供者需要自體備血400-800ml。
造血幹細胞移植的預處理
在造血幹細胞移植前,患者須接受一個療程的大劑量化療或聯合大劑量的放療,這種治療稱為預處理(conditioning),這是造血幹細胞移植的中心環節之一。預處理的主要目的為:(1)為造血幹細胞的植入騰出必要的空間;(2)抑制或摧毀體內免疫系統,以免移植物被排斥;(3)儘可能清除基礎疾病,減少復發。根據疾病和所進行的造血幹細胞類型不同,所選擇的預處理方案的側重點各有不同。惡性血液病目前常用的預處理方案有:①Cy/TBI(環磷醯胺+全身照射);②Bu/Cy(馬里蘭+環磷醯胺);③Bu/Flu(馬里蘭+氟達拉賓)等,尚可在這些基礎方案中增加藥物或調整用藥劑量。在HLA半相合或無關供者造血幹細胞移植的預處理方案中通常加用抗胸腺細胞球蛋白或抗淋巴細胞球蛋白。再生障礙性貧血進行異基因造血幹細胞移植的預處理方案多選擇大劑量環磷醯胺聯合抗胸腺細胞球蛋白。白血病自體造血幹細胞移植可選用上述某種預處理方案,但惡性淋巴瘤自體移植常用的預處理方案為CBV(環磷醯胺+卡莫司汀+依託泊苷)或BEAM(卡莫司汀+依託泊苷+阿糖胞苷+美法侖)。多發性骨髓瘤自體造血幹細胞移植的預處理方案多選擇大劑量馬法蘭。根據預處理強度的不同,可分為清髓性預處理和減低劑量的預處理方案。清髓性方案主要通過聯合套用多種化療藥物進行超大劑量的化療,有時配合以放療來達到預處理的目的。這種預處理方式能夠最大限度的清除體內的殘留病灶以減少基礎疾病的復發,但由於毒性作用較大而增加移植相關死亡率。因此對於多數耐受性較好,特別是年輕的惡性疾病患者主張清髓性預處理方案進行造血幹細胞移植。經過多年的不斷改進,目前Cy/TBI和Bu/Cy成為臨床中最為經典的清髓性預處理方案,二者在長期生存率方面沒有明顯的差別,對於急性淋巴細胞白血病患者推薦含有TBI的預處理方案。減低預處理劑量的預處理方案所套用的化療和放療劑量都比較小,其主要目的是抑制受者的免疫反應,便於供者的細胞植入,以形成供受者嵌合體,並通過供者淋巴細胞輸注逐步變為完全嵌合體,發揮移植物抗腫瘤作用。此種預處理方案的毒性作用較小,受者內臟器功能受損較少,主要適用於疾病進展緩慢、腫瘤負荷相對較小、年齡大或重要臟器功能異常而不適合常規移植的患者。減低預處理劑量的預處理方案中的化療藥物主要是免疫抑制作用較強藥物,如氟達拉濱及抗胸腺細胞免疫球蛋白,放療劑量可低至2Gy。由於預處理後殘存的腫瘤細胞較多,免疫抑制作用較弱,可能影響供者幹細胞的植入,同時增加了移植後基礎疾病復發的機會。此外,移植後供者淋巴細胞輸注也可能給這類患者帶來更多的移植物抗宿主病等問題,還需要更進一步的探索。
骨髓採集
1)骨髓採集的方法:供者術前注意休息,保持良好的精神狀況。還應加強營養,但不要食油膩食物,以防骨髓血中脂肪過多,造成骨髓血回輸困難。採集骨髓血前一天需住院,住院當天晚上進半流食,麻醉師將進行相關檢查,告知麻醉期間的相關問題及注意事項,供者簽署麻醉知情同意書。採集骨髓血前12h應禁食、禁水。供者進入手術室,經硬膜外麻醉後採集骨髓血,整個採集骨髓血的過程約需1-2小時。採集點一般為兩側髂後上棘和髂前上棘,採集方法遵循一個部位多方向、多層面的穿刺原則。注射器要預先加入含肝素的RPMI1640細胞培養液,所採集骨髓實際上是血液與骨髓的混合液,又稱為“骨髓血”。採集骨髓血後供者回病房應去枕平臥休息6小時,先不要進食喝水。4小時後可喝少量的水。骨髓血採集量以其含的有核細胞數和患者的體重決定,單獨異基因骨髓移植所需要的有核細胞數最好達到3×108/kg以上,所采骨髓血液的總量約0.5-1升。由於採集的骨髓里有一些骨髓小顆粒,需要採取過濾並壓碎措施,以防骨髓血輸注時發生肺栓塞。常用的過濾方法包括針頭過濾和不鏽鋼網過濾。2)血型不合骨髓的處理:①供者和受者ABO血型主要不合時(即供者有受者不具備的血型抗原),採集的骨髓需套用羥乙基澱粉等方法進行去除紅細胞的處理,以免出現急性溶血反應。處理後所得血漿中富含骨髓細胞,而紅細胞輸回供者。
②供者和患者ABO血型次要不合時(即供者具有受者不具備的血型抗體),當供者的血型抗體滴度高於1:256時,可能導致不同程度的溶血。此時最簡便的方法是離心棄去部分血漿。
③供者和受者ABO血型雙向不合時,按上述兩種方法處理。
3)骨髓輸注:上述骨髓血均有外周靜脈或中心靜脈輸入,所用輸血器中不應有過濾網。異基因骨髓應儘量在採集後6小時內輸完,凍存的自體骨髓應在40℃水浴快速解凍後儘快輸注。由於骨髓中的脂肪可能引起肺栓塞,所以每袋的最後10ml應留在輸液袋內棄去。用肝素抗凝的骨髓輸注時要輸以相當量的魚精蛋白,每100單位肝素需1mg魚精蛋白。
造血幹細胞移植治療的費用
事實上,移植治療的費用並不比普通化療昂貴。常規的化療在緩解後通常需要維持3年,平均2-3月就要進行一次化療,每次化療的費用通常在1-2萬元左右,包括了化療藥、抗生素、成份血等治療的費用,維持治療的總花費也在20萬左右。而移植治療的常規花費也在20萬左右,與維持化療的費用相當。移植治療和維持化療的費用區別就在於,一個是一次性付清,另一個分期付款,但對於大部分髓性白血病、高危急淋的患兒來說,幹細胞移植有更好的臨床療效,因此移植治療有更高的性價比。