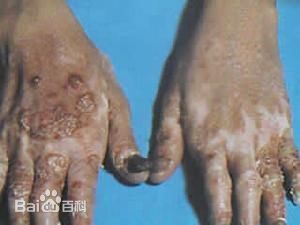
流行病學
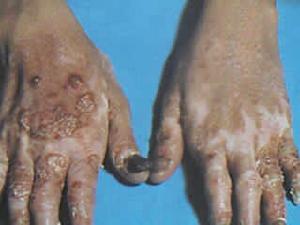 紅皮病型
紅皮病型2.國外統計發病率分別為2/100萬(美國,1977)、1.4/1100萬(荷蘭1978)、4.8/100萬(丹麥1963~1967年,平均8例/年)、8.1/100萬(瑞典,1958~1971年,平均15例/年)中國曾統計上海市13個醫院初診病例(1974)共16例。中國醫學科學院皮膚病研究所共發現35例(1980)我們自1954~1993年共見153例,按同期初診皮膚病患者數折算,占0.061%,略少於日本(O.071%);近年來有增加趨勢平均每年發現10~15例。男女比例為1.86∶1。與國外相比(男性51.6%~68%,女性32%~48.4%)男性稍多見。發病年齡為11~82歲,95例(73%)為30~39歲,較國外約早10年(40~60歲多見)。
病因
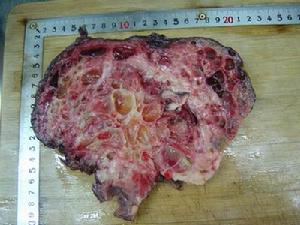 惡性腫瘤
惡性腫瘤發病機制
發病機制還不十分清楚,但對本病的發病機制提出以下的假說本病的皮膚浸潤經過3個階段:
1.不典型皮膚浸潤階段雖然對本病的最初組織病理變化仍有爭論,認為一開始為相互作用的T淋巴細胞和單核細胞的不典型浸潤,以後可消退局部持久存在或受不同影響發展成下個階段。
2.皮膚擴展階段上述不典型浸潤細胞可以影響再循環T細胞,當後者進入其他部位皮膚時,引起同樣的不典型相互作用或激發最初浸潤的因素直接影響其他部位鶒的皮膚,發生不典型多形性浸潤。隨著病變的發展,形成斑塊或腫瘤時,浸潤變得更單一主要為T細胞性瘤細胞,甚至在此期已有極輕微的系統性免疫異常。
3.系統性病變階段當皮損發展或累及血液其他內臟時單一形T細胞性瘤細胞浸潤突出患者細胞免疫明顯異常。異常免疫反應可發生在各個方面,可因遊走和再循環的異常方式尚未明確的皮膚刺激的傳遞(持續性抗原、環境中變應原)、異常T淋巴細胞的反應或輔助或抑制成分健康搜尋的異常調節而在組織中發生淋巴細胞和巨噬單核細胞的聚集。MF的發生與環境因素(如接觸石油工業品、工業廢物、廢氣、放射性污染物、殺蟲劑、農藥以及其他變應原,如光線或病毒)、機體易感性、異常淋巴細胞——單核細胞或淋巴細胞——Langerhans細胞相互作用,或異常抗原持續性刺激均有關係。根據上述假設和推理,他認為本病在早期為“反應性”,而後發展成惡性新生物性。
臨床表現
MF原發於皮膚但最終淋巴結和內臟常受累。
1.臨床表現和組織病理分期典型病例在臨床上和組織病理上可分3期,即紅斑期、斑塊期和腫瘤期。3期可互相重疊,因而3期損害可同時出現。
(1)紅斑期鶒:皮疹呈斑片狀,通常扁平面不萎縮,但有些患者則表現萎縮扁平非萎縮型斑片常有鱗屑附著,類似銀屑病或濕疹,後者呈圓形、卵圓形,亦可呈環狀多環狀或弓形。萎縮型斑片表面光亮,易皺縮,正常溝嵴消失,毛細血管擴張,色素減退或色素增深臨床上。呈血管萎縮性皮膚異色症,大斑塊型副銀屑病或斑駁性副銀屑病鶒。扁平非萎縮性斑片通常數月數年後繼發浸潤,也可出現內臟損害健康搜尋,而扁平萎縮性斑片則只有12%的患者演變為侵襲性MF,其餘患者保持現狀無改變
(2)斑塊期:由紅斑期進展而來,或在正常皮膚上發生,呈不規則性,界限清楚略高起的斑塊,顏色黃紅色、暗紅色至紫紅色不等。可自行消退,亦可融合為大的斑塊邊緣呈環狀弓形或匍行性,顏面受累時褶皺加深形成“獅面”。斑塊可互相融合成廣泛性,但有散在的正常皮膚存在。損害進一步發展可發生疼痛性表淺潰瘍。此期常發生淋巴結腫大,無觸痛,性質堅實,可自由推動。
(3)腫瘤期:可發生於原有斑塊上或正常皮膚上。皮損為大小不等,形狀不一的褐紅色高起結節,傾向早期破潰,形成深在性卵圓形潰瘍,基底被覆壞死性淡灰白色物質,潰瘍邊緣捲曲,好發於軀幹部,但亦可發生於任何部位甚至口腔和上呼吸道,一旦腫瘤發生,患者通常在數年內死亡。此外MF可見紅皮病型亞類,呈全身性剝脫和皮膚潮紅,毛髮稀少,甲營養不良掌跖角化有時全身性色素增深。偶亦見毛囊性黏蛋白病,色素減退損害與MF伴發健康搜尋。
檢查
1.血象早期血紅蛋白正常,晚期可有輕度貧血。偶或為溶血性貧血。有些病例白細胞增加。嗜酸粒細胞和單核細胞增加淋巴細胞減少這在泛發性斑塊和腫瘤期患者中尤為常見。提示預後較差我們的病例大多為Ⅰ~Ⅱ期,27.5%有嗜酸粒細胞增加,47.5%有單核細胞增加76%有淋巴細胞減少。文獻報導約20%病例(我們70.8%的病例)血中可找到異常淋巴細胞,占有核細胞數的6%~35%,大多在20%以下。
2.骨髓象健康搜尋一般正常,偶見漿細胞增加。我們檢查9例,6例嗜酸粒細胞和漿細胞增加,2例巨噬細胞增生6例見異常淋巴細胞鶒占有核細胞數2%~3%
3.外周血電解質正常,我們測定20例血鈣均正常。尿酸可增加。晚期血清白蛋白減少,α1球蛋白和α2球蛋白增加。循環輔助T細胞減少,對PHA刺激的反應性降低,無效細胞增加,單核細胞趨向性降低,單核細胞抑制因子減少,血清IgG和IgE增加健康搜尋。
4.紅細胞沉降率測定70例,其中60例(80.5%)有不同程度的增快(15~30mm/h)。
5.免疫測定①細胞免疫反應(包括結核菌素試驗、DNCB試驗、鏈素反應以及淋巴細胞轉換率測定)呈陰性或低於正常。40例DNCB試驗,其中22例(53.84%)為陰性;50例OT試驗健康搜尋,其中32例(64.28%)為陰性;20例LTT,其中15例(78.58%)低於正常。②螢光檢查示血管壁中有IgG、IgA、IgM和IgD沉積。
6.其他如肝臟累及時,血清鹼性磷酸酶值增加其他肝功能測定也異常。肺臟受累時,X線攝片示腫瘤樣陰影,但無特徵性。
治療
以增強患者免疫力為主。許多療法可使疾病獲得時間不等的緩解。局部皮質類固醇激素治療局部氮芥治療或卡莫司汀(卡氮芥)和PUVA可用於分期ⅠA,ⅠB和ⅡA。全身皮膚電子束治療可用於分期ⅡA,ⅡB。單劑化療或光免疫化學療法可用於早期治療Ⅲ期患者健康搜尋系統性化療,維A類,光化學免疫療法和α干擾素可用於Ⅵ期治療。
1.局部皮質類固醇激素療法早期(斑片期T1和T2)可用高強皮質類固醇乳劑外用T1患者完全緩解為63%,總有效率為94%。T2患者完全緩解率僅25%,總有效率為82%。治療停止後易復發
2.局部氮芥療法100mg氮芥溶於60ml自來水中外用全身(陰部除外),每天1次套用數月。80%ⅠA患者,68%ⅠB患者,61%ⅡA患者,49%ⅡB患者60%Ⅲ期患者顯效。約10%患者可獲得長期緩解8年以上主要副作用為皮膚過敏;套用軟膏基質可減輕反應,但療效較水劑差。治療停止後至少1/2患者復發,再治療仍有效。
3.局部卡莫司汀(卡氮芥)治療配製每毫升含2mg卡莫司汀的乙醇液每天用此種原液5ml加水至60ml。每天1次外用全身(皺襞部、陰部及手足部如無皮損,可不用)皮損局限時,可僅外用於患部平均療程8~12周。如經3~6個月治療無效,則可將藥物濃度加倍,重複治療12周。小片及頑固性皮損可直接用原液外用治療。患者對卡莫司汀(卡氮芥)的耐受性較氮芥好接觸過敏少見。但套用低濃度卡莫司汀(卡氮芥)患者中,少於10%的患者可發生骨髓抑制。長期套用卡莫司汀(卡氮芥)治療者可發生持久和嚴重的毛細血管擴張。
4.紫外線療法約75%斑片期患者,用UVB治療可完全緩解。PUVA套用更廣由於其較深的穿透性,更適合真皮內損害。限局性斑片或斑塊損害的患者中,88%的患者損害完全緩解,損害廣泛者,52%患者可完全緩解。腫瘤期患者無效紅皮病患者對PUVA耐受性差。PUVA治療緩解期短,平均約1年,因此需經常維持治療。亦可用維A類和干擾素α與PUVA聯合套用。
5.體外光化學療法治療前患者服用補骨脂素,然後將血細胞抽出用PUVA在體外處理約20%的MF皮損完全緩解,20%患者部分緩解鶒。紅皮病患者總有效率為80%。本療法費用昂貴,應先考慮其他更經濟的治療方法。
6.放射療法全身電子束治療,劑量超過3000Gy對MF的治療很有效。分期T1患者98%可完全緩解;T27l%;T336%;T464%。T1患者50%可長期緩解;T2患者20%可長期緩解。紅皮病型耐受性差。常見副作用為紅斑,水腫損害加重,禿髮和甲脫落。
7.生物反應改變劑α干擾素對MF治療有效率約60%,19%可完全緩解。可有發熱、寒戰白細胞減少和抑鬱等毒副作用。干擾素療法可與維A酸療法聯合套用。
8.維A酸類維A酸(異維甲酸)和阿維A酯(依曲替酯)治療MF44%有效開始劑量1mg/(kg•d)健康搜尋,根據患者耐受劑量可增至3mg/(kg•d)。維A酸類對IB(T2)患者,Ⅲ期患者有效。對Ⅳ期患者可減輕症狀。Targretin為一種合成性維A酸,能與RXR受體優先結合,引起許多腫瘤細胞凋亡,對MF亦有效。
9.系統性化療系統性化療用於晚期MF治療,常用單鶒一製劑。氨甲蝶呤5~125mg/周,對T3患者治療有效。41%的患者可達完全緩解,17%患者部分緩解,總有效率為58%。平均存活率為8.4年69%患者可存活5年。環磷醯胺、多柔比星(阿黴素)、長春新鹼和潑尼松龍(CHOP)聯合化療可用於晚期患者。
10.熔毒療法DAB389IL-2為融合白喉毒素於白介素-2的重組體。此製劑可選擇性地與表達白介素-2受體的細胞接合導致該細胞死亡。該製劑治療表達白介素-2受體的MF病例,有效率為37%,其中完全緩解者為14%。副作用為發熱、寒戰低血壓、噁心和嘔吐。大劑量套用時可引起血管滲漏綜合徵(vascular-leaksyndrome)。