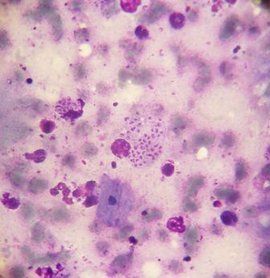
瑞氏染料
由酸性染料伊紅(E-)和鹼性染料亞甲藍(M+)組成。伊紅通常為鈉鹽,有色部分為陰離子。亞甲藍(又名美藍)為四甲基硫堇染料,有對醌型和鄰醌型兩種結構。通常為氯鹽,即氯化美藍,有色部分為陽離子。美藍容易氧化為一、二、三甲基硫堇等次級染料(即天青)。將適量伊紅、美藍溶解在甲醇中,即為瑞氏染料。甲醇的作用:一是溶解美藍和伊紅;二是固定細胞形態。
染色原理
既有物理的吸附作用,又有化學的親和作用。各種細胞成分化學性質不同,對各種染料的親和力也不一樣。如血紅蛋白、嗜酸性顆粒為鹼性蛋白質,與酸性染料伊紅結合,染粉紅色,稱為嗜酸性物質;細胞核蛋白、淋巴細胞、嗜鹼性粒細胞胞質為酸性,與鹼性染料美藍或天青結合,染紫藍色或藍色,稱為嗜鹼性物質;中性顆粒呈等電狀態與伊紅和美藍均可結合,染淡紫紅色,稱為嗜中性物質、原始紅細胞、早幼紅細胞胞質、核仁含較多酸性物質,染成較濃厚的藍色;中幼紅細胞既含酸性物質,又含鹼性物質,染成紅藍色或灰紅色;完全成熟紅細胞,酸性物質徹底消失後,染成粉紅色。
染液配製
溶劑
用 甲醇作瑞氏 染料溶劑,即成瑞氏染液。甲醇是瑞氏染料良好溶劑,有兩種作用:
( 1 )甲醇使瑞氏染料中美藍( M )與伊紅( E )在溶液中離解,可使細胞成分選擇性吸附其中的有色物質而著色。 在配製的瑞氏染液中美藍如放置過久即可氧化而含有天青,美藍天青與伊紅化合物能使核染成紫紅色,但不能使胞漿染為藍色,多餘 美藍就可以 使胞漿染成藍色,染色主要是化學作用,是離子彼此結合的反應。
( 2 )甲醇具有強大的脫水力,可將細胞固定在一定形態及增加細胞結構的表面積,提高細胞對染料吸收作用,同時由於甲醇吸附染色液中的水,使染色液升溫,加速染色反應。
瑞氏染液配製:
瑞氏染料 830gm 或 1g
甲醇( AR ) 500ml 或 600ml
先稱乾燥(事先放入溫箱乾燥過夜)瑞氏染料放置乳缽內, 用乳棒輕輕 敲碎染料成粉末,再行研磨至聽不到 研芝麻聲 即呈細粉末,加少許甘油或甲醇溶解研磨,使染料在乳缸內顯“一面鏡”光澤,而無染料粉粒沉著,再加較多量甲醇研磨呈一面鏡光亮,靜置片刻,將上層液體倒入 一 清潔儲存瓶內(最好用甲醇空瓶),再加甲醇研磨,重複數次,直至乳缽內染料及甲醇用完為止,搖勻,密封瓶口,存室溫暗處,儲存愈久,則染料溶解、分解就越好,一般儲存 3 個月以上為佳。
緩衝液
1) 緩衝液作用:染色對氫離子濃度是十分敏感的,據觀察 pH 值的改變,可使蛋白質與染料形成的化合物重新離解。 緩衝液須保持 一定的 pH 使染色穩定, PBS 的 pH 一般在 6.4~6.8 ,偏鹼性染料可與緩衝液中 酸基起 中和作用,偏酸性染料則與緩衝液中的鹼基起中和作用,使 pH 恆定。
2) 緩衝液配製( pH6.4~6.8 ,弱酸性):
配方 1 : 配方 2 :
1% KH 2 PO 4 30ml M/15 KH 2 PO 4 73.5 ml
1% Na 2 HPO 4 20ml M/15 Na 2 HPO 4 26.5ml
H 2 O( 新鮮 ) 加至 1000ml
置室溫黑暗處,瓶口密封,防止黴菌污染,如有污染則應報廢。
pH的影響
(pH6.4~pH6.8)
細胞各種成分均屬蛋白質,因蛋白質系兩性電解質,所帶電荷隨溶液pH而定,在偏酸性環境中正電荷增多,易與伊紅結合,紅細胞和嗜酸性粒細胞染色偏紅,細胞核呈淡藍色或不染色;在偏鹼性環境中負電荷增多,易與美藍結合,所有細胞呈灰藍色,顆粒呈深暗,嗜酸性顆粒呈暗褐,甚至棕黑色,中性顆粒偏粗,呈紫黑色。稀釋染液必須用緩衝液,沖洗用水應近中性,否則可導致細胞染色呈色異常,形態難以識別,甚至錯誤。
染色方法和注意事項
(1)血塗片乾透後固定,否則細胞在染色過程中容易脫落。
(2)沖洗時應以流水沖洗,不能先倒掉染液,防染料沉著在血塗片上。沖洗時間不能過久,以防脫色。如血塗片上有染料顆粒沉積,可滴加甲醇,然後立即用流水沖洗。
(3)染色過淡可以復染,復染時應先加緩衝液,然後加染液。染色過深可用流水沖洗或浸泡,也可用甲醇脫色。
(4)瑞氏染色Ⅰ液由瑞氏染料、甲醇(AR級以上)和甘油組成,Ⅱ液為PBS(pH6.4~pH6.8)。