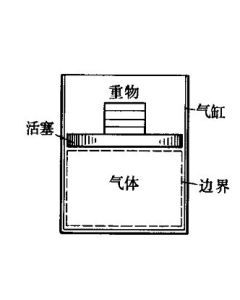
簡介
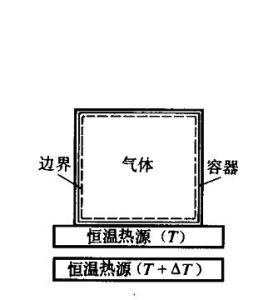 熱力過程
熱力過程容積V保持不變的熱力過程,又稱等容過程,例如密閉容器內的加熱或冷卻過程。過程方程為:V=常數,因此根據狀態方程有:式中p1、p2、T1、T2、分別為系統初、終態的壓力和溫度。定容過程在p-V圖(見圖)上由垂直線1-2表示。它表明系統對外不作功,向系統輸入的熱量Q全部轉變成系統內能U的增加,即式中m為系統的質量,cv為定容比熱容。
定壓過程
壓力p保持不變的熱力過程,又稱等壓過程。例如在大氣壓力下,氣缸中氣體的受熱膨脹。過程方程為:p=常數,因此V1/V2=T1/T2。它在p-V圖上由水平線3-4表示。這時,系統對外所作的功
W=p(V2-V1)=m﹙R÷M﹚(T2-T1)=nR(T2-T1)
外界向系統輸入的熱量
Q=H2-H1=mcp(T2-T1)
式中R為理想氣體的通用氣體常數,cp為定壓比熱容;H為系統的焓。
定溫過程
溫度T保持不變的過程,又稱等溫過程。例如室溫下緩慢地壓縮氣體的過程。過程方程為:T=常數,因此,p1V1=p2V2。它在p-V圖上由等邊雙曲線5-6表示,過程中向系統輸入的熱量等於系統對外界所作之功,右圖公式中ln為自然對數。
複雜過程
絕熱過程系統與外界沒有熱量交換的熱力過程。例如氣體在氣缸內的絕熱膨脹。可逆的絕熱過程在過程進行中其熵不變,故又稱定熵過程。過程方程為:pV=常數,因此有:式中,稱為絕熱指數或比熱容比,其中cv為定容比熱容。絕熱過程在p-V圖上表示為
高次雙曲線7-8,這時系統對外界所作的功。
多變過程
符合過程方程pV=常數,其中多變指數n在過程中保持不變的熱力過程。參數關係式為過程中向系統輸入的熱量系統對外界所作的功當多變指數n值分別取0、1、γ、±∞時,多變過程就相應地成為前面提到的定壓、定溫、絕熱和定容過程。