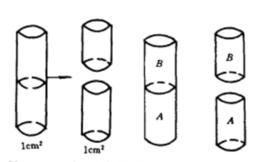
概念
兩部分完全相同的液體(A,A)相互接觸後,它們之間相互吸引的能量。這兩部分液體之間不會再形成新的界面,或者說要將同一種液體分開的話,為了克服分子間的相互作用力所需要消耗的能量,儘管這個實驗在實際上無法進行,但可以這樣計算所消耗的能量:
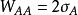 內聚功
內聚功式中:W為內聚功,σ為液體的表面張力。
此能量稱為液體的內聚功,即同種液體之間的吸引強度。相反的情況,則稱為黏附功,如圖b所示。
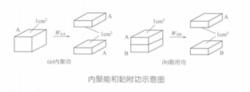 內聚功
內聚功表中列出了幾種液體的內聚功和這些液體對水的粘附力
 內聚功
內聚功套用舉例
研究內聚功、粘附功,根據K的正負判斷兩個相是否展開對冶金過程是有用的。例如,渣與金屬之間的粘附功為:W=σ +σ -σ
渣的內聚功為:W 2σ
所以K = W - W
為了使渣和金屬易於分離,必須使W< W,即希望K為負值。這就要求σ和σ越大越好。σ,說明渣的內聚功大,不易分散;σ大,說明渣與金屬界面縮小的趨勢大,有利於渣一金屬的分離。以鹼性電弧爐冶煉高碳鋼時,在還原期必須要造電石渣,才能對鋼液進行擴散脫氧和去硫。但是,電石渣中含有CaC,它會使渣一鋼界面張力降低,這就不利於渣與鋼液的分離,造成鋼的污染,使鋼的質量變壞,所以在出鋼時,先要把電石渣破壞,使之變為白渣(一種界面張力較高的渣)後再出鋼。