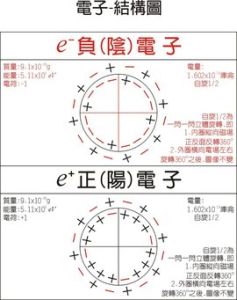
英文
化學裡面的術語
英文名稱:valence electron
舉例
1個CO2中含的價電子數為4+6×2=16個。
1個N2中含的價電子數為5x2=10個
價電子數
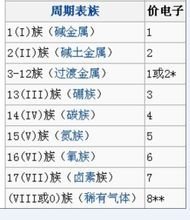 價電子
價電子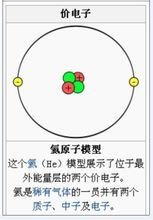 價電子
價電子化學作用
一原子最外層電子殼的價電子支配原子的化學鍵作用。因此,相同價電子數的原子在元素周期表被放置於同一列。一般來說,原子的價電子數愈少,活性就愈高。所以1族鹼金屬非常活潑,該族包括了鋰、鈉及鉀,它們是金屬中活性最高的一群。
每一個原子,如果有滿原子價的話都穩定得多,換句話就是活性會低得多。實現這個有兩個方式:一個原子可以跟鄰近原子分享電子,一條共價鍵,或者從其他原子中移走電子,一條離子鍵。另一種離子鍵需要一原子把它的一些電子送給另一個原子;這也可以,因為把整個外層送出就能剩下滿原子價。通過移動電子,兩原子就連結起來了。這就是化學鍵,而且就提它們把原子建成分子及離子化合物。共有三種主要的化學鍵和一種大小比化學鍵小得不多的分子間作用力:
離子鍵
共價鍵
配位鍵(這是一種特殊的共價鍵,由一個原子提供兩個電子)
氫鍵(這是一種分子間作用力)
金屬鍵
價電子同時亦決定該元素的電導性能。