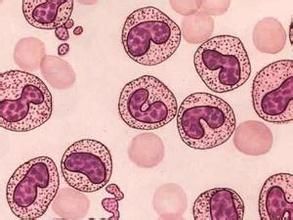
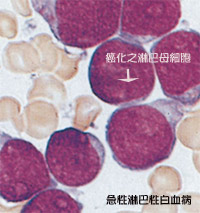
 急性淋巴細胞白血病
急性淋巴細胞白血病 疾病描述
急性淋巴細胞白血病(ALL)是急性白血病的一種類型。ALL是兒童最常見的白血病類型, 成人發病率較低,占成人急性白血病的15%~25%,老年人患病率 更低,占急性淋巴細胞白血病的14%左右。
症狀體徵
 急性淋巴細胞白血病症狀
急性淋巴細胞白血病症狀 1.貧血是由於骨髓紅系細胞的增殖受抑 ,部分病例存在紅細胞壽命的縮短,以及出血等亦是導致貧血的原因,當然在套用 化學治療後,藥物抑制了紅系細胞的增殖,又可加重貧血症狀。
2.發熱半數的患 者以發熱為早期表現。可低熱,亦可高達39~40℃以上,伴畏寒、出汗等。雖然白血病本 身可以發熱,但較高熱往往提示有繼發感染。導致感染的原因是機體免疫功能 的低下,包括正常白細胞增殖的受抑,粒細胞減少,細胞免疫功能低下等,當患者進行化 學治療後,包括套用腎上腺皮質激素後更易患感染。常見的感染為上呼吸道感染,其中以 口腔炎最多見。齒齦炎或咽峽炎,嚴重時可發生潰瘍甚至壞死。此外,肺炎、 腸炎 、腎盂腎炎、肛周炎、癤腫也較常見。嚴重感染可並發菌血症或 敗血症。有些患者可有發熱而找不到感染灶。白血病開始階段的感染多數是細菌感染 ,尤其是革蘭陰性桿菌感染,後期病例往往夾雜真菌感染,或是細菌的混合感染。後期病 例可見肺孢子蟲感染及巨細胞病毒感染 。
3.出血出血的原因主要是血小板減少, 血小板減少的原因是由於骨髓巨核細胞增殖受抑,其次是白血病細胞的血管壁浸潤,部分 並發彌散性血管內凝血者則出現明顯的出血症狀,化學治療後由於同時抑制了巨核細胞的 增殖會加重出血症狀。出血最嚴重的是顱內出血,顱內出血者常伴有顱內白血病細胞浸潤 ,常是白血病致死的原因之一。有資料表明急性白血病死於出血者占62.24%,其中87%為顱 內出血。
4.器官和組織浸潤的表現白血病細胞可有多臟器的浸潤,出現不同的 浸潤症狀:
(1)多見的是骨髓的浸潤出現胸骨壓痛,骨及關節的浸潤出現疼痛症狀 ,少數病例的骨痛症狀是由於白血病骨髓壞死所致。
(2)淋巴結、肝、脾的浸潤可 出現不同程度的腫大。較急非淋常見,各約占75%、85%、78%。
(3)約有10%的病例 在起病時即有頭痛、噁心、嘔吐,已有中樞神經系統白血病的表現。腦脊髓膜浸潤出現腦 膜白血病是中樞神經系統白血病浸潤的常見類型,中樞神經 系統白血病(CNS-L)還可表現為腦實質的浸潤以及脊髓的浸潤,根據不同部位可出現相 應的定位體徵。
(4)皮膚浸潤在急淋中並不多見,若有皮膚累及者,多系早期B細 胞表型者。
(5)睪丸受浸潤,出現無痛性腫大,多為一側性,另一側雖不腫大,但 活檢時往往也有白血病細胞浸潤。睪丸白血病多見於急淋白血病化療緩解後的男性幼兒或 青年,是僅次於CNS-L的白血病髓外復發的根源。
5.分型對白血病的分型已從70年 代FAB分類法演進到今天的MICM分型(形態、免疫、細胞遺傳學和分子生物學)
(1) FAB形態學分類:急淋分為3個亞型L1,L2,L3。
(2)免疫學分類:
①B細胞的免疫表達早期前B細胞示HLA-DR,TdT(末端脫氧核苷酸轉移酶),CD34, CD19,CD24,CD10(CALLA)等陽性;前B細胞示HLA-DR,CD19,CD24,CD10,CD20、Cμ(胞 漿重鏈)陽性,B細胞示HLA-DR,CD19,CD24,CD10,C20,CIg,C21陽性。
②T細 胞的免疫表達T細胞抗原CD7是最敏感的,但有的T細胞急淋者會示陰性結果,因此須加測 CD5及CD2。兒童T細胞急淋很少表達HLA-DR陽性。CD3常示胞質陽性及表面陰性。
(3)細胞遺傳學分類:急淋的染色體改變:前B細胞急淋t(1;19);B細胞急淋t(8;14)、t (2;8)、t(8;22);T細胞急淋t(11;14)、t(1;14)、t(8;14)、t(10;14)、t(7;9)、 t(7;14)、INV(14)。此外尚可在急淋中有t(9;22),常為預後欠佳的染色體改變。
(4)分子生物學:隨著分子生物學技術的不斷發展,如PCR、FISH和原位PCR基因診 斷技術,有些白血病患者未發現有染色體異常,但基因診斷技術可發現異常 的融合基因;如t(8;14)(q24;q32)的myc與免疫球蛋白(Ig)基因融合、t(1;19)(q23; p13)的E2A與PBX基因融合、t(1;14)(p32;q11)的SCL(TAL-1)與TCR基因融合、t(10;14) (q24;q11)的HOX-11與TCR基因融合、t(11;14)(q13;q32)的BCL-1與Ig基因融合和t(14; 18)(q32;q21)的BCL-2與Ig基因融合。這些融合基因常常與急淋有關。
疾病病因
 老年人急性淋巴細胞白血病病因
老年人急性淋巴細胞白血病病因 診斷檢查
 老年人急性淋巴細胞白血病檢查
老年人急性淋巴細胞白血病檢查 診斷:急淋的診斷主要依靠骨髓檢查,見大量原始淋巴細胞,至少在25%,但一般急淋 的骨髓象其原始細胞比例遠超過25%。
實驗室檢查:
1.外周血象白細胞計數於 發病時,約有60%病例是增高的,>10×10E9/L,其中超過50×10E9/L者占近1/4病例。白 細胞計數愈高,則原始淋巴細胞的比例亦愈高;白細胞計數不高者,有的較少出現原始細 胞或不出現原始細胞,即所謂的亞白血病性白血病及非白血病性白血病 。若外周血白細胞計數>50×10E9/L(5萬/mm3)。往往有明顯的淋巴結、肝、脾腫大,並常為T 細胞免疫表型者。紅細胞計數常見降低,多數病例(2/3病例)呈中等度貧血,血細胞比容< 30%,屬正細胞、正色素性貧血。血小板計數降低,約有60%以上病例<50×10E9/L(5 萬/mm3)。
2.骨髓檢查骨髓液穿刺除作瑞氏染色形態學檢查外,還可作免疫表型, 組織化學及細胞遺傳學檢測。當骨髓細胞密度甚高,以及網狀纖維增生而致骨髓液抽取有 困難時(出現“乾抽”現象),則必須作骨髓活檢。骨髓檢查呈現細胞增生增高,並見大量 淋巴系白血病細胞,但髓系及紅系前體細胞的形態是正常的,但數量減少,巨核細胞常示增生不良。
3.細胞化學過氧化物酶陰性;糖原PAS反 應陽性成塊或顆粒狀;非特異性酯酶陰性;中性粒細胞鹼性磷酸酶增加。
4.血液 生化
(1)血尿酸測定由於白血病細胞的細胞轉換率高,因此出現代謝紊亂 ,表現血尿酸增高,但很少見痛風症狀,然而要注意是否會出現尿酸性腎病,即使在 沒有過高的白血病細胞時,亦會有血尿酸的增高。更要注意的是當患者同時有嚴重脫水時 ,尿酸性腎病發生的可能更大,甚至可致嚴重腎功能減退。
(2)血乳酸脫氫酶是增 高的,原因是白血病細胞的轉換增加。
5.腦脊液(CSF)檢 查兒童急淋初發者約有3%病例有中樞神經系統的侵犯,除一般CSF常規檢查外,CSF離心沉 淀濃縮找白血病細胞對診斷是有幫助的。需注意的是當外周血細胞很高,白血病細胞比例 很高時,腰椎穿刺可能造成的出血,會導致外周血白血病細胞的“種入”,因此有主張腰 椎穿刺遲緩幾天操作,待化療後外周血白細胞已明顯下降不易找到白血病細胞時再做腰穿 比較妥善。有中樞神經系統(腦及脊髓膜)浸潤時,表現為CSF壓力增高 ,蛋白增多,糖降低,並可見白血病細胞。
其他輔助檢查:X線檢查:胸片示前縱隔腫塊者占 5%~10%病例,胸腺腫大常伴有胸腔積液。這類病例常見於T細胞急淋者。
鑑別診斷
 老年人急性淋巴細胞白血病診斷
老年人急性淋巴細胞白血病診斷 2.由於急淋臨床的非特異性症狀表現如發熱、關節症狀,有輕度貧 血要與幼年型類風濕性關節炎或紅斑狼瘡相鑑別,切忌在診斷未明時濫用 腎上腺皮質激素,不然將導致症狀緩解,延誤診斷。
3.某些感染性疾病如傳 染性單核細胞增多症、弓形體病、巨細胞病毒感染 均可有發熱、淋巴結腫大及肝脾腫大,並外周血可見異形淋巴細胞,鑑別主要靠細胞 形態學檢查。
4.此外急淋中的非白血病性白血病型亦要與再障急做鑑別,但骨髓 檢查有助於此2類疾病的鑑別,生化方面再障病例的血尿酸及乳酸脫氫酶均是降低的,而在 白血病時可以升高。
治療方案
 老年人急性淋巴細胞白血病治療
老年人急性淋巴細胞白血病治療 (1)糾正貧血:多數病例在發病 時有中等度貧血或重度貧血,貧血的徹底糾正有待白血病的緩解,但在疾病尚 未取得緩解而又有重度貧血者,組織缺氧症狀明顯者,又因在化療過程中可能加重貧血症 狀,因此需作適當補充治療以糾正貧血。一般宜使血紅蛋白維持在50g/L以上,以免產生明 顯的組織缺氧及有關臟器(如心臟)的功能影響。輸血量不宜過多,以防導致體內臟器組織 含鐵血黃素沉積,產生血色病。若單純以糾正貧血為目的而輸血,可輸注紅細胞懸液,以 避免過多的輸入白細胞及血小板而導致免疫反應。
(2)發熱處理:多數白 血病患者於發病時或病程中有發熱。發熱的原因絕大多數是由於感染所致,因此對發熱病 例體溫>38℃者需作仔細的病原菌檢測,如咽拭培養,血、尿、痰液培養,X線胸部檢查等 。病程早期的發熱多數是細菌感染,外周血白細胞計數<1×10E9/L者,多見的是革蘭陰性 桿菌感染。發熱病例採樣作病原菌檢測後即進行治療。常用的抗生素組合是頭孢菌素加氨 基糖甙類,例如頭孢他啶(復達欣)加阿米卡星。當然抗生素的選擇應根據不同病期,不同 感染部位,外周血白細胞高低等情況來估計可能的病原菌而選用不同的抗生素。對疑及有 革蘭陽性球菌、金葡菌感染者宜加用萬古黴素,以後待藥敏試驗有結果後再予以調整。晚 期病例的發熱可能是卡氏肺孢子蟲感染,常表現為肺孢子蟲肺炎,治療可用甲氧苄啶 (磺胺增效劑;三甲氧苄氨嘧),20mg/(kg/d),加用磺胺甲噁唑(Sulfamethoxazele) 100mg/(kg/d),口服或靜脈注射,療程為14天。亦可套用噴他脒(戊烷脒)4mg/(kg/d),肌 注,療程10~14天,噴他脒(戊烷脒)對腎臟有毒性,亦有白細胞、血小板降低及低血糖等 副反應,臨床應注意。晚期病例,特別是用過多種抗生素及長期反覆套用腎上腺皮質激素 及化療藥物者,易並真菌感染,可用酮康唑0.1~0.2g口服,3次/d或用氟康唑200~ 400mg靜脈滴注,1次/d,或用兩性黴素B靜脈滴注,劑量由1mg/d開始 ,逐日增加至每日總量1mg/kg。有發熱感染嚴重者,在套用抗生素的同時可靜脈滴注大劑 量人血丙種球蛋白,400mg/(kg/d),療程5天左右。對嚴重感染而外周血有顆粒細胞缺乏者 ,可皮下注射G-CSF或莫拉司亭(GM-CSF),300μg/d,療程7~10天。對未能找到感染病灶 ,多種病原菌檢查陰性,多種抗病原菌治療又不見效者,其發熱原因少數可能是由於白血 病本身的代謝所致,可給予對症處理,如對乙醯氨基酚(必理通)0.5~1.0g,1~3次/d,或 用吲哚美辛(消炎痛栓劑)25~50mg肛用。
(3)出血處理:出血的原因主要是血小板 減少,因此補充血小板是治療出血的有效措施。連續單採血小板懸液,每隔天輸注250ml, 亦可輸注非連續單採血小板懸液或新鮮全血。止血藥物卡巴克絡(安絡血)10mg口服,3次/d ,酚磺乙胺(止血敏)1~2g靜脈滴注,1次/d。由於白血病患者的出血絕大多數並非由於纖 維蛋白溶解所致,並且白血病患者易並發彌散性血管內凝血,因此除非有足夠的實驗依據 證實是由於纖維蛋白溶解而致出血,否則不宜套用抗纖溶藥物。若並有DIC,肝素宜用小劑量 12.5~25mg,1次/6h。
(4)高尿酸血症處理:血尿酸>420μ mol/L(7mg/dl),口服別嘌醇每次0.1g,3~4次/d,待血尿酸下降後可減為1~2次/d,每次 0.1g,同時給碳酸氫鈉口服,3次/d,每次1g以鹼化尿液,並補充適量液體,保持足量尿液 ,對化療前外周血白細胞明顯增高者,於化療的同時可套用別嘌醇預防高尿酸血症的出現 。
(5)維持營養:白血病系嚴重消耗性疾病,特別是化、放療的副作用引起患者消 化道功能紊亂。應注意補充營養,維持水、電解質平衡,給患者高蛋白、高熱量、 易消化食物,必要時經靜脈補充營養。
2.化學治療化學治療可分為2個主要階段, 即誘導緩解治療及緩解後治療。誘導緩解治療的目的是使病情穩定,達到完全緩解標準。 所謂完全緩解,即白血病的症狀和體徵消失,Hb≥100g/L(男)或90g/L(女及兒童),中性粒 細胞絕對值≥1.5×10E9/L,血小板≥100×10E9/L,外周血白細胞分類中無白血病細胞; 骨髓象:原粒細胞+早幼粒細胞(原單核+幼單核細胞或原淋巴+幼淋巴細胞)≤5%,紅細 胞及巨核細胞系列正常。白血病細胞增殖周期大致為5天左右。有些抗白血病藥物作用於周 期中的特定階段。所以每1個療程化療需持續7~10天,致使各增殖期的白血病細胞都有機 會被藥物殺滅。每1個療程結束後,間歇2周再用第2療程,其目的是使正常造血恢復,且誘 使休止期(GO期)白血病細胞進入增殖周期 ,有利於下1個療程化療藥物的殺滅。急性白血病未治療時體內白血病細胞的數量估計 為10E10~10E13,經誘導緩解階段治療達到完全緩解標準時體內白血病細胞估計在10E8~ 10E9,且在髓外某些隱蔽之處仍可有白血病細胞浸潤。因此,完全緩解後應實施鞏固強化 階段的治療4~6個療程。然後進入維持階段,化療將持續較長時間,以便進一步消滅殘存 白血病細胞,防止復發,延長緩解和無病生存期。目前多採用聯合化療,藥物組合應符合以 下各條件:①作用於細胞周期不同階段的藥物;②各藥物間有相互協同作用,以最大限度 地殺滅白血病細胞;③各藥物副作用不重疊,對重要臟器損傷較小。
3.生物學治 療
(1)免疫治療:白血病時,由於化療、放療和疾病本身原因。患者的免疫功能低下, 通過非特異性免疫刺激,可使患者的免疫功能恢復,從而殺滅體內的殘留白血病細胞。早 期的觀察證實凍乾卡介苗(卡介苗)、左鏇咪唑等非特異性免疫治療可延長ALL的 緩解期,自從單克隆抗體技術問世以來,人們已用特異性抗ALL細胞表面抗原McAb治療 ALL,取得了一定療效,主要表現為外周血原淋巴細胞迅速減少,但其療效短暫,骨髓中白 血病細胞基本上沒有減少。尚無1例ALL患者套用單抗獲CR。其療效有待進一步觀察。
(2)干擾素治療:干擾素是具有廣泛生物學活性的調節蛋白,可抑制白 血病細胞的克隆性生長,提高白血病患者自然殺傷細胞的活性,並有加強致敏淋巴細胞, 增強巨噬細胞活性等作用。但在成人ALL臨床使用干擾素的療效有待進一 步觀察和研究。
4.造血幹細胞移植骨髓移植(BMT)是 成人ALL治療策略中一個重要組成部分。在大劑量化療和放療後,BMT能起到重建造血和重 建免疫功能。由於BMT使白血病患者能耐受大劑量的化療和放療,而且植活的異基因骨髓尚 有抗白血病的過繼性免疫治療作用,因此BMT為白血病患者提供了長期無白血病存活或根治 的機會。成人ALL第1次CR接受allo-BMT,5年生存率達45%以上。第2次CR後接受allo-BMT, 3年生存率為15%~41%,均明顯優於化療,後者化療CR2的年生存率僅5%。一般認為,成人 ALLBMT可選擇在CR1或CR2後進行,可明顯提高生存率和延長無病生存期。
5.擇優 方案急淋治療目前首選化療,採用聯合化療如DVP方案並輔以有效的免疫藥物及支持治療, 治療後注意預防髓外白血病的發生,有HLA相合供體者建議酌情做骨髓移植 ,最大限度地提高無病生存期。
預後及預防
 老年人急性淋巴細胞白血病預防
老年人急性淋巴細胞白血病預防 預防:提高機體免疫力,預防 感染為主。
流行病學
 老年人及嬰幼兒健康
老年人及嬰幼兒健康 1.地區分布白血病是世界範圍較多見的惡性腫瘤 ,屬於我國十大高發惡性腫瘤之一。我國白血病年發病率為2.73/10萬人口,標化率為 2.62/10萬人口,與日本相似(2.4/10萬~2.7/10萬人口),明顯低於歐美6.4/10萬~ 10.5/10萬人口。歐美國家的亞裔移民白血病發病率也明顯低於白種人。我國各地區白血病 發病率基本接近全國平均水平,少數地區白血病發病率與全國水平不一致。如河北開灤煤礦、湖北江漢油田 的白血病發病率各達6.11/10萬人口及7.40/10萬人口,提示環境污染 可能與白血病的發病相關。
2.性別、年齡分布各國男性白血病的發病均高於 女性。男、女之比為1~1.6∶1。1986年我國男性發病率為2.82/10萬人口、女性為2.45/10 萬人口,在老年期男性發病率明顯高於女性。白血病見於各年齡組,自 嬰幼兒至高齡老年。我國防大學1986年普查0~9歲及60~69歲年齡 階段存在不同程度的發病高峰。ALL多見於兒童,<10歲組中,ALL占70%,其次為AML,< 20歲組以AML較多見,ALL略次之,20~40歲組以AML居首,CML次之,>40歲以AML或CML為 多見。
3.白血病的類型分布我國白血病的類型隨年代進展而有所變化,表現為急 性病例增多。北京協和醫院1921~1942年慢性與急 性白血病之比為2.38∶1;1949~1955年為0.7∶1;1956~1958年則為0.33∶1。1986年普 查資料,1498例白血病中ANIL占57%,all27%,CML14%,CLL僅占2%,慢性白血病與急性之 比為0.24∶1,與非洲國家相似。西方國家慢性白血病發病率較高,尤其是CLL明顯多於亞洲國家。