病因
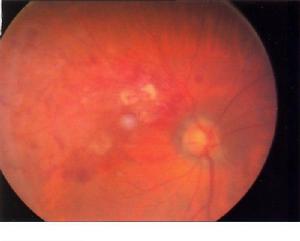 靜脈阻塞
靜脈阻塞視網膜中央靜脈阻塞根據有否視網膜缺血分缺血型(占25%)和非缺血型(占75%)2種,自然病程中無一例非缺血型發展為新生血管性青光眼,而缺血型中則有18%~60%發生多在靜脈阻塞後2~3個月時發生,80%病例在6個月內發生。主要通過眼底螢光血管造影來顯示有否視網膜毛細血管非灌注區來判斷缺血與否注意非缺血型也能轉變為缺血型。糖尿病就是一危險因素,糖尿病也是視網膜中央靜脈阻塞發生的一個危險致病因子。原發性開角型青光眼與視網膜中央靜脈阻塞有關,認為是機械性壓力作用所致因此將視網膜中央靜脈阻塞視作原發性開角型青光眼的危險因素。此外,80%發生了靜脈阻塞的患眼眼壓較對側眼的要低,認為這是代謝性酸中毒抑制了房水形成所致。
增殖性糖尿病性視網膜病變中約22%發生新生血管性青光眼,糖尿病中1型占15%且多伴增殖性視網膜病變2型占80%且多伴黃斑病變成人雙眼新生血管性青光眼或虹膜新生血管化幾乎均為糖尿病視網膜病變所致但發生視網膜病變與出現虹膜新生血管或青光眼的時間間隔不清楚。白內障手術、玻璃體視網膜手術後更易發生新生血管性青光眼,主要是與原先的糖尿病視網膜病變及視網膜缺氧有關。
其他較多見的伴發新生血管性青光眼的眼部疾病有:視網膜中央動脈阻塞(1%~17%),眼內腫瘤如惡性黑色素瘤(0.5%~15%)視網膜母細胞瘤的虹膜新生血管化可達30%~72%,玻璃體視網膜手術後的虹膜新生血管化也達23%~32%此外還見於諸如眼內血管性疾病的Coats病、靜脈周圍炎、鐮狀血細胞病;其他眼病有慢性葡萄膜炎、早產兒視網膜病變、虹膜異色症、剝脫綜合徵、鞏膜炎、眼內炎、交感性眼炎視神經纖維瘤病原發性虹膜萎縮、網狀組織細胞肉瘤、轉移性癌、眼外傷、Sturge-Weber綜合徵合併脈絡膜血管瘤,甚至白內障摘除等手術之後眼外血管性疾病如頸動脈阻塞病、頸動脈海綿竇瘺、無脈症、巨細胞性動脈炎等也可是新生血管性青光眼的病因。
發病機制
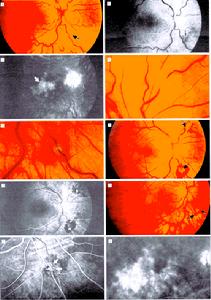 視網膜缺血
視網膜缺血臨床表現
新生血管性青光眼的共同表現有眼痛畏光視力常為眼前指數~手動,眼壓可達60mmHg以上,中到重度充血,常伴角膜水腫,虹膜新生血管,瞳孔緣色素外翻,房角內有不同程度的周邊前粘連。Shield將自虹膜新生血管形成至發生新生血管性青光眼的臨床病理過程分為3期,即青光眼前期、開角型青光眼期和閉角型青光眼期。
併發症:角膜水腫以及反覆性前房積血等。
診斷:根據原發病及臨床體徵,診斷不難。但需要鑑別。
鑑別診斷:早期診斷以便制定最佳的治療手段是NVG治療的關鍵。關於鑑別診斷,需要根據疾病的兩個階段進行考慮:一是早期僅有NVI,二是晚期已有眼壓升高角膜混濁和血管充血。無論處於哪一階段,全面而詳細的眼科病史和體檢通常可以確立診斷。對於真性NVG,病史至關重要,糖尿病、既往的視力損害(提示陳舊性CRVO或視網膜脫離)、高血壓或動脈硬化(提示可能存在的頸動脈疾病)均有臨床價值,即使後節檢查外觀良好也不應該完全排除NVI。
治療方案
常規濾過性手術常常失敗,術前全視網膜光凝術或冷凝術使新生血管退化,或術中術後套用抗代謝藥可提高手術成功率。房水引流裝置或閥門植入手術近年也用於治療新生血管性青光眼。若上述方法失敗,可考慮睫狀體破壞手術減少房屋水形成,降低眼壓以緩解症狀。視網膜缺氧和毛細血管無關注是虹膜新生血管形成的根源,一旦發現視網膜有缺血現象時應作廣泛視網膜光凝術,以預防虹膜新生血管的發生。
治療
(1)全視網膜光凝(panretinal photocoagulationPRP):PRP的作用機制尚不明了由於視網膜缺血是發生NVI的關鍵因素,PRP必然在某種程度上消除了血管形成因子的來源或拮抗了其效應。視網膜缺氧引起視網膜血管慢性擴張,進而引起視網膜新生血管形成。視網膜血管供養內層視網膜,視網膜氧消耗總量的2/3卻在外層和色素上皮層。光凝可以選擇性地破壞高氧耗的外層,使脈絡膜的氧成分向視網膜內層擴散從而緩解內層視網膜的缺氧。視網膜血管的自動調節機制表現為在周圍環境低氧水平時擴張,高氧水平時收縮。
2)全視網膜冷凍:在指征適於PRP治療時,但因為角膜、晶狀體或玻璃體混濁明顯影響眼底可見度,可以考慮施行全視網膜冷凍。全視網膜冷凍作為一項主要的治療措施,比PRP造成更明顯的炎症和血-視網膜屏障破壞,其潛在性併發症包括牽引性和滲出性視網膜脫離以及玻璃體積血。已經失去有用視力的患眼,同時套用全視網膜冷凍和睫狀體冷凍,可以同時控制NVI和眼壓,但術後炎症和疼痛比較嚴重。因此,只有在其他治療失敗或不可能進行時,作為最後一項措施,採用冷凍治療
(3)虹膜角膜角光凝:房角光凝最早提出於1977年,當時正在評估PRP在治療NVG中的作用和有效性。某些情況下,在PRP治療前,先行房角光凝可以提供“一段暫緩期”以延遲迫在眉睫的粘連性房角關閉。然而,此後如果不能進行PRP,房角光凝本身不能有效地防止房角粘連關閉的發生,反而時常加重炎症和加快房角新生血管形成的進展。
(4)藥物:在發生房角粘連關閉以前開角型青光眼是由於小梁網受到纖維血管膜的阻塞另外,糖尿病性視網膜病變或CRVO的患者可能同時存在著開角型青光眼。在房角開放的情況下常規的抗青光眼藥物還可有效地降低眼壓,然而除非予以PRP治療防止房角關閉,藥物治療的效果僅有暫時緩解的作用。在此期間,局部套用1%阿托品,2次/d以緩解眼部充血,糖皮質激素4次/d以緩解眼部炎症。
護理
新生血管性青光眼手術前的護理新生血管性青光眼手術的護理,術前心理護理:術前做好患者及家屬的解釋工作,使他們了解到該病的治療癒合過程,強調術後1周內可能出現的併發症及眼部不適,解除患者未來不必要的驚慌和疑慮,向其解釋術前使用降眼壓藥的必要性(可避免高眼壓狀態下手術引起暴發性前房、玻璃體腔出血和脈絡膜脫離的危險),以利於協調醫護人員的治療工作。
術前用藥:由於高眼壓下手術可引起以上眾多併發症,因此,術前加強降眼壓治療,盡最大可能降低眼壓同時聯合套用止血劑,是利於手術中操作,避免術中新生血管大出血,提高治癒率的關鍵所在。
新生血管性青光眼手術後的護理
新生血管性青光眼手術的護理,術後護理:加強術後1周內眼壓的密切觀察,注意觀察眼壓的波動,觀察角膜的變化,若出現一過性眼壓升高,應加用甘露醇等降眼壓藥對症處理,否則易引起角膜大泡,淺前房,前房出血等併發症。經加強降眼壓藥和對症處理後均能恢復正常。由於視網膜冷凝範圍廣泛,術後有眼球萎縮的可能,應加強隨訪,作好心理準備。
防治
新生血管性青光眼應如何防治1、術前充分控制全身病(高血壓、高血糖等),最大限度降低眼壓,在粘彈輔助下行小梁切除術。術後輔以5-FU尿嘧啶及按摩治療。
2、術前心理護理:術前做好患者及家屬的解釋工作,使他們了解到該病的治療癒合過程,強調術後1周內可能出現的併發症及眼部不適,解除患者未來不必要的驚慌和疑慮,向其解釋術前使用降眼壓苭的必要性(可避免高眼壓狀態下手術引起暴發性前房、玻璃體腔出血和脈絡膜脫離的危險),以利於協調醫護人員的治療工作。
3、術後護理:加強術後1周內眼壓的密切觀察,注意觀察眼壓的波動,觀察角膜的變化,若出現一過性眼壓升高,套用降眼壓苭對症處理,否則易引起角膜大泡,淺前房,前房出血等併發症。由於視網膜冷凝範圍廣泛,術後有眼球萎縮的可能,應加強隨訪,作好心理準備。
4、治療:常規濾過性手術常常失敗,術前全視網膜光凝術或冷凝術使新生血管退化,或術中術後套用抗代謝苭可提高手術成功率。房水引流裝置或閥門植入手術近年也用於治療新生血管性青光眼。若上述方法失敗,可考慮睫狀體破壞手術減少房屋水形成,降低眼壓以緩解症狀。視網膜缺氧和毛細血管無關注是虹膜新生血管形成的根源,一旦發現視網膜有缺血現象時應作廣泛視網膜光凝術,以預防虹膜新生血管的發生。
