鈾化合物
正文
鈾在不同情況下,可以生成U(Ⅲ)到U(Ⅵ)的各種鈾化合物,其中最穩定的是U(Ⅵ)的化合物,其次是U(Ⅳ)的化合物。主要化合物有:氧化物、氟化物、碳化物、矽化物。(見彩圖) 鈾化合物
鈾化合物二氧化鈾 UO2 二氧化鈾是深褐色粉末,密度為10.96克/厘米3,熔點2878°C。二氧化鈾具有半導體性質,電阻率隨溫度升高而下降。由於二氧化鈾具有受強輻照時不發生異性變形、在高溫下晶格結構不變、不揮發和不與水發生化學反應等特性,已廣泛用於製造反應堆燃料元件。
二氧化鈾在室溫下較穩定,但在空氣中加熱到200°C以上時會氧化成八氧化三鈾。二氧化鈾在高溫下能與氟化氫、氟化銨等作用生成四氟化鈾;溶解在過氧化氫的鹼溶液中,生成過氧鈾酸鹽。二氧化鈾可用金屬熱還原法還原成金屬鈾,還原劑常用鈣和鎂。
具有工業意義的二氧化鈾製備方法有兩種:
① 高溫還原法 三氧化鈾或八氧化三鈾在800~900°C與氫進行還原反應而得;或用氨作還原劑,在550°C也可製得二氧化鈾。
② 熱分解法 重鈾酸銨(NH4)2U2O7、三碳酸鈾醯銨(NH4)4【UO2(CO3)3】及草酸鈾醯UO2C2O4等鈾鹽,在隔絕空氣的情況下熱分解,生成三氧化鈾,分解產生的還原性氣體,可進一步將三氧化鈾還原成二氧化鈾。分解溫度約為450°C,還原溫度為650~800°C。
三氧化鈾 UO3 三氧化鈾隨著生成條件不同,具有無定形和多種晶體結構,至少有六種晶體異構體,並各具有不同的特性。其顏色通常為橙色,隨著晶體結構不同,顏色也不同。
幾乎所有的鈾醯鹽、鈾醯銨復鹽、鈾酸銨鹽在空氣中煅燒,都可生成三氧化鈾。工業上最常用的製備方法是三碳酸鈾醯銨、硝酸鈾醯 UO2(NO3)2、重鈾酸銨及鈾的水合過氧化物在400°C下熱分解。
八氧化三鈾U3O8 八氧化三鈾粉末的顏色隨製備的溫度不同而呈橄欖綠、墨綠,有時呈黑色。三氧化鈾在溫度大於500°C時,即可轉化為八氧化三鈾。重鈾酸銨在800°C熱分解也可得到八氧化三鈾。
氟化物 已發現的氟化物有UF3、U4F17、U2F9、UF5和 UF6。UF3不揮發。UF6是唯一穩定而易揮發的鈾化合物,在氣體擴散法分離鈾同位素的工藝中,占有重要地位。四氟化鈾則是生產金屬鈾工藝中的重要化合物。
四氟化鈾 UF4 四氟化鈾呈翠綠色,又稱綠鹽。四氟化鈾很穩定,在800°C才與氧反應,在250~400°C與氟反應生成六氟化鈾,在高溫下鹼金屬或鹼土金屬能將其還原成金屬鈾。四氟化鈾的製法有兩種:①濕法,在酸性溶液中,將六價鈾還原成四價,再與氫氟酸作用,生成四氟化鈾沉澱;在低於100°C時,在真空或惰性氣體氣氛中,用氫氟酸處理二氧化鈾,也可得四氟化鈾,稱為低溫氟化法。上述兩種方法所得的四氟化鈾都是水合物。②乾法,二氧化鈾和氟化氫在500~700°C可轉化為四氟化鈾;用氟里昂作氟化劑時,由於它具有還原性,也可以三氧化鈾為原料製得四氟化鈾:
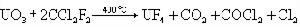
六氟化鈾 UF6 六氟化鈾是近於白色的粉末,容易揮發,已廣泛用於氣體擴散法分離鈾同位素。六氟化鈾不很活潑,在一般條件下不與氧、氫或氯反應;與氫在300°C以上才發生反應,反應緩慢;與水反應劇烈,生成UO2F2和HF,並釋放出大量熱。六氟化鈾是強氟化劑和氧化劑,它可使鎳合金腐蝕形成氟化膜而抗腐蝕,還可與多數有機物起氟化反應。製備六氟化鈾可用粉末狀四氟化鈾在約300°C與氟反應。
鈾酸鹽 單鈾酸鹽和多鈾酸鹽(又稱重鈾酸鹽)統稱鈾酸鹽。單鈾酸H2UO4形成的鹽具有M2UO4通式,M是一價金屬陽離子,鈾呈六價。單鈾酸在空氣中與鹼金屬氧化物、碳酸鹽或乙酸鹽一起加熱,可得單鈾酸鹽。多鈾酸鹽中重要的是重鈾酸銨,在鈾工業中是回收鈾的重要中間產品,俗稱黃餅。重鈾酸銨的製法,在工業上是將氨水加入到硫酸鈾醯或硝酸鈾醯溶液中,即可生成重鈾酸銨沉澱。重鈾酸銨的分子式過去一直認為是 (NH4)2U2O7,近來研究表明,它是三氧化鈾-氨-水的三元體系,隨沉澱生成的pH等條件的不同,三元組成也不同。
氫化鈾 UH3 氫化鈾是實驗室中由鈾製備大部分鈾化合物的中間產物。塊狀金屬鈾在 250°C時與氫迅速反應,生成黑色粉末狀氫化鈾,溫度高於400°C時,氫化鈾開始分解,可得高活性細粉末狀的鈾。這種鈾特別適於合成鈾的化合物,這是氫化鈾最主要的用途。
鈾的碳化物和矽化物 鈾的碳化物具有獨特的金屬傳導性,其熔點和硬度都很高,適於做核燃料。共有三種碳化鈾:UC、U2C3和UC2。UC和分散在石墨中的UC2,是高溫反應堆使用的核燃料形式。將氫化鈾分解而得的細鈾粉末與甲烷作用,在650°C生成UC,在950°C以上生成UC2。也可用碳還原氟化鈾,然後用真空電弧熔化及澆鑄而得UC。
鈾的矽化物主要是矽化鈾U3Si,它的密度高(15.6克/厘米3),寄生中子吸收截面低,同時對水有良好的耐腐蝕性。初步輻照試驗已證明,它是一個潛在的有用的核燃料。矽化鈾可用真空感應爐熔化鈾和矽製得,由於其組成範圍很窄,實際上很少得到單相合金,往往含有過量的鈾或U3Si2。
參考書目
E.H.P.科德芬克著,《核原料》編輯部《鈾化學》翻譯組譯:《鈾化學》,原子能出版社,北京,1977。(E.H.P.Cordfunke,The Chemistry of Uranium,Elsevier,Amsterdam,1969.)
