成份
 迭力
迭力主要組成成份為加巴噴丁
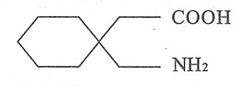
化學名稱:1-氨基甲基-環己乙酸。
化學結構式:
分子式:CHNO
分子量:171.24
性狀
本品為硬膠囊,內容物為白色或類白色粉狀粉末。
適應症
1.皰疹感染後神經痛:用於成人皰疹後神經痛的治療。
2.癲癇:用於成人和12歲以上兒童伴或不伴繼發性全身發作的部分性發作的輔助治療。也可用於3~12歲兒童的部分性發作的輔助治療。
規格
0.1g
用法用量
1. 皰疹感染後神經痛:第一天一次性服用加巴噴丁0.3g(3粒);第二天服用0.6g(6粒),分兩次服完;第三天服用0.9g(9粒),分三次服完。隨後,根據緩解疼痛的需要,可逐漸增加劑量至每天1.8g(18粒),分三次服用。國外臨床研究中,在每天1.8g(18粒)至3.6g(36粒)劑量範圍內其療效相當,每天超過1.8g(18粒)的劑量未顯示出更多益處。
2.癲癇:加巴噴丁可與其它抗癲癇藥物合用進行聯合治療。加巴噴丁的給藥途徑為口服,分次給藥(每日3次)。給藥方法從初始低劑量逐漸遞增至有效劑量。12歲以上患者:在給藥第一天可採用每日一次,每次0.3g(3粒);第二天為每日二次,每次0.3g(3粒),第三天為每日三次,每次0.3g(3粒),之後維持此劑量服用。據國外研究文獻報導,加巴噴丁的用藥劑量可增至每日1.8g(18粒),還有部分病人在用藥劑量達每日2.4g(24粒)仍能耐受。每天2.4g(24粒)以後劑量的安全性尚不確定。
3~12歲的兒科患者:開始劑量應該為10~15mg/kg/d,每日3次,在大約3天達到有效劑量。在5歲以上的患者加巴噴丁的有效劑量為25~35mg/kg/d,每日三次。3~4歲的兒科患者的有效劑量是40mg/kg/d,每日三次。如有必要,劑量可增為50mg/kg/d。長期臨床研究表明劑量增加到50mg/kg/d耐受性良好。
兩次服藥之間的間隔時間最長不能超過12小時。為減少頭暈、嗜睡等不良反應的發生,第一天用藥可在睡前服用。在加巴噴丁用藥過程中無需監測加巴噴丁的血藥濃度。而且,由於加巴噴丁在藥代動力學方面與其它常規抗癲癇藥物之間無明顯的相互作用,所以與此藥聯合治療不會改變這些常規抗癲癇藥物的血漿濃度。
在治療過程中,加巴噴丁的停藥或新治療方案的加入均需逐漸進行,時間最少為一周。
門診病人很難測量肌酐清除率。腎功能穩定的患者的肌酐清除率(CCr)可以根據Cockcroft和Gault的方程式合理的估計:
女性CCr =(0.85)(140-age)(weight)/[(72)(SCr)]
男性CCr =(140-age)(weight)/[(72)(SCr)]
其中年齡單位是年,體重單位是千克,SCr是血清肌酐,單位是mg/dL。
12歲以上腎功能損傷的或正在進行血液透析的患者推薦進行如下劑量調整:
表 依據患者腎功能情況進行的加巴噴丁用藥劑量調節
腎功能情況肌酐清除率(ml/min) 每日用藥總量(mg/day) 劑量方案(mg)
>60 1200 400T.I.D
30-60 600 300B.I.D
15-30 300 300Q.D
<15 150 300Q.D.O.Da
血液透析 -- 200-300b
a .隔日給藥。
b.未接受過加巴噴丁治療的患者的初始劑量為300~400mg,然後每透析4小時給加巴噴丁200~300mg。
12歲以下腎功能損傷患者尚未進行加巴噴丁使用的研究。
老年患者給藥劑量:
因為老年患者很可能腎功能下降,在劑量選擇上應該慎重,對這些患者應該根據肌酐清除率調整給藥劑量。
不良反應
1.皰疹感染後神經痛:
主要是眩暈,嗜睡,以及周圍性水腫,國外臨床試驗中發生的其他發生率高於1%並高於安慰劑對照組的不良事件包括:
全身:衰弱、感染、頭痛、意外外傷、腹痛。
消化系統:腹瀉、便秘、口乾、噁心、嘔吐、胃腸脹氣。
代謝和營養紊亂:體重增加、高血糖。
神經系統:共濟失調、思維異常、異常步態、不配合、感覺遲鈍。
呼吸系統:咽炎。
皮膚和附屬器官:皮疹。
特殊感官:弱視、復視、結膜炎、中耳炎。
2.癲癇:
最常見的不良事件是嗜睡、疲勞、眩暈、頭痛、噁心、嘔吐、體重增加、緊張、失眠、共濟失調、眼球震顫、感覺異常及厭食。
偶有出現衰弱、視覺障礙(弱視、復視)、震顫、關節脫臼、異常思維、健忘、口乾、抑鬱及情緒化傾向。
在臨床研究中以下情況偶有發生:消化不良、便秘、腹痛、尿失禁、食慾增加、鼻炎、咽炎、咳嗽、肌痛、背痛、面部和肢端或全身水腫、勃起功能下降、牙齒異常、牙齦炎、瘙癢症、白細胞減少症、骨折、血管擴張及高血壓。
另外,在12歲以下兒童的臨床試驗中觀察到攻擊性行為、情緒不穩定、多動(過多的運動,部分不能控制)、病毒感染、發熱。
加巴噴丁膠囊治療的患者中有發生出血性胰腺炎的報導。(見注意事項)
有個別病例服用加巴噴丁膠囊治療時發生過敏反應的報導(Stevens-Johnson綜合徵,多形性紅斑)。
實驗室檢查 臨床對照研究中,有16%的患者出現可能與臨床相關的血糖波動(<3.3mmol/L或者≥7.8mmol/L,正常值範圍3.5~5.5mmol/L)(見注意事項)。與其他抗癲癇藥同時使用,有肝功能試驗結果升高的報導。
禁忌
已知對該藥中任一成份過敏的人群、急性胰腺炎的患者禁服加巴噴丁膠囊。加巴噴丁膠囊對於原發性全身發作,如失神發作的患者無效。
注意事項
國外研究報導:
撤藥促使癲癇發作以及癲癇持續狀態
抗癲癇藥物不應該突然停止服用,因為可能增加癲癇發作的頻率。
在安慰劑對照研究中,加巴噴丁治療組患者癲癇持續狀態的發生率為0.6%(3/543),而安慰劑組為0.5%(2/378)。在所有研究(包括對照和非對照的)中用加巴噴丁治療的2074名患者中有31名(1.5%)出現癲癇持續狀態。其中14名患者在以前的治療中或服用其他藥物時未出現過癲癇持續狀態。由於沒有足夠的病史資料可以用,所以不能說加巴噴丁的治療是否與癲癇持續狀態的發生率比未用加巴噴丁治療者高或低有關係。
潛在的致癌作用:
動物致癌性臨床前研究發現雄性大鼠胰腺腺泡腺癌的發生率較高,該結果的臨床意義尚不清楚。加巴噴丁上市前臨床研究對於預測其誘發人體腫瘤的潛在可能性尚不明確。臨床研究包括2085名長期服藥的患者,在停止服用加巴噴丁後2年內其中10名患者出現了新的腫瘤(2例乳腺癌、3例腦癌、2例肺癌、1例腎上腺癌、1例非何杰金氏淋巴瘤和1例子宮內膜癌),11名患者出現腫瘤惡化(其中9例腦癌、1例乳腺癌、1例前列腺癌)。由於沒有未經過加巴噴丁治療的相似人群在腫瘤發生和復發率上的背景資料,因此不可能知道該研究中治療是否會影響發生率。
突然的和不能解釋的死亡:
在加巴噴丁上市前研究過程中,2203名治療者(其中2103名患者為長期治療)中有8人出現了突然的和不能解釋的死亡。
這些死亡者中的一些可解釋為癲癇發作導致的死亡,例如在晚上癲癇發作未被察覺。該情況的發生率為0.0038人/年。儘管該比率已經超過了相同年齡和性別健康者的比率,但卻在未服用加巴噴丁的癲癇者突然死亡發生率的範圍之內(從普通者的0.0005~與該試驗相似的臨床試驗人群的0.003,或0.0005~難治患者的0.005)。因此,結果是否可信取決於接受加巴噴丁治療的人群的可比性和統計的精確性。
特殊注意事項:
臨床對照研究中,16%的患者出現了可能有臨床意義的血糖波動(<3.3mmol/L或者≥7.8mmol/L,正常值範圍3.5~5.5mmol/L)。因此糖尿病患者需經常監測血糖,如必要,隨時調整降糖藥劑量。
腎功能不全的患者,服用本品必須減量(見用法用量)。
曾有服用本品發生出血性胰腺炎的報告。因此,如出現胰腺炎的臨床症狀(持續性腹痛、噁心、反覆嘔吐),應立即停用本品,並進行全面的體檢,臨床和實驗室檢查以期儘早診斷胰腺炎。
對慢性胰腺炎的患者,尚無充分的使用加巴噴丁的經驗,應由醫生決定加巴噴丁的使用。
同時使用嗎啡治療的病人加巴噴丁的血藥濃度可能會升高。應仔細觀察病人是否出現嗜睡等中樞神經系統抑制現象,應適當減少加巴噴丁或嗎啡的劑量(見藥物相互作用)。
對駕駛及機械操作的影響
本品作用於中樞神經系統,可引起鎮靜、眩暈或類似症狀。
因此,即便按照規定劑量服用本品,也可降低反應速度,使駕駛能力、操縱複雜機器的能力和在暴露環境中工作的能力受到損害,特別在治療初期、藥物加量、更換藥物時或者同時飲酒時。
孕婦及哺乳期婦女用藥
目前尚無孕期婦女使用本品的經驗,只有在充分評估利益/風險後,才可以使用本品。
本品在母乳中有分泌,因尚不能排除本品可致嬰兒嚴重不良事件的可能,所以哺乳期婦女在必須使用本品時,應停止哺乳或停止使用本品(考慮到對母親進行抗癲癇治療的必要性)。
兒童用藥
有關兒童的用法用量參見“用法用量”項下。
老年用藥
治療皰疹感染後神經痛同樣的劑量對75歲及以上患者的療效比年輕患者的療效好。但是也不能排除其他因素的影響。除周圍性水腫和共濟失調隨年齡增長而增加外,副作用的類型和發生率在各年齡組之間相似。
治療癲癇,65歲以上的人群,未進行過系統的研究。然而臨床觀察表明,該年齡段人群中不良事件的表現與較年輕者未見不同。
藥物相互作用
加巴噴丁很少代謝,也不干擾其他一般合用的抗癲癇藥物的代謝。
這部分描述的藥物相互作用數據是從相關健康成人和癲癇症患者的研究中得到的。
苯妥英:已服用苯妥英治療維持至少二個月的癲癇患者(N=8)進行加巴噴丁(每次0.4 g,每日三次)單次和多次給藥的研究,結果表明加巴噴丁對苯妥英的穩態血漿濃度沒有影響,並且苯妥英對加巴噴丁的藥代動力學也沒有影響。
卡巴咪嗪:服用加巴噴丁(每次0.4g,每日三次;N=12)不影響卡巴咪嗪和卡巴咪嗪10,11環氧化物的穩態血漿濃度。同樣地,服用卡巴咪嗪也不會改變加巴噴丁的藥代動力學。
丙戊酸:在同時服用加巴噴丁(每次0.4 g,每日三次;N=17)前和服用期間,丙戊酸平均穩態血漿濃度無差異,加巴噴丁的藥代動力學數據也不受丙戊酸的影響。
鎮靜安眠劑:不管是單獨服用還是聯合用藥,鎮靜安眠劑或加巴噴丁(每次0.3g,每日三次;N=12)穩態藥代動力學數據評估是一樣的。
萘普生:同時使用萘普生鈉膠囊(250mg)和Neurontin(125mg),加巴噴丁的吸收增加12%到15%。加巴噴丁對萘普生的藥代動力學參數沒有影響。兩者所給的劑量均低於各自的治療劑量。在推薦劑量範圍時其相互作用情況尚不清楚。
二氫可待因酮:合用加巴噴丁(0.125至0.5g;N=48)後二氫可待因酮(10mg,N=50)的Cmax和AUC降低,與所給二氫可待因酮的劑量呈依賴關係。合用加巴噴丁(0.125g)使二氫可待因酮(10mg,N=50)的Cmax和AUC降低約3%~4%,合用加巴噴丁(0.5g)使二氫可待因酮(10mg,N=50)的Cmax和AUC降低約21%~22%。這種相互作用機制尚不明確。二氫可待因酮能增加加巴噴丁的AUC約14%。其他劑量的相互作用情況還不明確。
嗎啡:據文獻報導,給予60mg控釋嗎啡膠囊2小時後再給予0.6g加巴噴丁膠囊(N=12),加巴噴丁的平均AUC比未用嗎啡時增加了44%(見警告)。服用加巴噴丁後嗎啡的藥代動力學參數沒有變化。與其它劑量的相互作用尚不清楚。
甲氰咪胍:服用甲氰咪胍每次0.3g,每日4次(N=12),加巴噴丁平均表觀口服清除率下降14%,肌酐清除率下降10%。因而,甲氰咪胍可能會改變加巴噴丁肌酐的腎排泄。由甲氰咪胍引起的加巴噴丁排泄的小幅度下降沒有重要的臨床意義。加巴噴丁對甲氰咪胍的影響沒有評價。
口服避孕藥:服用含有2.5mg乙酸炔諾酮和50μg乙炔基雌二醇的藥片後,不管是否同時服用加巴噴丁(每次0.4g,每日三次;N=13),乙酸炔諾酮和乙炔基雌二醇的AUC和半衰期是類似的。和加巴噴丁聯合給藥時,炔諾酮的Cmax升高13%;這一相互作用沒有重要的臨床意義。
抗酸劑(氫氧化鋁):氫氧化鋁降低加巴噴丁的生物利用度大約20%。服用氫氧化鋁後2小時服用加巴噴丁,生物利用度下降大約5%。因此,建議加巴噴丁應在氫氧化鋁服用後至少2小時服用。
丙磺舒(羧苯磺丙胺)的作用:丙磺舒是一種腎小管分泌阻滯劑。將加巴噴丁結合或不結合丙磺舒試驗的藥代物動力學參數進行比較,結果證實加巴噴丁不能流經被丙磺舒阻滯的腎小管路徑。
藥物過量
據報導,在服用加巴噴丁過量達49克的患者中,可出現復視、口齒不清、嗜睡、淡漠和腹瀉。所有患者經搶救後康復。
加巴噴丁可通過血液透析清除。儘管在本品過量的患者尚未進行血液透析,但在一些腎功能損害患者體內可被觀察到其清除過程。
藥理毒理
藥理作用
加巴噴丁抗驚厥作用的機制尚不明確,但動物試驗提示,與其他上市的抗驚厥藥物相似,加巴噴丁可抑制癲癇發作。小鼠和大鼠最大電休克試驗、苯四唑癲癇發作試驗以及其他動物試驗(如遺傳性癲癇模型等)結果提示,加巴噴丁具有抗癲癇作用,但這些癲癇模型與人體的相關性尚不清楚。
加巴噴丁在結構上與神經遞質GABA相關,但不與GABA受體產生相互作用,它既不能代謝轉化為GABA或GABA激動劑,也不是GABA攝取或降解的抑制劑。放射性配體結合試驗發現,加巴噴丁濃度達到100μm時,對許多常見受體位點無親和力,包括苯二氮卓受體、谷氨酸受體、NMD受體、quisqualate受體、海人草酸受體、番木鱉鹼-不敏感性或-敏感性的氨基乙酸受體、α1、α2或β受體、腺苷A1或A2受體、M或N受體、多巴胺D1或D2受體、H1受體、5-羥色胺S1或S2受體、阿片μ,δ或k受體、尼群地平或地爾硫卓標記的電壓敏感鈣通道位點、蛙毒素A 20-α-苯甲酸鹽標記的電壓敏感的鈉通道位點。由於在評價藥物對NMDA受體作用的幾個常用試驗所得出的結果是相反,故目前尚無任何關於加巴噴丁對NMDA受體作用的統一認識。
體外研究顯示加巴噴丁在大鼠腦內的結合位點分布於新皮層和海馬,其高親和力的結合蛋白被證實為電壓激活鈣通道的輔助亞單位,相關功能尚未闡明。
毒理研究
遺傳毒性
加巴噴丁Ames試驗、CHL HGPRT突變試驗、CHL染色體畸變試驗、中國倉鼠骨髓染色體畸變試驗和微核試驗、小鼠微核試驗、大鼠肝細胞程式外DNA合成試驗(UDS)結果均為陰性。
生殖毒性
一般生殖毒性:大鼠經口給予加巴噴丁(500,1000和2000mg/kg/天)後,所有胎仔均受影響。致畸敏感期毒性:妊娠小鼠經口給予加巴噴丁1000或3000 mg/kg/天,出現胚胎毒性,頭骨、椎骨、前肢和後肢骨骼骨化延遲,無毒劑量為500 mg/kg/天。圍產期毒性:家兔給予加巴噴丁60,300和1500mg/kg/天,植入後胎仔丟失率增加。
另外,在大鼠一般生殖毒性試驗(經口給藥2000 mg/kg)、致畸敏感期毒性試驗(1500 mg/kg)、圍產期毒性試驗(500,1000和2000 mg/kg)中,大鼠輸尿管積水和/或腎盂積水的發生率升高。按體表面積比推算,小鼠、大鼠和家兔給予加巴噴丁的劑量分別為人用劑量的4、5、8倍時,未見畸胎髮生率增加。
致癌性
小鼠和大鼠分別經口給予加巴噴丁200、600、2000 mg/kg/天和250、1000、2000 mg/kg/天,連續2年。結果發現高劑量組雄性動物胰腺腺泡細胞瘤和胰腺腺泡細胞癌發生率明顯升高,但未影響動物存活,也未出現轉移和浸潤。研究提示,加巴噴丁在體外可促進大鼠胰腺腺泡細胞的DNA合成,因此,其可能為一種增強有絲分裂的促癌劑。但加巴噴丁對其他細胞和種屬(包括人)促細胞增殖的作用尚不明確。
臨床研究顯示,2085名長期服藥的患者(大於12歲),在停止服用加巴噴丁後2年內有10名患者出現了新的腫瘤(2例乳腺癌、3例腦癌、2例肺癌、1例腎上腺癌、1例非何杰金氏淋巴瘤和1例子宮內膜癌),11名患者出現腫瘤惡化(其中9例腦癌、1例乳腺癌、1例前列腺癌)。由於沒有未經過加巴噴丁治療的相似人群在腫瘤發生和復發率上的背景資料,因此不確定以上腫瘤的發生或惡化與治療有關。
藥代動力學
據文獻報導,服用加巴噴丁後所有的藥理學作用都來自於其母體化合物的活性,加巴噴丁在人體的代謝是不明顯的。
口服生物利用度:加巴噴丁的生物利用度與劑量不成比例,當劑量增加時,生物利用度下降。在每日分三次給予劑量為900、1200、2400、3600和4800 mg加巴噴丁時,其生物利用度分別約為60%、47%、34%、33%和27%。食物對加巴噴丁的吸收速度和程度只有輕微的影響(AUC和Cmax有14%的增加)。
分布: 加巴噴丁在循環中大部分不與血漿蛋白結合(蛋白結合率<3%)。靜脈注射加巴噴丁150 mg後的表觀分布容積為58±6L(平均值±標準差)。癲癇患者腦脊液中加巴噴丁穩態谷濃度(Cmin)大約為相應血漿濃度的20%。
消除:加巴噴丁主要以原形通過腎臟排泄從全身循環系統中消除,在人體內的代謝不明顯。加巴噴丁的消除半衰期是5~7小時,並且不隨劑量或多次給藥而改變。加巴噴丁的消除速率常數、血漿清除和腎清除與肌酐清除率直接成正比(見特殊人群中腎臟功能不全的患者)。在老年患者和腎臟功能損傷的患者,加巴噴丁血漿清除率下降。加巴噴丁可以通過血液透析從血漿中清除。
特殊人群:腎功能不全的成年患者:腎功能不全(平均肌酐清除率為13~114 mL/min)的受試者(N=60)單劑量口服加巴噴丁400mg,加巴噴丁的平均半衰期為6.5小時(肌酐清除率>60 mL/min的患者)~52小時(肌酐清除率<30 mL/min的患者),加巴噴丁的腎臟清除率為90 mL/min(肌酐清除率>60 mL/min的患者)~10 mL/min(肌酐清除率<30 mL/min的患者)。平均血漿清除率從大約190 mL/min下降到20 mL/min。
腎功能損傷的患者或進行血液透析的患者需進行劑量調整。
腎功能不全的兒科患者尚未進行研究。
血液透析:在無尿症的患者的研究中(N=11),加巴噴丁在未透析時的表觀消除半衰期大約為132個小時;一周透析三次(每次持續4小時),加巴噴丁的表觀消除半衰期從132小時減少到51小時,減少了大約60%。由此可見,血液透析對無尿症患者體內加巴噴丁的消除影響很大。
血液透析的患者需進行劑量調整。
肝疾患者:由於加巴噴丁不代謝,所以未對肝臟損傷的患者進行研究。
年齡:在20~80歲的受試者中進行年齡影響的研究。加巴噴丁的表觀口服清除率(CL/F)隨著年齡增加而下降了,從在30歲以下的人中大約225mL/min到70歲以上的人中大約125mL/min。腎臟清除率(CLr)和根據體表調整過的腎臟清除率也隨著年齡的增加而降低;然而,加巴噴丁的腎臟清除率隨著年齡下降在很大程度上能解釋為腎臟功能的下降。有與年齡相關的腎臟功能疾病患者中要求減少加巴噴丁劑量。
兒科:加巴噴丁的藥物代謝動力學在48名年齡在1個月到12歲的兒科的受試者中進行,劑量約為10mg/kg。血漿濃度峰值在各個年齡組是相似的,達峰時間約為給藥後2~3小時。通常,兒科的受試者年齡在1個月到小於5歲之間比5歲和更大的患兒中觀察到的暴露量約低30%(AUC)。因此,標準化每個體重的口服清除率在越小的兒童中越高。加巴噴丁的表觀口服清除率直接與肌酐清除率成比例。加巴噴丁消除半衰期平均為4.7個小時並且在整個年齡組的研究結果基本相似。
據國外文獻報告,在253名年齡在1個月到13歲的兒科的患者中進行了一個總體的藥物動力學分析。患者接受10到65 mg/kg/天,每日三次給予。表觀口服清除率(CL/F)直接與肌酐清除率成比例,這個關係在單劑量和在穩態時是相似的。當按公斤體重標化後,在小於5歲的兒童中可觀察到比5歲或更大的兒童中更高的口服清除率值。在小於1歲的嬰兒中的清除率是非常易變的。在5歲和更大的兒科患者中觀察到的標準的口服清除率和在成人中給予單個劑量後的值相一致。標準化每公斤體重的口服分布體積在整個年齡範圍是不變的。
藥物代謝動力學資料表明在3~4歲癲癇症的兒科患者中有效的每日劑量應該是40 mg/kg/天,其達到的平均血漿濃度,與那些5歲或更大的患者接受加巴噴丁30 mg/kg/天所達到的血漿濃度是相似的。
性別:雖然沒有進行正式的研究來對比加巴噴丁在男性和女性中的藥物代謝動力學,現有的資料顯示男性和女性的藥物代謝動力學參數是相似的並且沒有明顯的性別差異。
種族:種族的藥物代謝動力學差異還沒有研究。由於加巴噴丁主要是腎臟排泄的,並且肌酐清除率沒有大的種族差異,因此認為種族的藥物代謝動力學沒有差異。
貯藏
密封保存,避免高溫。
包裝
鋁塑泡罩板,4×12粒/板/盒。
有效期
24個月
執行標準
YBH04852004
批准文號
國藥準字H20040527
生產企業
江蘇恩華藥業股份有限公司
核准日期
2006年07月24日
修訂日期
2008年05月22日
