原理
親電取代反應主要發生在芳香體系或富電子的不飽和碳上,就本質而言均是較強親電基團對負電子體系進攻,取代較弱親電基團。但對於芳香體系和脂肪體系,由於具體環境不同,其反應歷程亦有所不同,現分述如下。芳香親電取代(aromatic electrophilic substitution)是芳香體系最重要的有機反應之一,常用於向芳香環系引入官能團,因此研究時間較長,在機理方面已基本達成一致。
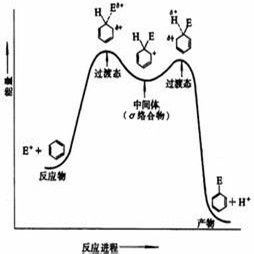
芳香系親電取代機理一致,右圖給出了苯環的一般歷程,親電基團首先與芳香環電子結合形成π絡合物,之後再過渡到一個中間體σ絡合物。最後當新基團親電能力強於氫離子時,就會從芳香環上脫去氫離子完成反應。
脂肪體系親電取代反應與芳香體系有較大不同,其機理更類似於脂肪族的親核取代反應,一般可分為SE1和SE2,這與脂肪族親核取代機理中的SN1和SN2類似。而卡賓插入反應這樣先插入,再消去的歷程就稱為SE2。
主要反應
對於親電取代反應,其最為主要的反應類型均在芳香體系中產生,所以這裡僅僅對芳香親電取代進行一定的舉例介紹。
硝化反應
 醯基化及還原
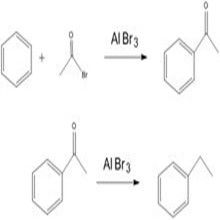
醯基化及還原該反應由CharlesFriedel和JamesCrafts發現於1877年,當時採用三氯化鋁等路易斯酸為催化劑,原來特指苯上的烷基化或醯基化。但經過發展,現在泛指芳香體系中由鹵代烷或醯鹵為反應物在路易斯酸催化下進行的親電取代反應。
傅克反應就反應物的不同可分為傅克-烷基化反應和傅克-醯基化反應,兩者均是向芳環引入碳鏈的方法。其中烷基化反應由於涉及碳正離子過程,除叔碳外均有嚴重的重排反應,往往得不到純淨的目標產物,所以常使用先醯基化再還原的過程。
鹵化反應
有機化合物分子中的氫被鹵素取代的反應稱為鹵化反應,機理上也是親電取代反應。該反應在藥物修飾上比較常見,此外也是製備芳香系格式試劑的前驅反應。
磺化反應
有機化合物分子中的氫被磺酸基取代的反應稱為磺化反應。苯及其衍生物幾乎都可以進行這一反應,其機理也屬於親電取代反應。但是與上述三個反應不同,磺化反應在芳香體系中有比較強的可逆性,一般濃硫酸中發生正反應產生磺酸基;而在稀硫酸中發生逆反應脫去磺酸基,因此常用磺酸基作保護基使用。此外,在早期的化工過程中,該反應也是製造苯酚的前驅反應。
定位規則
對於芳香體系,特別是含有苯環的化合物在進行親電取代反應時,在已有取代基的情況下,新上基團的位置有很強的選擇性,由這一選擇性總結的經驗規則就叫做定位規則。
定位規則主要是基於已有取代基對苯環π電子云密度的影響來考慮的,簡單來說即是將取代基分為鄰對位取代基(orthe-para diecting group)和間位取代基(meta directing group),前者使新進入基團進入苯環鄰位或者對位,而後者使新進入基團進入苯環間位。