概念
根據抗體產生過程中親合力的變化,通過測定IgG抗體親合力指數(avid ity index,AI),可用於鑑別病原體原發(近期)感染和既往感染。IgG抗體產生早期(即感染早期),AI相對較低,隨著時間的延長,AI逐漸升高。因此,有研究提出AI<30%為低親合力抗體,提示原發感染;AI>50%為高親合力抗體,表明既往感染或再發感染;AI介於30%~50%為中等親合力抗體。
測定抗體親合力鑑別原發感染和再激活感染
研究背景
抗體AI已廣泛套用於鑑別人巨細胞病毒(human cytomegalovirus,HC-MV)、EBV、弓形蟲和肺炎支原體等的原發感染和再感染或再激活感染。檢測單份標本的抗HCMV-IgG AI判斷HCMV近期原發感染具有較高的靈敏度和特異性。在ELISA基礎上,用溫育法 測定抗HCMV-IgG AI,研究抗體濃度對AI測定的影響,通過AI判斷HCMV原發感染和再次或再激活感染。
結果討論
抗HCMV-IgG濃度過高時包被抗原相對不足,存在過剩的IgG,此時由於高親合力的IgG在尿素的作用下仍然能與包被抗原結合,而非變性孔IgG與包被抗原的結合已經飽和,所測得的A值相對恆定,因此影響AI測定,得出較高的AI值。這與K li-mashevskaya等的報導一致。而Dangel等卻認為高濃度的IgG會引起錯誤的低AI值結果,可能與實驗方法及試劑的不同有關。而在檢測血漿抗HC-MV-IgG濃度約100 IU/mL的AI時,AI值隨稀釋倍數不同出現一定的波動,但不影響結果的判斷。
尿素處理時間長短可影響AI的高低,尤其是低AI的標本會因為變性時間不足而得出明顯高於真實的AI值。國內的研究在檢測抗HCMV-IgG AI時多採用簡化的洗脫法,認為取50%為判斷近期原發感染的界值。經比較2種方法分別檢測8份血漿的結果,溫育法檢測的AI低於洗脫法,但無顯著性差異,說明溫育法(變性孔尿素終濃度4mol/L)與該洗脫法具有相近的使低親合力抗體變性的能力。由此本研究採用Hedman對於AI的解釋,以AI<30%判斷近期原發感染,以AI>30%排除近期原發感染,判斷為既往感染或再發感染。
抗HCMV-IgM抗體不僅在HCMV近期原發感染時出現,再發感染也可產生。特異性IgM用於判斷HCMV的活動性感染,結合抗HCMV-IgM和AI能夠有效判斷感染的時間。在50份血漿中,AI<30%有15例,判斷為近期原發感染,其中5例檢出抗HCMV-IgM,其餘10例可能由於抗HCMV-IgM轉陰未能檢出;AI>50%有16例,判斷其感染時間大於3個月,其中5例抗HCMV-IgM陽性判斷為再發感染。
Lutz等觀察到HCMV原發感染的免疫抑制患者抗體成熟明顯延遲,IgG由低親合力到高親合力需一年以上,而正常人為2~6月。本研究中觀察了8例免疫抑制患者血漿抗HCMV-IgG AI的變化情況,其中6例AI升高不明顯。所以這類患者在利用AI判斷感染時間應考慮這一特點,對於免疫抑制患者的AI變化需要深入的研究。
溫育法測定抗HCMV-IgG AI能夠區分HCMV的原發感染和再次或再激活感染,結合抗HCMV-IgM可以判斷感染的情況及時間。這對於孕婦HCMV感染的診斷具有重要的意義。藉助AI判斷孕婦HCMV的感染類型,可以決定是否進一步行羊膜腔穿刺等侵入性檢查診斷宮內HCMV感染。免疫抑制患者存在抗體的產生和成熟延緩,HCMV的核酸的檢測可作為血清學診斷的補充。
神經生長因子低親合力受體在肝細胞的表達
神經生長因子受體( NGFR)由兩個亞基組成即神經生長因子低親合力受體-P75( low-affinity nerve growth factor receptor,P75) 和神經生長因子高親合力受體-酪氨酸激酶A( tyrosine kinase A,TrkA)。Trim等認為,人與大鼠(hepatic stellate cells,HSCs膜特異性表達P75,P75能誘導HSCs調亡。國內尚無此方面的報導 。相關研究採用大鼠離體培養的活化HSCs和肝纖維化患者及大鼠的HSCs,觀察P75的表達分布,旨在探討肝纖維化的發病機制,為神經生長因子(nerve hepatic stnellate cells,growth factor,NGF)用於肝纖維化的臨床治療打下實驗基礎。
1951年,Levi-Montalcini首次在小鼠肉瘤細胞中發現了對神經系統發育、分化及維持神經元特殊功能有重要作用的NGF,以後的研究發現,NGF在機體組織器官中分布十分廣泛,許多細胞株包括HSCs均有存在。研究表明,NGFR通過P75和TrkA發揮作用。TrkA是NGF的功能性受體,傳遞信號,促進神經細胞再生,而P75的功能尚不明晰。1996年,國外學者報導,P75在完全沒有TrkA 的參與下,可獨立誘導細胞凋亡。因此,研究P75在HSCs的表達分布,有助於探究 P75 的功能及作用機理。
HSCs是肝纖維化形成過程中合成細胞外基質的最主要細胞,肝纖維化恢復期,凋亡的HSCs明顯增多。實驗證明,在CCl造成大鼠肝纖維化模型後的自動恢復過程中,HSCs凋亡是中心事件。所以,抑制HSCs增殖、誘導其凋亡是抗肝纖維化的重要策略。Takahashi等報導,NGFR是細胞膜受體,存在於多種細胞表面。Trim等報導,靜止狀態離體培養的大鼠HSCs不表達P75,而活化的HSCs表達P75;在人和大鼠的肝內,HSCs表達P75,肝細
胞不表達P75,P75應答配體NGF的刺激進入凋亡;將100μg/LNGF與HSCs共同培養24h後,HSCs凋亡數量明顯增加,且呈劑量依賴關係,指出NGF對體外培養的HSCs凋亡有誘導作用,其作用機制可能包括NGF及P75的作用。
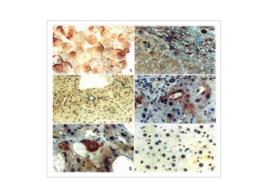
實驗觀察到,肝纖維化患者和大鼠HSCs表達P75,與Trim的結果一致;P75在HSCs膜表達,呈線狀或顆粒狀分布,與Takahashi的結果一致;同時,實驗發現,肝纖維化患者和大鼠的肝細胞也有P75表達,這與Trim 報導的HSCs特異性表達P75不符,有待於進一步探討。
Rabizadeh等認為,P75會誘導HSCs凋亡的機理是因為NGF通過與細胞表面受體P75結合而誘導神經細胞的凋亡。因此推測,其作用機理可能是NGF與P75結合在HSCs膜上,可促進P75誘導HSCs的活性,促進HSCs凋亡,不利於肝纖維化的進展。
P75在HSCs的發現為抗肝纖維化藥物的研發提供了一個新的靶點。推測,當肝纖維化發生時,給予高濃度的NGF可能獲得較好的療效;同時,如果能找到某種上調活化HSCs表達P75的藥物,將對阻抑肝纖維化的進程起到積極作用。