成份
本品主要成份為更昔洛韋,其化學名稱為9-(1,3-二羥基-2-丙氧甲基)-鳥嘌呤。
性狀
本品為無色澄明液體。
適應症
本品僅用於:
1、預防可能發生於有巨細胞病毒感染風險的器官移植受者的巨細胞病毒病。
2、治療免疫功能缺陷患者(包括愛滋病患者)發生的巨細胞病毒性視網膜炎。
規格
(1)100ml:更昔洛韋50mg與葡萄糖5g
(2)250ml:更昔洛韋0.25g與葡萄糖12.5g
用法用量
 更昔洛韋葡萄糖注射液
更昔洛韋葡萄糖注射液 更昔洛韋葡萄糖注射液
更昔洛韋葡萄糖注射液(一)對於腎功能正常者:
1、治療CMV視網膜炎的標準劑量:
1)初始劑量:5mg/kg,每12小時一次,恆定速率靜脈滴注,每次滴注時間1小時以上,連用14~21天。
2)維持劑量:5mg/kg,每天1次,7天/周,恆定速率靜脈滴注,每次滴注時間1小時以上;或者6mg/kg,每天1次,5天/周,恆定速率靜脈滴注,每次滴注時間1小時以上。
2、預防器官移植受者的巨細胞病毒病:
1)初始劑量:5mg/kg,每12小時一次,恆定速率靜脈滴注,每次滴注時間1小時以上,連用7~14天。
2)維持劑量:5mg/kg,每天1次,7天/周,恆定速率靜脈滴注,每次滴注時間1小時以上;或者6mg/kg,每天1次,5天/周,恆定速率靜脈滴注,每次滴注時間1小時以上。
(二)特殊用藥指導
1、腎功能不全者:
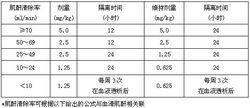
對於腎功能不全患者,參照下表中推薦劑量和用藥間隔進行調整:
接受血液透析的患者劑量不可超過1.25mg/kg,每周3次,在血液透析後進行。本品需在血液透析完成後短時間內給藥,因為血液透析可減少大約50%的血漿濃度。
由於對腎功能不全病人推薦使用調整劑量,其血清肌酐或肌酐清除率水平應密切監控。
2、患者的監測:由於接受更昔洛韋的患者發生粒細胞減少症,貧血和血小板減少症的頻率高(見不良事件),建議經常進行全血細胞計數和血小板計數,特別是以前使用更昔洛韋或其他核苷類拮抗劑出現血細胞減少者,或治療開始時中性粒細胞計數小於1000個/μL者。
3、減量:腎功能不全患者需減低劑量。對於出現中性粒細胞減少、貧血和/或血小板減少的患者考慮減量(見不良事件)。更昔洛韋不可用於嚴重中性粒細胞減少(ANC小於500個/μL)或嚴重血小板減少(血小板小於25000個/μL)的患者。
註:本品僅供靜脈滴注給藥,不可肌肉注射。本品使用時不可靜脈快速注射或靜脈推注,不可超過推薦劑量,不可超過推薦的滴注速率。
禁忌
對更昔洛韋或阿昔洛韋過敏者禁用。
注意事項
警告:如果絕對中性粒細胞計數少於500個細胞/μL或血小板計數少於25,000個細胞/μL不能使用本品。
1、患者須知:
所有患者需被告知更昔洛韋的主要毒性為粒細胞減少症(中性粒細胞減少症),貧血和血小板減少症,並易引起出血和感染,必要時需進行劑量調整,包括停藥。應強調在治療中密切接受血細胞計數檢查的重要性。需通知患者更昔洛韋與測定血清肌酐水平有關。應警告患者更昔洛韋在動物引起精子生成減少並可能對人類造成生殖力損害。應警告可能妊娠的女性更昔洛韋可能造成胎兒損害,不建議妊娠使用。建議可能妊娠的女性在使用本品治療時需採取有效的避孕措施。建議男性在本品治療期間和治療後至少90天應避孕。應警告患者更昔洛韋在動物可以引起腫瘤。雖然沒有對人類進行相關研究的資料,更昔洛韋應被認為是一種潛在的致癌物。
所有HIV陽性患者:這些患者可能正在接受齊多夫定(Zidovudine)治療。需警告患者同時使用更昔洛韋和齊多夫定在一些患者不耐受,可能引起嚴重的粒細胞減少症(中性粒細胞減少症)。AIDS患者可能正在接受去羥肌苷(Didanosine)治療。需警告患者同時使用更昔洛韋和去羥肌苷可能引起血清去羥肌苷濃度顯著提高。
HIV陽性伴CMV視網膜炎患者:更昔洛韋不是CMV視網膜炎的治癒藥物,免疫損傷的患者在治療中和治療後可能持續經歷視網膜炎的發展過程。
需建議患者在接受更昔洛韋治療期間最少4至6周進行1次眼科隨訪檢查。有些患者可能需要更頻繁的隨訪。
器官移植受體:應警告器官移植受體,在對照臨床試驗中,接受本品的器官移植受體腎損害的發生率高,特別是合併使用腎毒性藥物者,如環孢素和兩性黴素B。雖然此毒性反應的特異性機制尚未確定,且大多數病例為可逆反應,但在同一試驗中接受本品的患者比接受安慰劑的患者腎損害的發生率高,提示本品起重要作用。
2、實驗室檢查
由於接受本品的患者出現中性粒細胞減少症、貧血和血小板減少症的頻率高,推薦定期進行全血細胞計數和血小板計數檢查。特別是以往使用更昔洛韋或其他核苷類拮抗劑出現白細胞減少或在治療開始時中性粒細胞計數低於1000個/μL者,應每天進行血細胞計數檢查。如中性粒細胞計數在500/μL以下或血小板計數在25,000/μL以下時應當暫停用藥。直至中性粒細胞增至750/μL以上時方可重新給藥。在評價更昔洛韋的臨床試驗中均可觀察到血清肌酐水平增加。在腎功能不全患者需密切監測血清肌酐和肌酐清除率以進行必要的劑量調整。
3、更昔洛韋不能治癒巨細胞病毒感染,因此用於愛滋病患者合併巨細胞病毒感染時往往需長期維持用藥,防止復發。
孕婦及哺乳期婦女用藥
更昔洛韋在人類用藥的推薦劑量水平可能引起致畸和胚胎毒性。沒有對妊娠婦女的足夠的、良好對照研究。故僅在充分顯示治療益處超過對胎兒的潛在危害的情況下,方可在妊娠期使用本品。
對更昔洛韋是否分泌入人類乳汁的情況未知。由於許多藥物可分泌入人乳,且更昔洛韋治療可引起動物致癌和致畸效果,考慮更昔洛韋對乳兒可能有嚴重的不良反應,因此,哺乳期婦女慎用。如哺乳期必須接受本品,則應在治療期停止授乳。使用最後一劑本品後至哺乳前最少的安全間隔尚未知。
兒童用藥
本品對兒科患者的療效和安全性尚未確定,由於潛在長期的致癌性和生殖毒性,故在兒科人群使用本品應特別謹慎。僅在仔細評價且認為潛在的獲益超過風險時方可給兒科患者用藥。
接受本品治療的所報導的兒童不良事件與成人報導的事件相似。粒細胞減少症(17%)和血小板減少症(10%)是最常報導的不良事件。
老年用藥
本品在老年患者的藥代動力學資料尚未確立。由於老年個體通常腎小球濾過率低,故在本品治療前和治療中應特別注意評價腎功能。
對本品的臨床研究中未包括足夠的65歲或以上患者,不能確定他們的反應是否與年輕個體不同。其他的臨床實踐亦沒有確定老年患者和年輕患者反應差異。一般來說,由於老年患者肝、腎或心臟功能降低,以及合併其它疾病或藥物治療,所以對老年患者選擇劑量時應特別小心,通常從劑量範圍的最低點開始。
藥物相互作用
去羥肌苷:在更昔洛韋口服製劑用藥前2小時或同時服用去羥肌苷,穩態去羥肌苷AUC0-12將增加111±114%(範圍:10%至493%)(n=12)。更昔洛韋口服前2小時服用去羥肌苷,更昔洛韋的穩態AUC下降21±17%(範圍:-44%至5%),但兩藥同時使用時更昔洛韋的AUC不受影響(n=12)。兩種藥物腎清除率均沒有顯著改變。
當標準更昔洛韋靜脈初始劑量(5mg/kg靜脈滴注維持1小時,每12小時1次)與去羥肌苷200mg口服,每12小時1次聯合使用,穩態去羥肌苷AUC0-12增加70±40%(範圍:3%至121%,n=11),C增加49±48%(範圍:-28%至125%)。在另一試驗中,當標準更昔洛韋靜脈維持量(5mg/kg靜脈滴注維持1小時,每24小時1次)與去羥肌苷200mg口服,每12小時1次聯合使用,在去羥肌苷的第一個劑量間隔,去羥肌苷AUC0-12增加50±26%(範圍:22%至100%,n=11),C增加36±36%(範圍:-27%至94%)。在不與更昔洛韋聯合使用時的劑量間隔內,去羥肌苷的血漿濃度(AUC12-24)不變。更昔洛韋的藥代動力學參數不受去羥肌苷的影響。各試驗中兩藥的腎清除率均無顯著改變。
齊多夫定:當更昔洛韋口服製劑劑量為1000mg每8小時1次,合併齊多夫定100mg每4小時1次時,平均穩態更昔洛韋AUC0-8下降17±25%(範圍:-52%至23%)(n=12)。更昔洛韋存在時,齊多夫定穩態AUC0-4,增加19±27%(範圍:-11%至74%)。由於齊多夫定和更昔洛韋均有可能引起中性粒細胞減少和貧血,一些患者可能不能耐受兩種藥物在全量聯合使用。
丙磺舒:當更昔洛韋口服製劑劑量1000mg每8小時1次,合併丙橫舒500mg,每6小時1次時,平均穩態更昔洛韋AUC0-8增加53±91%(範圍:-14%至299%)(n=10)。更昔洛韋腎清除率降低22±20%(-54%至-4%),這種相互作用與競爭腎小管分泌有關。
亞胺培南-西司他丁(Imipenem-cilastatin):同時接受更昔洛韋和亞胺培南-西司他丁的患者有出現無顯著特點的癲癇發作的報導,故除非潛在獲益超過風險,這些藥物不可同時使用。
其它藥物:抑制快速分裂細胞群,如骨髓,精原細胞和皮膚生髮層和胃腸道黏膜細胞複製的藥物與更昔洛韋合併使用均可增加毒性。因此,此類藥物如氨苯碸,戊烷脒,5-氟胞嘧啶,長春新鹼,長春鹼,阿黴素,兩性黴素B,甲氧苄氨嘧啶/磺胺甲基異噁唑複合物或其他核苷拮抗劑僅可在潛在獲益超過風險時與更昔洛韋同時使用。
沒有更昔洛韋與器官移植受體常用藥物相互作用的正式研究。更昔洛韋與環孢素或兩性黴素B等已知潛在腎毒性藥物同時使用可增加血清肌酐的水平。在一項回顧性分析中,91例異位肝移植患者接受更昔洛韋(5mg/kg靜脈滴注維持1小時,每12小時1次)和口服環孢黴素(治療劑量),沒有觀察到對環孢黴素全血濃度的影響。
藥物過量
靜脈注射本品過量可致包括不可逆轉的各類血小板減少症,持續性骨髓抑制,可逆性中性粒細胞減少或粒細胞減少症,肝、腎功能損害和癲癇。對於用藥過量患者,透析能降低藥物血漿濃度。
藥理毒理
核苷類抗病毒藥。本品進入細胞後迅速被磷酸化為單磷酸化合物,然後經細胞激酶的作用成為三磷酸化合物,在已感染巨細胞病毒的細胞內其磷酸化較正常細胞更快。更昔洛韋可競爭性抑制DNA多聚酶,並摻入病毒及宿主細胞的DNA中,從而抑制DNA合成。本品對病毒DNA多聚酶的抑制作用較宿主細胞多聚酶為強。動物實驗中本品有致畸、致癌、免疫抑制作用和生殖系統毒性。
藥代動力學
本品在體內廣泛分布於各種組織中,並可透過胎盤。腦脊液內濃度為同期血藥濃度的24%~70%;本品亦可進入眼內組織。分布容積(Vd)為0.74±0.15L/kg(n=98)。蛋白結合率低,為1%~2%,在體內不代謝。成人靜脈滴注5mg/kg(1小時內)後的血藥峰濃度(Cmax)範圍在8.27±1.02(n=16)ug/ml和9.0±1.4ug/ml(n=16),血消除半衰期(t1/2β)為3.5±0.9小時(n=98),腎功能減退者可延長至9~30小時。本品主要以原形經腎排出。
貯藏
密閉,在涼暗處保存。
包裝
玻璃輸液瓶。
有效期
暫定18個月。
