周期律
periodic law
正文
元素的性質隨著元素的原子序數(即原子核外電子數或核電荷數)的增加呈周期性變化的規律。周期律的發現是化學系統化過程中的一個重要里程碑。簡史 1829年德國化學家J.W.德貝賴納研究了當時已知的54種元素的原子量和化學性質間的關係,發現幾個“三元素組”。如鋰、鈉、鉀、氯、溴、碘、……,同組元素性質相似,中間那個元素的性質介於前後兩個元素之間,其原子量為前後兩種元素原子量的平均值。19世紀中葉英國化學家J.H.格拉德斯通、W.奧德林和法國化學家J.-B.-A.杜馬等人對元素作過分類工作,因當時有許多元素尚未被發現,又沒有公認的測定原子量的方法,只得到了局部的結論。1858年義大利化學家S.坎尼扎羅提出測定原子量的方法,統一的原子量迅速被測定,為發現化學元素間內在聯繫的工作創造了有利的條件。1862年法國化學家A.-E.-B.德尚庫托瓦提出“螺鏇圖”,把已知元素按原子量由小到大循序排在繞著圓柱體的螺線上,某些性質相似的元素排在同一條母線上,如鋰、鈉、鉀、氯、溴、碘、……等,這是化學歷史上第一次提出的元素周期性。當時因巴黎科學院未及時發表,所以未起到應有的作用。1865年英國化學家J.A.R.紐蘭茲把已知元素按原子量由小到大循序排列成表時發現,從任一種元素算起,第8種元素的性質與第1種相似。他把這個規律稱為“八音律”。表的前二列幾乎與現代周期表第2、3周期相應,但因是按原子量大小機械排列,未能揭示元素間的內在聯繫。1869年俄國化學家Д.И.門捷列夫在仔細研究大量資料和前人工作的基礎上提出周期律的基本論點:元素性質是原子量的周期函式。1869年德意志化學家J.L.邁爾也提出一張元素周期表,明確指出元素性質是原子量的周期函式。他的工作偏重於元素的物理性質。
門捷列夫和邁爾的研究結果在同一年發表,表明周期律發現的條件已經成熟,所以發表後不久就得到化學界的公認。
周期系理論 門捷列夫認為:元素性質是原子量的周期函式,原子量決定元素的特徵,同族元素的性質相似,但不是簡單的重複,如氯和碘的性質既相似又有明顯的區別;根據原子量來排列已知元素時,如果遇到性質和元素周期性不符,是原子量值錯誤所致。如已知鈹的當量為4.5,當時誤認為其化合價是3,則原子量為13.5,這樣鈹的位置在碳(原子量為12)和氮(原子量為14)之間,不能反映元素的周期性,他研究了鈹的性質,認為應是2價,原子量為9.0,應把它排在鋰和硼之間。對於當時尚未發現的某些元素,他不僅在周期表中給它們留有空位,並且預言了部分性質。門捷列夫把當時已知的63種元素排成周期表,初步實現了元素的系統化。
周期系理論建立以後又經歷了重要的發展過程。門捷列夫預言的3種元素,鎵於1875年、鈧於1879年、鍺於1886年依次發現,其性質幾乎與預言的完全相同。1894~1899年,6種稀有氣體先後發現,門捷列夫和許多科學家認為應在周期表上增添一個零族,進一步完善了周期系。這樣,周期表就有7個周期9個族,除0和Ⅷ族外,各族均分主副族。1962年合成稀有氣體化合物後,有人主張把原先的0和Ⅷ族改為ⅧA(主)和ⅧB(副)族。1913年英國物理學家H.G.J.莫塞萊由 X射線實驗結果提出原子序數概念。此後對元素周期系的敘述改為:元素性質是原子序數的周期函式。1940年美國化學家E.M.麥克米倫、G.T.西博格合成了93號元素鎿和94號元素鈽。1944~1961年間,西博格等又合成了 95~103號超鈾元素, 後來又合成了104~109號元素。由已經合成的元素性質可知,隨著原子序數的增大,其穩定性急劇降低。如鎿237的半衰期為2.14×106年,鈽244為8.26×107年,而261104為 70秒,261107僅為2×10-3秒,因此曾有人認為人工只能合成110號以前的元素。60年代末,以原子核殼層結構理論為基礎發展起來的超重核穩定島的假設認為,存在一些幻數穩定結構,目前人們正試圖從自然界尋找和在實驗室中合成超重核。
周期表 有長表(見彩圖)、
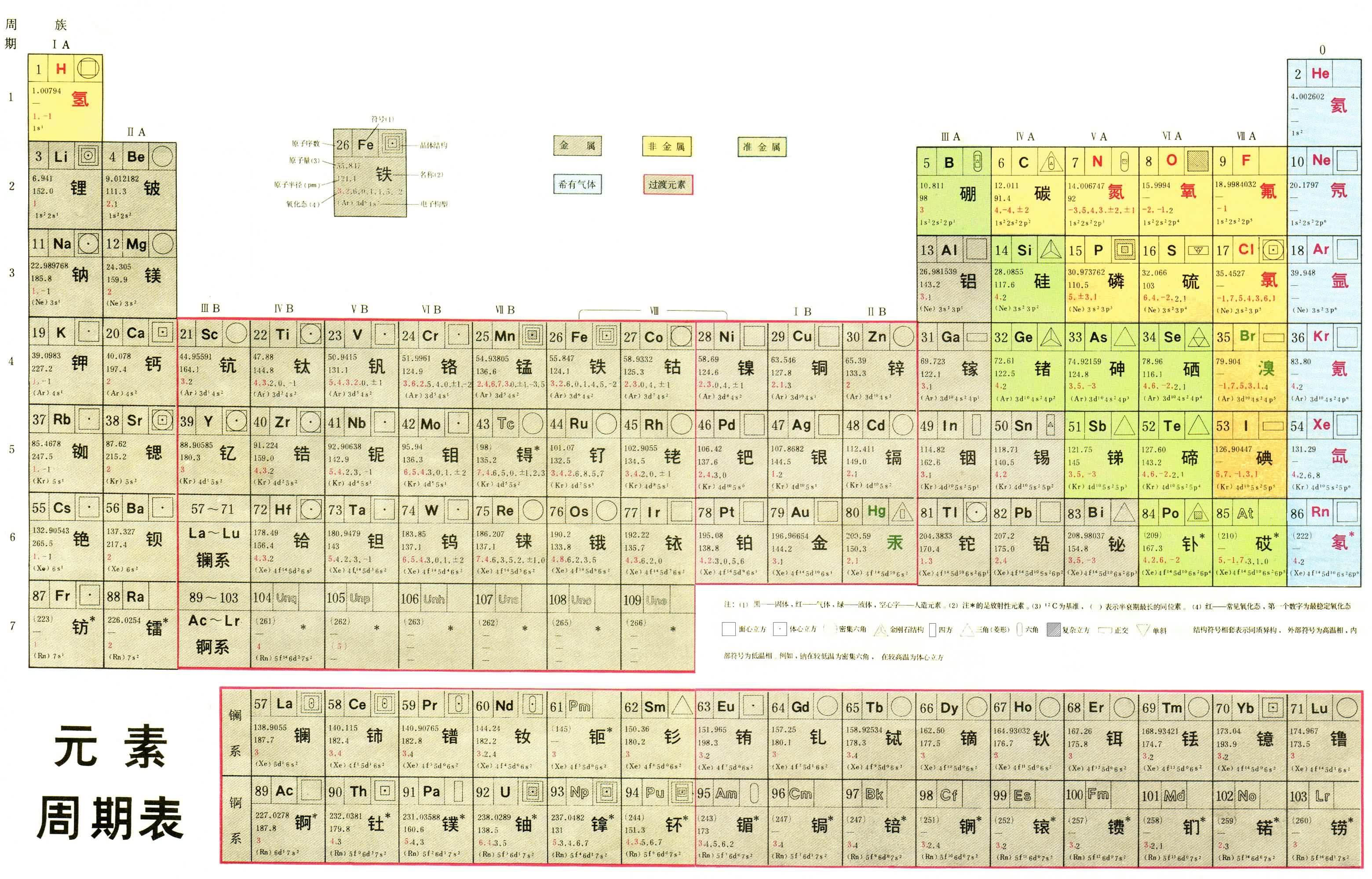 短表兩種。約在1930年前,短表被廣泛套用,目前主要用長表。長表有7個周期、18列和9個族(如把0族和Ⅷ族看作ⅧA和ⅧB族,就只有8個族)。從第4周期開始分主(A)、副(B)族,以第4周期為例,19、20號元素屬ⅠA、ⅡA族,31~35號元素屬ⅢA~ⅦA族,36號元素屬0族,29、30號元素屬ⅠB、ⅡB族,21~25號元素屬ⅢB~ⅦB族,26~28號元素屬Ⅷ族。按照另一分法,19~25號元素屬ⅠA~ⅦA族,26~28號元素屬Ⅷ族,29~35號元素屬ⅠB~ⅦB族,36號稀有氣體元素氪屬0族。
短表兩種。約在1930年前,短表被廣泛套用,目前主要用長表。長表有7個周期、18列和9個族(如把0族和Ⅷ族看作ⅧA和ⅧB族,就只有8個族)。從第4周期開始分主(A)、副(B)族,以第4周期為例,19、20號元素屬ⅠA、ⅡA族,31~35號元素屬ⅢA~ⅦA族,36號元素屬0族,29、30號元素屬ⅠB、ⅡB族,21~25號元素屬ⅢB~ⅦB族,26~28號元素屬Ⅷ族。按照另一分法,19~25號元素屬ⅠA~ⅦA族,26~28號元素屬Ⅷ族,29~35號元素屬ⅠB~ⅦB族,36號稀有氣體元素氪屬0族。 第1周期中有 2種元素,第2、第3周期各有8種元素,第4、第5周期各有18種元素,第6周期有32種元素,第7周期至今只有23種元素。第4、5、6周期中 21~28、39~46、57、72~78號元素是過渡元素。57~71號元素是鑭系元素,89~103號元素是錒系元素。
周期表中各元素性質,如金屬性、非金屬性、氧化物和水化物的酸鹼性……等性質的遞變都很有規律,對於研究和套用化學知識有指導作用。

