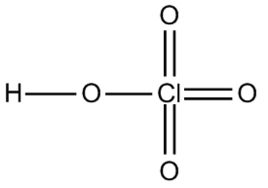
基本性質
物理性質
外觀與性狀:無水物為無色透明的發煙液體,加熱即猛烈爆炸(但市售恆沸高氯酸不混入可燃物則一般不會爆炸)
CAS:7601-90-3
MDL:MFCD00011325
SMILES:O[Cl](=O)(=O)=O
EINECS:231-512-4
熔點(℃):-122
相對密度(水=1):1.76
沸點(℃):130(爆炸)
分子式:HClO4
分子量:100.46
含量:優級純、分析純均在70~72%之間。
飽和蒸氣壓(kPa):2.00(14℃)
溶解性:與水混溶。
酸性:是目前已發現的無機含氧酸中酸性最強的酸。
化學性質
強氧化劑。與有機物、還原劑、易燃物如硫、磷等接觸或混合時有引起燃燒爆炸的危險。在室溫下分解,加熱則爆炸。無水物與水起猛烈作用而放熱。具有強氧化作用和腐蝕性。
化學反應
反應類型
1、高氯酸和鹼金屬、鹼土金屬劇烈反應,猛烈爆炸,生成大量白霧。
2、稀的高氯酸和鎂、鋁等活潑金屬快速反應,生成大量氣泡,放出大量熱。
3、木炭、硫磺和純度較高的高氯酸反應,立刻發生烯燒然後爆炸。
4、高氯酸能鐵、鉻、鎳、鋅等劇烈反應生成氧化物,還能將元素磷和硫分別氧化成磷酸和硫酸。
5、室溫時氧化活性很弱,與Zn、Al、Cr等都不反應,與Sn、Ti、V反應緩慢,但濃熱的高氯酸是強氧化劑可與大多數金屬包括金,銀髮生反應將他們氧化,生成對應的高氯酸鹽和水。濃熱的高氯酸是強氧化劑可與大多數金屬包括金,銀髮生反應將他們氧化,生成對應的“高價金屬高氯酸鹽”和水。
反應式
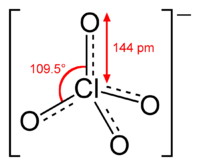 高氯酸
高氯酸高氯酸和五氧化二磷反應:2HClO+2PO→ClO+HPO
高氯酸和硫酸鋇反應:HClO+BaSO→Ba(HSO4)(ClO)
高氯酸和氫氧化鈉反應(放出大量熱):NaOH+HClO→NaClO+HO
高氯酸和氟氣劇烈反應(爆炸):2F+2HClO→2HF+2FClO+O
氫氧化鎂和高氯酸反應:Mg(OH)+2HClO→Mg(ClO)+2HO
氫氧化鋁和高氯酸反應:Al(OH)+3HClO→Al(ClO4)+3HO
高氯酸和氨水反應(放出大量熱):HClO+NH·HO→NHClO+HO
高氯酸和鹽酸反應(氧化還原反應):HClO+7HCl→4Cl+4HO
氫氧化鉀和高氯酸反應(放出大量熱):KOH+HClO→KClO(微溶)+HO
乳酸鈉和高氯酸反應:CHONa+HClO→CHO+NaClO(如果高氯酸比較多,有可能把乳酸的醇羥基氧化為羧基,即變成丙酮酸)。
基本用途
用於電鍍工業、電影膠片、人造金剛石工業、電拋光工業和醫藥工業。也用於生產砂輪除去碳粒雜質。用作強氧化劑。還用於生產煙花和炸藥。50%高氯酸用作丙烯腈聚合物的溶劑。是製造金屬高氯酸鹽的原料。可作化學分析試劑。
可作溶劑,例如可用作高效液相色譜以及丙烯腈聚合物的溶劑;作化學分析試劑,氧化劑,乾燥劑;可作原料,生產煙花,炸藥,金屬高鋁酸鹽;還可用於電鍍工業、電影膠片、人造金剛石工業、電拋光工業和醫藥工業。
使用注意事項
健康危害:該品有強烈腐蝕性。皮膚黏膜接觸、誤服或吸入後,引起強烈刺激症狀。
燃爆危險:該品助燃,具強腐蝕性、強刺激性,可致人體灼傷。
安全術語
1.切勿吸入蒸汽。
2.不慎與眼睛接觸後,請立即用大量清水沖洗並徵求醫生意見。
3.穿戴適當的防護服。
4.若發生事故或感不適,立即就醫(可能的話,出示其標籤)。
管制信息
該品根據《危險化學品安全管理條例》受公安部門管制。
急救措施
皮膚接觸:立即脫去污染的衣著,用大量流動清水沖洗至少15分鐘。就醫。
眼睛接觸:立即提起眼瞼,用大量流動清水或生理鹽水徹底沖洗至少15分鐘。就醫。
吸入:迅速脫離現場至空氣新鮮處。保持呼吸道通暢。如呼吸困難,給輸氧。如呼吸停止,立即進行人工呼吸。就醫。
食入:用水漱口,給飲牛奶或蛋清。就醫。
消防措施
有害燃燒產物:氯化氫。
滅火方法:考慮到火場中可能存在有機物會引起爆炸,不可輕易接近。
滅火劑:霧狀水、泡沫、二氧化碳、砂土。
泄漏應急處理
應急處理:迅速撤離泄漏污染區人員至安全區,並進行隔離,嚴格限制出入。建議應急處理人員戴自給正壓式呼吸器,穿防毒服。不要直接接觸泄漏物。勿使泄漏物與有機物、還原劑、易燃物接觸。儘可能切斷泄漏源。防止流入下水道、排洪溝等限制性空間。
小量泄漏:用砂土、乾燥石灰或蘇打灰混合。
大量泄漏:構築圍堤或挖坑收容。用泵轉移至槽車或專用收集器內,回收或運至廢物處理場所處置。
操作注意事項
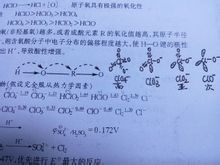 各氧化態氯酸的空間構型圖及其各電勢
各氧化態氯酸的空間構型圖及其各電勢操作注意事項:密閉操作,局部排風。操作儘可能機械化、自動化。操作人員必須經過專門培訓,嚴格遵守操作規程。建議操作人員佩戴過濾式防毒面具(全面罩)或自給式呼吸器,穿聚乙烯防毒服,戴防酸手套。遠離火種、熱源,工作場所嚴禁吸菸。防止蒸氣泄漏到工作場所空氣中。避免與酸類、鹼類、胺類接觸。尤其要注意避免與水接觸。搬運時要輕裝輕卸,防止包裝及容器損壞。禁止震動、撞擊和摩擦。配備相應品種和數量的消防器材及泄漏應急處理設備。倒空的容器可能殘留有害物。稀釋或製備溶液時,應把酸加入水中,避免沸騰和飛濺。
儲存注意事項
儲存注意事項:儲存於陰涼、通風的庫房。遠離火種、熱源。庫溫不宜超過30℃。保持容器密封。應與酸類、鹼類、胺類等分開存放,切忌混儲。儲區應備有泄漏應急處理設備和合適的收容材料。
製備
高氯酸鈉法將氯酸鈉在溶解槽內加水,通入蒸汽於45~50℃下溶解,使其飽和後加入氫氧化鋇除去鉻酸根等雜質,經壓濾,清液送去電解,製得高氯酸鈉。把高氯酸鈉加入反應器,再加入31%鹽酸(用量為理論量的110%~120%)進行複分解反應,生成高氯酸,過濾除去氯化鈉結晶,濾液經蒸發濃縮至高氯酸含量60%以上,製得工業高氯酸。其化學方程式為:
NaClO₃+H₂O→NaClO₄+H₂↑
NaClO₄+HCl→HClO₄+NaCl
工業上使用電解氯酸鈉的方法生產高氯酸鈉, 高氯酸可由高氯酸鈉和濃硫酸經複分解反應製備:
NaClO₄+H₂SO₄(濃)→NaHSO₄+HClO₄(易爆)
還有高氯酸鋇和硫酸反應過濾,以及用硝酸氧化氯酸銨都可製備高氯酸
上游原料:氯酸鈉、鹽酸
下游產品:高氯酸鋰、高氯酸、過氧化二異丙苯