簡介
具有環狀結構的配合物,由具有兩個或多個配位體與同一金屬離子形成螯合環的化學反應——螯合作用而得到。配體和金屬離子間的配位鍵通常有兩種類型:
(1)配體上酸的基團離解去H+,然後與金屬離子配位;
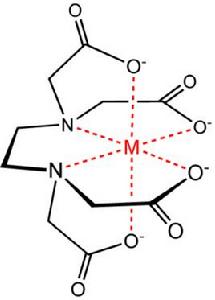
 金屬EDTA螯合物
金屬EDTA螯合物(2)配體上含有孤電子對的中性基團與金屬離子配位.
螯合物最顯著的一種特性是其熱力學穩定性和熱穩定性。螯合環的穩定性與芳香環相似。螯合物可為不帶電荷的中性分子,也可為帶電的絡離子,前者易溶於有機溶液中,後者可溶於水中,此性質可用於分離和分析金屬離子。金屬離子與配體形成螯合物的一般原則是軟硬酸鹼理論,就是:硬親硬,軟親軟。
金屬離子與多齒配體生成的螯合物,比它與單齒配體生成的類似配合物有較高的穩定性。這是由於要同時斷開螯合劑配位於金屬上的兩個鍵是困難的。由螯合作用得到的某些金屬螯合劑用途很廣,例如EDTA為六齒螯合劑,可用於水軟化,食物保存等方面;環狀配體冠醚類對鹼金屬和鹼土金屬的分離和分析特別適用。
配合物
螯合物是(舊稱內絡鹽)是由中心離子和多齒配體結合而成的具有環狀結構的配合物。 螯合物是配合物的一種,在螯合物的結構中,一定有一個或多個多齒配體提供多對電子與中心體形成配位鍵。“螯”指螃蟹的大鉗,此名稱比喻多齒配體像螃蟹一樣用兩隻大鉗緊緊夾住中心體。
螯合物通常比一般配合物要穩定。從配合物的研究可知,具有五元環或六元環的螯合物很穩定,而且所形成的環越多,螯合物越穩定。
螯合反應
又稱螯合作用或螯合效應。螯合配位體 (含兩個或兩個以上具有孤對電子原子的配位體) 與中心離子同時形成兩個或更多的配位鍵而生成環狀結構的配位化合物,即螯合 [物] 的反應。例如,乙二胺四乙酸[EDTA,(—OOCCH2)2NCH2CH2N (CH2COO—)2]能與許多金屬離子如Fe、Th、Hg、Cu、Ni、Pb等通過四個 (有時為三個) 羧酸基和二個氮原子鍵合而形成五個五元螯合環,生成比絡合物具有更高穩定性的金屬——EDTA螯合物。 天然水體和廢水中的金屬發生螯合作用對重金屬元素在環境中的遷移、歸宿或毒性有很大影響。對微量金屬離子有明顯的反應,靈敏度很高。
常見的螯合劑
具有多基配位體能與金屬離子起螯合作用,生成螯合物的試劑。在用水廢水化學中,常用的有有機螯合劑,如氨羧絡合劑 (包括氨基三乙酸即NTA、乙二胺四乙酸即EDTA等)、雙硫腙、8-羥基喹啉、鄰菲咯啉(C12H8N2)、酒石酸鉀鈉、檸檬酸銨及無機螯合劑多磷酸鹽等。螯合劑對各種金屬離子具有較高的選擇性和靈敏度,所生成的金屬螯合物比同類的絡合物具有更好的穩定性。在環境污染化學及化工工業中,常作為絡合滴定劑、金屬指示劑、金屬分離劑、抗氧化劑、掩蔽劑、去鍋垢劑、除藻劑、浮選劑、殺菌劑等。特別在水質分析中,測定水的硬度、金屬離子的濃度等已有廣泛套用 。
可形成螯合物的配體叫螯合劑。常見的螯合劑如下:
乙二胺(en),二齒
2,2'-聯吡啶(bipy),二齒
1,10-二氮菲(phen),二齒
草酸根(ox),二齒
乙二胺四乙酸(EDTA),六齒
值得一提的是EDTA (ethylenediaminetetracetic acid),它能提供2個氮原子和4個羧基氧原子與金屬配合,可以用1個分子把需要6配位的鈣離子緊緊包裹起來,生成極穩定的產物。其化學結構表示如下:
(HOOCCH)NCHCHN(CHCOOH)
相關套用
在水污染化學、分析化學、有機和生化等方面的套用十分廣泛,如水中金屬離子的分離分析、水的軟化、分級沉澱、纖維染色、清洗金屬、浮選、殺菌、蛋白質的水解與合成以及穩定維生素等。
工業工程
螯合物在工業中用來除去金屬雜質,如水的軟化、去除有毒的重金屬離子等。比如重金屬生產和使用的工廠使用重金屬捕捉劑來沉澱重金屬離子,達到淨化廢水的效果。
生物工程
金屬螯合反應對於輔酶、輔因子和酶的結合來說意義重大。
一些生命必須的物質是螯合物,如血紅蛋白和葉綠素中卟啉環上的4個氮原子把金屬原子(血紅蛋白含Fe ,葉綠素含Mg )固定在環中心。
分析化學
螯合物的穩定常數都非常高,許多螯合反應都是定量進行的,可以用來滴定。
化學包覆:在無機粉體表面的吸附或化學反應對顆粒表面螯合有機分子中的官能團進行包覆使顆粒表面改性。
螯合程度的檢測
如果配體和銀離子結合後,紫外可見區有變化,可以用紫外光譜測定反應進行的程度;如果沒有光信號變化,也可以使用電化學手段,用銀-氯化銀電極測定體系游離銀離子濃度;如果是固體的話,只能用溶劑洗滌固體,將游離銀離子洗脫,然後用原子吸收或其他手段檢測銀離子含量。