靶向製劑的定義與分類
 脂質體靶向製劑
脂質體靶向製劑靶向製劑亦稱靶向給藥系統(targeting drug delivery system,TDDS)。系指載體將藥物通過局部給藥或全身血液循環而選擇性地濃集定位於靶組織、靶器官、靶細胞或細胞內結構的給藥系統。
靶向製劑特點:定位濃集、控制釋藥、無毒及生物可降解性等。
靶向製劑主要有如下幾類:
1、被動靶向製劑(passive targeting preparation) 又稱為淋巴系統靶向性。利用脂質體進入體內即被巨噬細胞作為異物吞噬特點形成天然傾向的富集作用。
2、主動靶向製劑 (active targeting preparation)系指用經過修飾的藥物載體作為“飛彈”,將藥物定向地運送到靶區濃集發揮藥效。
3、物理化學靶向製劑 (Physical and chemical targeting preparation) 套用物理化學方法使靶向製劑在特定部位發揮藥效。
脂質體(liposome)的概念
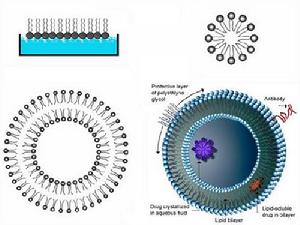
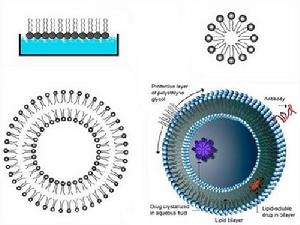
脂質體 (liposome): 系指將藥物包封於類脂質雙分子層內而形成的微型泡囊體。
脂質體的分類
脂質體按照所包含類脂質雙分子層的層數不同,分為單室脂質體和多室脂質體。小單室脂質體(SUV):粒徑約0.02~0.08m;大單室脂質體 (LUV)為單層大泡囊,粒徑在0.1~lm。多層雙分子層的泡囊稱為多室脂質體 (MIV),粒徑在1~5m之間。
脂質體的組成與結構
脂質體的組成:類脂質(磷脂)及附加劑。
1、磷脂類:包括天然磷脂和合成磷脂二類。磷脂的結構特點為一個磷酸基和一個季銨鹽基組成的親水性基團,以及由兩個較長的烴基組成的親脂性基團。
天然磷脂以卵磷脂(磷脂醯膽鹼,PC)為主,來源於蛋黃和大豆,顯中性。
合成磷脂主要有dppp(二棕櫚醯磷脂醯膽鹼)、DPPE(二棕櫚醯磷脂醯乙醇胺)、DSPC(二硬脂醯磷脂醯膽鹼)等,其均屬氫化磷脂類,具有性質穩定,抗氧化性強,成品穩定等特點,是目前國外首選的輔料。
2、膽固醇:膽固醇與磷脂是共同構成細胞膜和脂質體的基礎物質。膽固醇具有調節膜流動性的作用,故可稱為脂質體“流動性緩衝劑”。
脂質體的製備
1、注入法:主要用於製備單室脂質體,少數為多室脂質體,其粒徑絕大多數在2m以下。
2、薄膜分散法:主要用於製備多室或大單室脂質體,超聲後以單室脂質體為主。
3、超音波分散法:主要用於製備以單室為主單室脂質體。
4、逆相蒸發法:將磷脂溶於有機溶劑,加入含藥物的緩衝液,超聲使成穩定w/o乳劑,減壓除去有機溶劑在鏇轉器壁上形成薄膜,加入緩衝液使凝膠脫落,製得水性混懸液,通過凝膠色譜法或超速離心法,除去未包入的藥物,即得大單室脂質體。
5、冷凍乾燥法:適合於熱敏感的藥物。
6、重建脂質體:單室或多室型。是目前國外套用最為廣泛的製備方法之一。其具有工藝穩定、適合於工業化生產、質量易於控制、產品穩定性好等特點。
脂質體的質量控制與評價
1、形態、粒徑及其分布
採用掃描電鏡、雷射散射法或雷射掃描法測定。根據給藥途徑不同要求其粒徑不同。如注射給藥脂質體的粒徑應小於200nm,且分布均勻,呈正態性,跨距宜小。
2、包封率和載藥量
包封率:包封率=(脂質體中包封的藥物/脂質體中藥物總量)×100%
一般採用葡聚糖凝膠、超速離心法、透析法等分離方法將溶液中游離藥物和脂質體分離,分別測定,計算包封率。通常要求脂質體的藥物包封率達80%以上。
載藥量:載藥量=[脂質體中藥物量/(脂質體中藥物+載體總量)]×100%
載藥量的大小直接影響到藥物的臨床套用劑量,故載藥量愈大,愈易滿足臨床需要。載藥量與藥物的性質有關,通常親脂性藥物或親水性藥物較易製成脂質體。
3、脂質體的穩定性
1)、物理穩定性:主要用滲漏率表示。
滲漏率=(放置前介質中藥物量-放置後介質中的藥量)/製劑中藥量x100%
膽固醇以加固脂質雙分子層膜,降低膜流動,可減小滲漏率。
2)、化學穩定性:
(1)磷脂氧化指數:氧化指數=A233nm=A215nm;一般規定磷脂氧化指數應小於0.2。
(2)磷脂量的測定:基於每個磷脂分子中僅含1個磷原素,採用化學法將樣品中磷脂轉變為無機磷後測定磷摩爾量(或重量),即可推出磷脂量。
4、防止氧化的措施:
防止氧化的一般措施有充入氮氣,添加抗氧劑-生育酚、金屬絡合劑等;也可直接採用氫化飽和磷脂。
5、脂質體的滅菌:
滅菌的一般方法有過濾除菌、無菌操作、-射線照射(60鈷15~20kGy)、121℃熱壓滅菌等。
脂質體的特點
1、靶向性和淋巴定向性:肝、脾網狀內皮系統的被動靶向性。用於肝寄生蟲病、利什曼病等單核-巨噬細胞系統疾病的防治。如肝利什曼原蟲藥銻酸葡胺脂質體,其肝中濃度比普通製劑提高了200~700倍。
2、緩釋作用:緩慢釋放,延緩腎排泄和代謝,從而延長作用時間。
3、降低藥物毒性:如兩性黴素B脂質體可降低心臟毒性。
4、提高穩定性:如胰島素脂質體、疫苗等可提高主藥的穩定性。
脂質體作為藥物載體的臨床套用
1、抗腫瘤藥物載體:阿黴素脂質體和順鉑脂質體已在國外上市。
2、抗寄生蟲藥物載體:苯硫咪唑脂質體和阿苯達唑脂質體等。利用脂質體的被動靶向性,提高藥物的生物利用度,減少用量,降低毒副作用。
3、抗菌藥物載體:慶大黴素脂質體和兩性黴素B,可減少藥物的耐藥性,降低心臟毒性。
4、激素類藥物載體。
給藥途徑
脂質體的給藥途徑主要包括(1)靜脈注射;(2)肌內和皮下注射;(3)口服給藥;(4)眼部給藥;(5)肺部給藥;(6)經皮給藥;(7)鼻腔給藥。
脂質體的體內過程
脂質體與細胞之間作用的主要形式包括膜間轉運(細胞膜的脂質交換)、接觸釋藥、吸附、融合和內吞。
脂質體的發展趨勢及存在問題
1. 趨勢:高效、低毒和靶向。
2. 問題:穩定性較差,防止滲漏。